
- •2. Физико-химические свойства газа, газоконденсатной смеси и пластовой воды, используемые при определении термобарических параметров газовых и газоконденсатных пластов и скважин
- •2.1 Составы природных газов (рис 30-31)
- •2.2. Определение физических свойств газа
- •2.2.1. Критические параметры природных газов и их компонентов
- •2.2.2 Фактор ацентричности молекул реальных газов (рис стр.44)
- •2.2.3 Приведенные параметры природных газов (рис 39-40)
- •2.2.4 Плотность газа (рис стр 40-43)
- •2.2.5 Коэффициенты сверхсжимаемости газов (рис стр-44-56)
- •2.2.6 Вязкость газа (рис 56-63)
- •2.2.7 Влагосодержание газа
- •2.2.8 Теплоемкость газа (рис 71-82)
- •2.2.9 Теплопроводность газа (рис 82-87)
- •1÷9 Теплопроводность газов при Рат: 1 – метана, 2 – этана, 3 – азота, 4 – пропана, 5 – n-бутана, 6 – n-пентана, 7 – углекислого газа, 8 – n-гексана, 9 – n-гептана.
- •2.2.10 Дросселирование газа. Коэффициент Джоуля-Томсона. (рис 87-91)
- •2.3 Гидратообразование газов (рис 97-107)
- •2.3.1 Структура и свойства гидратов
- •2.3.2 Методы определения равновесных давления и температуры гидратообразования (рис 101-107)
- •2.4 Определение физических свойств пластовых вод
- •2.4.1 Плотность пластовых вод
- •2.4.2. Вязкость пластовых вод
- •2.4.3 Сжимаемость пластовых вод
- •2.4.4 Растворимость природных газов в воде
2.2.5 Коэффициенты сверхсжимаемости газов (рис стр-44-56)
Коэффициент сверхсжимаемости газов – это отношение объема υ при заданных значениях Р и Т к объему этого газа, определенному при идентичных Р и Т по законам идеального газа υид. Коэффициент сверхсжимаемости характеризует отклонение объема реального газа от объема “идеального”. Формула, связывающая основные параметры газа – объем, давление и температуру, называется уравнением состояния газа. Уравнение состояния идеального газа получено из условия отсутствия межмолекулярных взаимодействий и без учета объема самих молекул и имеет вид
υид=nRT/P (2.19)
где n – число молей газа; R – универсальная газовая постоянная; Т и Р – температура и давление газа.
Уравнение состояния реального газа может быть представлено в виде:
υ=nZRT/P (2.20)
Универсальная газовая постоянная R выражает работу одного моля газа при повышении его температуры на один градус и в системе СИ имеет размерность Дж/кмоль·град.
Коэффициент сверхсжимаемости газа Z зависит от состава газа, давления и температуры. Значение коэффициента может быть определено графическим и аналитическим способами. Способ определения следует выбирать, исходя из требуемой точности его значения. Наиболее простым способом определения Z является графический. Для определения Z природных газов, содержащих не более 2% (мольных) высококипящих углеводородов С5+, 2% ароматических углеводородов и около 5% полярных и кислых компонентов, можно использовать графическую зависимость Z от приведенного давления Рпр и приведенной температуры Тпр, показанных на рисунках 2.4 и 2.5. На рисунках 2.6÷2.8 приведены зависимости Z от Р и Т для N2, CO2 и H2S.
При более высоком содержании в газе высококипящих углеводородов С5+ и полярных компонентов коэффициент сверхсжимаемости Z следует определять с учетом ацентричного фактора по формуле:
Z=Z(0)+ωсмZ(1) (2.21)
где Z(0), Z(1) – коэффициенты, определяемые из графиков зависимостей Z(0) и Z(1) от приведенных параметров Рпр и Тпр, показанных на рисунках 2.9 и 2.10; ωсм – фактор ацентричности, определяемый по известному составу газа по формуле:
 (2.22)
(2.22)
где ωi – фактор ацентричности i-го компонента, определяемый из таблицы 2.2 или по формуле (2.6).
Псевдокритические параметры, необходимые для определения Рпр и Тпр, с помощью которых из графиков находят Z(0) и Z(1), должны быть определены в зависимости от состава газа. Если в газе количество высококипящих углеводородов и полярных веществ более 5%, то псевдокритические параметры должны быть определены согласно [18]:

Рисунок 2.4 – Зависимость коэффициента сверхсжимаемости Z метана от приведенных давления и температуры.

Рисунок 2.5 – Зависимость коэффициента сверхсжимаемости Z природного газа от приведенных давления и температуры.

Рисунок 2.6 – Зависимость коэффициента сверхсжимаемости Z азота от давления и температуры.

Рисунок 2.7 – Зависимость коэффициента сверхсжимаемости Z углекислого газа от давления и температуры.

Рисунок 2.8 – Зависимость коэффициента сверхсжимаемости Z сероводорода от давления и температуры.

Рисунок 2.9 – Зависимость коэффициента сверхсжимаемости Z(0) простых веществ от приведенных давления и температуры.
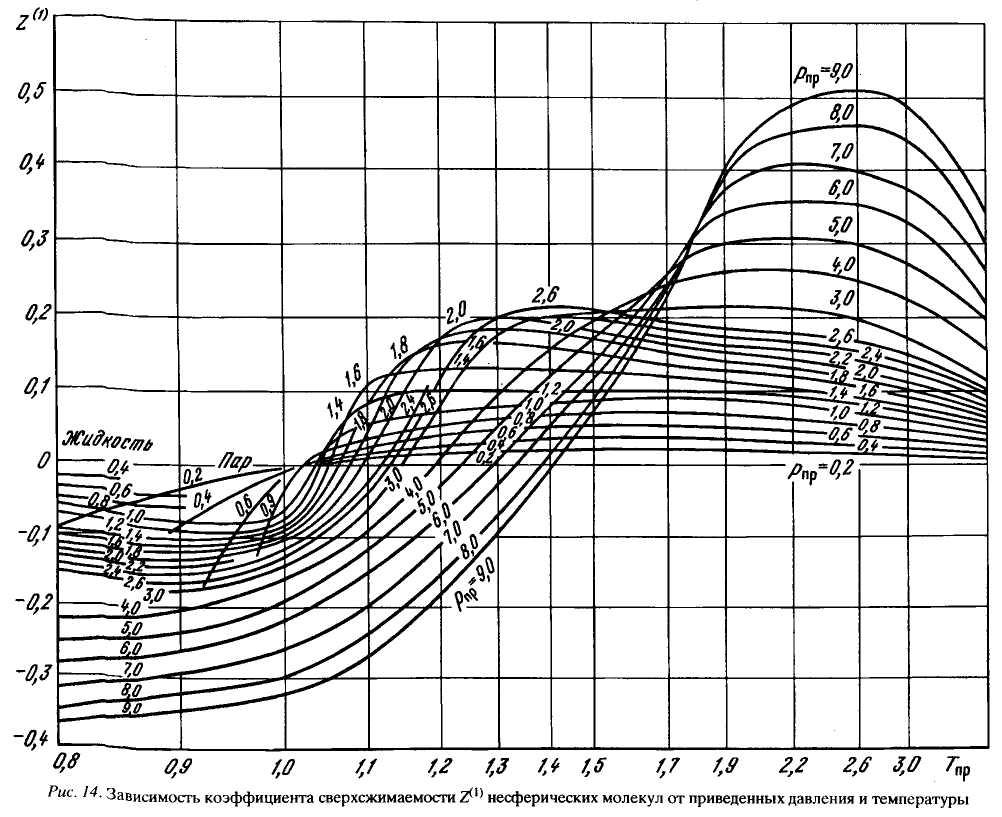
Рисунок 2.10 – Зависимость коэффициента сверхсжимаемости Z(1) несферических молекул от приведенного давления и температуры.
Если в газе содержится более 5% СО2, то значение Z должно быть рассчитано следующим образом:
– по формулам (2.3) вычисляют псевдокритические давление Рпк и температуру Тпк;
– вычисляется фактор ацентричности смеси ωсм, исключая из нее СО2, по формуле:
 (2.23)
(2.23)
– по известной величине ωугл и концентрации СО2 в газе из графика, показанного на рисунке 2.11а и б, определяется величина ε, являющейся температурной поправкой для используемой при расчетах псевдокритической температуры. При наличии в газе СО2 и H2S значение ε может быть рассчитано и по формуле:
![]() (2.24)
(2.24)
где А – суммарные мольные доли СО2 и H2S в газе; В – мольная доля H2S.


Рисунок 2.11 – Зависимость псевдокритической температурной поправки ε от концентрации в смеси СО2 и фактора ацентричности ω.
Зная Рпк, Тпк и ω вычисляют новые псевдокритические параметры:
![]() ;
;
![]() (2.25)
(2.25)

Рисунок 2.12 – Зависимость псевдокритической температурной поправки ε от концентрации в смеси СО2 и H2S.
Зная Рпк, Тпк и ω, вычисляют новые псевдокритические параметры:
По известным величинам заданных Р и Т и вычисленным Р*пк и Т*пк рассчитывают приведенные параметры:
![]()
![]() (2.26)
(2.26)
Используя графики, приведенные в [18] определяют Z(0) и Z(1), а затем, используя формулу (2.21), вычисляют значение Z.
При наличии в газе СО2 и H2S коэффициент сверхсжимаемости Z определяется аналогичным образом, с той лишь разницей, что при вычислении фактора ацентричности ωугл по формуле (2.23) из состава газа исключается не только СО2, но и H2S.
Если для определения газов, содержащих кислые компоненты, т.е. СО2 и H2S, используются графики, показанные на рисунках 2.1 и 2.2, то последовательность расчета выполняется следующим образом:
– по формулам (2.3) рассчитываются значения Рпк и Тпк;
– по графикам из рисунка 2.11 находят поправочный коэффициент ε;
– вычисляются новые псевдокритические параметры по формулам
![]() (2.27)
(2.27)
где xH2S – мольная доля сероводорода в смеси;
![]() (2.28)
(2.28)
Используя формулу (2.26), рассчитывают величины Рпр и Тпр, а затем по этим приведенным параметрам из графика в [18] находят коэффициенты сверхсжимаемости Z(0) и Z(1). По известным Z(0) и Z(1) вычисляют Z.
Для более точных расчетов коэффициент сверхсжимаемости природных газов Z должен быть определен по кубическим уравнениям состояния газов, наиболее широкое распространение, среди которых получили уравнения Соаве, Редлиха-Квонга, Пенга-Робинсона. При этих методах расчета присутствие в газе кислых компонентов практически не влияет на величину погрешности при определении Z, если расчеты ведутся с учетом коэффициентов взаимодействия.
Для определения коэффициента сверхсжимаемости Z кубические уравнения состояния решаются относительно Z. Имеющее достаточно высокую точность уравнение Редлиха-Квонга для определения Z записывается в виде:
![]() (2.29)
(2.29)
где
асм=∑xiai; bсм=∑xibi (2.30)
![]() ;
;
![]() (2.31)
(2.31)
Уравнение (2.29) дает искомую точность для газообразных компонентов и их смесей. Наличие в смеси компонентов в жидком состоянии, а также молекул различного строения резко увеличивает погрешность расчетов.
Повышение точности величины Z при этом возможно путем введения поправки ΔZ на Z, определенной по формуле (2.21).
Наиболее точно коэффициент сверхсжимаемости Z определяется из уравнения состояния Пенга-Робинсона, имеющего относительно Z вид:
См. ниже за таблицей 2.5:
Z3–(l–A)Z2+(A–3B2–2B)Z–(AB–B2–B3)=0, (2.32)
где A=aP/R2T; B=bP/RT; (2.33)
 ;
;
 (2.34)
(2.34)
![]() ;
;
![]() (2.35)
(2.35)
![]() ;
;
![]() (2.36)
(2.36)
Значения коэффициента Cij в формуле (2.34) приведены в таблице 2.5.
Таблица 2.5 – Значение коэффициента Сij в формуле (2.34)
|
Компоненты газа |
Cij | ||||||||||||
|
N2 |
CO2 |
H2S |
CH4 |
C2H6 |
C3H8 |
n-C4H10 |
n-C5H12 |
n-C6H14 |
n-C7H16 |
n-C8H18 |
n-C9H20 |
n-C10H22 | |
|
N2 |
0 |
0 |
0,130 |
0,025 |
0,010 |
0,090 |
0,095 |
0,100 |
0,110 |
0,115 |
0,120 |
0,120 |
0,123 |
|
CO2 |
– |
0 |
0,135 |
0,105 |
0,130 |
0,125 |
0,115 |
0,115 |
0,115 |
0,115 |
0,115 |
0,115 |
0,115 |
|
H2S |
– |
– |
0 |
0,070 |
0,085 |
0,080 |
0,075 |
0,070 |
0,060 |
0,060 |
0,060 |
0,060 |
0,055 |
|
CH4 |
– |
– |
– |
0 |
0 |
0,010 |
0,025 |
0,030 |
0,030 |
0,035 |
0,040 |
0,040 |
0,045 |
|
C2H6 |
– |
– |
– |
– |
– |
0,005 |
0,010 |
0,010 |
0,020 |
0,020 |
0,020 |
0,020 |
0,020 |
|
C3H8 |
– |
– |
– |
– |
– |
0 |
0 |
0,005 |
0,005 |
0,005 |
0,005 |
0,005 |
0,005 |
|
n-C4H10 |
– |
– |
– |
– |
– |
– |
0 |
0,005 |
0,005 |
0 |
0 |
0,005 |
0,005 |
|
n-C5H12 |
– |
– |
– |
– |
– |
– |
– |
0 |
0 |
0 |
0 |
0 |
0 |
|
n-C6H14 |
– |
– |
– |
– |
– |
– |
– |
– |
0 |
0 |
0 |
0 |
0 |
|
n-C7H16 |
– |
– |
– |
– |
– |
– |
– |
– |
– |
0 |
0 |
0 |
0 |
|
n-C8H18 |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
0 |
0 |
0 |
|
n-C9H20 |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
0 |
0 |
|
n-C10H22 |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
0 |
0 |
Более простой вариант
2. Коэффициент сверхсжимаемости газа рассчитываем по формуле Пенга – Робинсона:
![]() ,
(2.22)
,
(2.22)
или
![]() ,
,
где:
![]() ,
,
![]() ,
,
![]() ,
,
![]() ,
,
![]() ,
,
![]() ,
,
![]() ,
,
![]()
