
Взаимодействие макроскопических тел, помещенных в электролит.
rD1 и rD2 - характерный размер двойных электрических слоев,
дебаевские радиусы. Когда на обеих поверхностях одинаковые знаки, то
преобладает отталкивание.
![]()
![]()
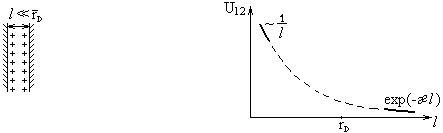
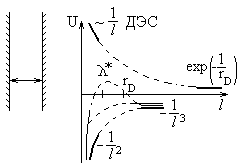 Учтем
молекулярные силы притяжения, силы
двойного электрического слоя, т.е.
рассмотрим общий случай:
Учтем
молекулярные силы притяжения, силы
двойного электрического слоя, т.е.
рассмотрим общий случай:
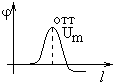
Если концентрация электролита слабая, то ближе к нижней кривой; при повышении концентрации электролита - получим "горб"; если и дальше будем увеличивать концентрацию, то дебаевский радиус отодвинется в лево и "горб" опять исчезнет. Для дистиллированной воды, или масла, rD ~ 1000Å, для обычной воды - rD ~ 10 - 100Å.
В ЗАИМОДЕЙСТВИЕ
МАКРОСКОПИЧЕСКИХ ТЕЛ, РАЗДЕЛЕННЫХ
ПРОСЛОЙКОЙ НА МАЛЫХ РАССТОЯНИЯХ (~30
Å).
ЗАИМОДЕЙСТВИЕ
МАКРОСКОПИЧЕСКИХ ТЕЛ, РАЗДЕЛЕННЫХ
ПРОСЛОЙКОЙ НА МАЛЫХ РАССТОЯНИЯХ (~30
Å).
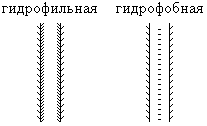 Эти
изменения плотности вблизи поверхности
приводят к дополнительным эффектам
взаимодействия.
Эти
изменения плотности вблизи поверхности
приводят к дополнительным эффектам
взаимодействия.
у поверхности у поверхности
больше меньше
гидрофильное гидрофобное
оталкивание притягивание
Эти силы возникают только при l ~30Å, и называются СОЛЬВАТАЦИОННЫМИ СИЛАМИ.
Что произойдет, если дальше сближать эти поверхности?
Расстояние между молекулами в жидкости порядка размера самих молекул, d ~ Å. При дальнейшем сближении пластин начинает сказываться структура жидкостей.

l1 предпочтительнее, чем l2,
структура жидкости будет сопротивляться.
Т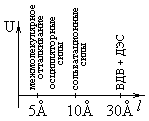 акие
силы называютСТРУКТУРНЫМИ
ОСЦИЛЛЯТОРНЫМИ.
Если подойти на расстояние порядка или
менее 5
Å, то начнется обыкновенное молекулярное
отталкивание.
акие
силы называютСТРУКТУРНЫМИ
ОСЦИЛЛЯТОРНЫМИ.
Если подойти на расстояние порядка или
менее 5
Å, то начнется обыкновенное молекулярное
отталкивание.
Коллоидные системы (растворы).
Это дисперсные системы с размером частиц от 100 Å и до 100 микрон (мкм). Дисперсная среда - жидкость, дисперсные (коллоидные частицы) - капельки другой жидкости.
Микроэмульсия - размер коллоидной частицы меньше длины волны света, лдя них характерно то, что можно создать термодинамичкски устойчивую эмульсию.
ПРОЦЕСС ИСЧЕЗНОВЕНИЯ ЭМУЛЬСИЙ.
- Седиментация
Скорость
седиментации
![]()
- Коагуляция (две частицы, столкнувшись, слипаются. Раствор- эмульсия постепенно исчезает)
- Лиофобные, лиофильные коллоидные растворы
Лиофильные коллоидные системы - самопроизвольно диспергируются и существуют сколько угодно долго (термодинамически устойчива).
F = U - TS
Поверхностная энергия r2 < KT - соответствующая тепловая энергия.
![]() .
.
Лиофильные коллоиды существуют только в случае, когда поверхностное натяжение между дисперсными частицей и средой -- чрезвычайно мало .
Лиофобные растворы - термодинамически неустойчивы. Здесь достаточно большое, поэтому процесс коагуляции идет нормально.
Как можно увеличить жизнь лиофобной системы?
ТЕОРИЯ УСТОЙЧИВОСТИ ЛИОФОБНЫХ КОЛЛОИДОВ
Быстрая коагуляция Предположим, что при некоторой температуре существует
к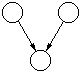 оллоидный
раствор; при каждом столкновении двух
частиц происходит их слияние, концентрация
частиц в растворе уменьшается со
временем. Считается, что скорость
выбывания частиц из раствора вероятности
столкновения~
квадрату концентрации:
оллоидный
раствор; при каждом столкновении двух
частиц происходит их слияние, концентрация
частиц в растворе уменьшается со
временем. Считается, что скорость
выбывания частиц из раствора вероятности
столкновения~
квадрату концентрации:
![]()
![]()
![]()
![]()
![]() - время, за которое концентрация
уменьшается в 2 раза. Если частицы как-то
взаимодействуют между собой (начинает
действовать отталкивание), то
- время, за которое концентрация
уменьшается в 2 раза. Если частицы как-то
взаимодействуют между собой (начинает
действовать отталкивание), то![]() увеличиваеься.
увеличиваеься.
Проведя расчеты, получим:
![]() ;
;![]() ,
еслиUm
>>
kT, то
>> 1.
,
еслиUm
>>
kT, то
>> 1.
При добавлении электролита в раствор происходит увеличение сил двойного слоя, затем 1) дебаевский радиус rD сдвигается влево и эти силы уменьшаются, тогда происходит замедление коагуляции;
2) в-д-в увеличивается.
КОЛЛОИДНЫЕ КРИСТАЛЛЫ:
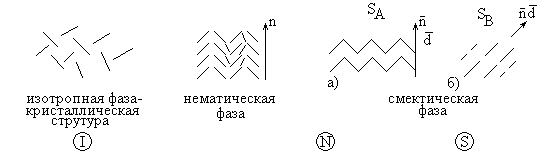
Термотропные жидкие кристаллы - анизотропные молекулы. Для некоторых веществ, обладающих такими молекулами возможно образовать кристаллическую структуру, сохраняя текучесть в определенной области температур.
Т.е. есть кристаллическая симметрия и свойство текучести.
DRыN
HOME OFFICE 2003
