
- •Шарафутдинова в.Г.
- •Раздел I. Материаловедение
- •Тема 1. Введение. Общие сведения о металлах, сплавах и неметаллических материалах
- •Тема 2. Физико-механические свойства материалов и методы их определения
- •Тема 3. Основы теории сплавов
- •Тема 4. Железоуглеродистые сплавы
- •Тема 5. Основы технологии термической обработки материалов
- •Тема 6. Цветные металлы и их сплавы
- •Тема 7. Вспомогательные и неметаллические материалы
- •Тема 8. Поведение материалов в особых условиях. Коррозия металлических материалов и её виды. Защита металлов и сплавов от коррозии
- •Раздел II. Технология материалов
- •Тема 9. Основы технологии производства металлов
- •Тема 10. Основы технологии литейного производства
- •Тема 11. Основы технологии обработки металлов давлением
- •Тема 12. Основы технологии получения неразъёмных соединений
- •Тема 13. Основы технологии обработки материалов резанием
- •Задания к контрольной работе №1 Задание 01
- •Задание 02
- •Задание 03
- •Задание 04
- •Задание 05
- •Задание 06
- •Задание 07
- •Задание 08
- •Задание 09
- •Задание 10
- •Задание 11
- •Задание 12
- •Задание 13
- •Задание 14
- •Задание 15
- •Задание 16
- •Задание 17
- •Задание 18
- •Задание 19
- •Задание 20
- •Задание 21
- •Задание 22
- •Задание 23
- •Задание 24
- •По дисциплине «Материаловедение и технология конструкционных материалов» для слушателей факультета заочного обучения
- •Методические указания к выполнению контрольной работы №1 по дисциплине «Материаловедение и технология материалов»
- •Кривая охлаждения заэвтектоидной стали, содержащей 1,2%с
- •Примерное содержание тестов для подготовки к зачету
- •Диаграммы состояния систем двухкомпонентных сплавов
Методические указания к выполнению контрольной работы №1 по дисциплине «Материаловедение и технология материалов»
т,°с
350
327°С
0 10 20 30 40 50 60 70 80 90 100% Sn
РЬ 100% 90 80 70 60 50 40 30 20 10 0
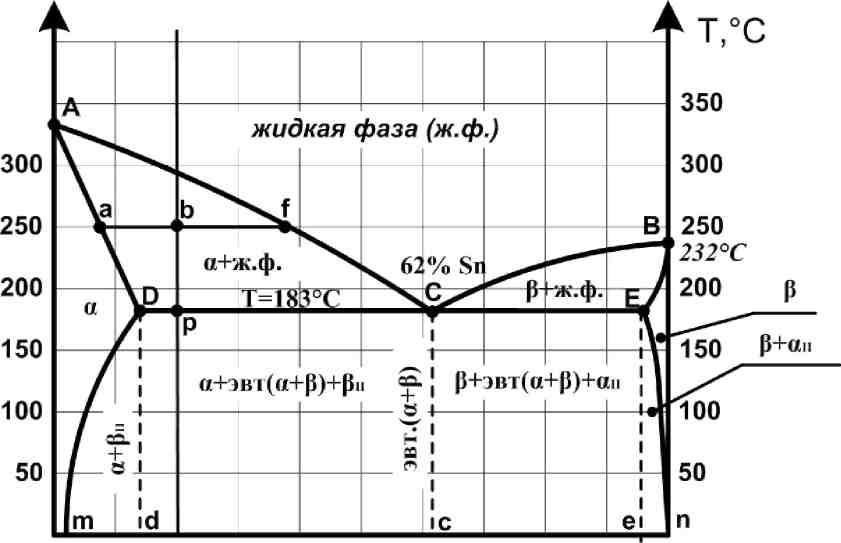
Рис. 1. Диаграмма состояния сплавов системы «свинец Pb - олово Sn»
Диаграмма состояния сплавов системы «свинец Pb - олово Sn» (рис. 1) относится к разновидности диаграмм состояния двойных сплавов III типа, является диаграммой состояния сплавов, испытывающих фазовые превращения в твёрдом состоянии (диаграмма состояния сплавов с переменной растворимостью компонентов в твёрдом состоянии). По внешнему виду диаграмма похожа на диаграмму состояния сплавов с ограниченной растворимостью компонентов в твёрдом состоянии. Отличие только состоит в том, что линии предельной растворимости компонентов не перпендикулярны оси концентрации. На диаграмме имеются области, в которых из однородных твёрдых растворов при понижении температуры выделяются вторичные фазы. Поэтому данный тип диаграммы характерен для сплавов, образующих при сплавлении компонентов твёрдые растворы, имеющих ограниченную взаимную растворимость друг в друге, изменяющуюся с изменением температуры.
Основные линии диаграммы:
ACB — линия ликвидус, линия начала процесса кристаллизации;
ADCEB — линия солидус, линия конца процесса кристаллизации;
27
Dm — линия переменной предельной растворимости олова Sn в свинце Pb;
En — линия переменной предельной растворимости свинца Pb в олове Sn;
DCE — линия кристаллизации эвтектики (T = 183ºC).
Основные точки диаграммы:
A — температура кристаллизации чистого свинца Pb (T = 327ºC);
B — температура кристаллизации чистого олова Sn (T = 232ºC);
C — температура кристаллизации эвтектического сплава 62% Sn + 38% Pb (T = 183ºC);
D — максимальная предельная растворимость олова Sn в свинце Pb (13% олова Sn в 87% свинца Pb при T = 183ºC);
E — максимальная предельная растворимость свинца Pb в олове Sn (4% свинца Pb в 96% олова Sn при T = 183ºC).
На диаграмме условно обозначены следующие фазы:
α — твёрдый раствор олова Sn в основном компоненте-растворителе свинце Pb;
β — твёрдый раствор свинца Pb в основном компоненте-растворителе олове Sn.
Из данной диаграммы видно, что с понижением температуры растворимость олова Sn в свинце Pb и, соответственно, свинца Pb в олове Sn (линии Dm и En соответственно) уменьшаются. Вследствие этого из твёрдых растворов выделяются избыточные фазы, то есть в сплаве образуются равномерно распределённые зоны, содержащие избыточное количество растворённого компонента. Таким образом, из α-твёрдого раствора, например, выделяются вторичные кристаллы β-твёрдого раствора (β II) переменного состава; из β-твёрдого раствора — вторичные кристаллы α-твёрдого раствора (αII). Составы этих вторичных кристаллов определяются соответственно линиями Dm и En.
Причинами выделения вторичных фаз (αII и βII) в сплавах в твёрдом состоянии при понижении температуры являются:
изменение параметров кристаллических решёток основных компонентов-растворителей;
изменение типов кристаллических решёток сплавляемых компонентов при понижении температуры (полиморфное превращение), что приводит к изменению растворяющей способности.
Сплавы составов левее точки m состоят из однородного α-твёрдого раствора — твёрдого раствора олова Sn в основном компоненте-растворителе свинце Pb, а сплавы стоящие правее точки n — из однородного β-твёрдого раствора — твёрдого раствора свинца Pb в основном компоненте-растворителе олове Sn.
Сплавы составов от точки m до точки d имеют микроструктуру, состоящую из кристаллов α-твёрдого раствора переменного состава и вторичных кристаллов β II-твёрдого раствора, а от точки e до точки n — из кристаллов β-твёрдого раствора переменною состава и вторичных кристаллов α II-твёрдого раствора.
На диаграмме также можно выделить следующие сплавы:
Эвтектический сплав (эвтектика). На диаграмме данный сплав соответствует проекции точки С на ось концентраций, содержит 62% олова Sn и 38% свинца Pb. Этот сплав начинает кристаллизоваться при самой низкой температуре 183ºC среди всех сплавов рассматриваемой системы; имеет при понижении температуры постоянный количественный состав компонентов; структура его в твёрдом состоянии представляет собой мелкодисперсную механическую смесь кристаллов α- и β-твёрдых растворов переменного состава.
28
Доэвтектические сплавы, имеющие состав от точки d до точки c состоят из первичных кристаллов α-твёрдого раствора, эвтектики (α + β) и мелких вторичных кристаллов β II-твёрдого раствора, выделившихся из твёрдой фазы при понижении температуры. Первичные кристаллы α-твёрдого раствора равномерно распределены в эвтектике (α + β). Доэвтектические сплавы начинают кристаллизоваться с выделения из жидкой фазы кристаллов α-твёрдого раствора переменного состава (область диаграммы ADC, лежащая между линиями ликвидус и солидус).
Заэвтектические сплавы, имеющие состав от точки c до точки e, состоят из первичных кристаллов β-твёрдого раствора, эвтектики (а + β) и мелких вторичных кристаллов α II-твёрдого раствора, выделившихся из твёрдой фазы при понижении температуры. Первичные кристаллы β-твёрдого раствора равномерно распределены в эвтектике (α + β). Заэвтектические сплавы начинают кристаллизоваться с выделения из жидкой фазы кристаллов β-твёрдого раствора переменного состава (область диаграммы CEB, лежащая между линиями ликвидус и солидус).
Таким образом, в структурно-фазовом составе сплавов рассматриваемой системы важное место занимает эвтектика, представляющая собой смесь мелкодисперсных фаз α и β. Она имеет постоянный количественный состав компонентов (Pb и Sn) и кристаллизуется при наименьшей для данной системы сплавов температуре tэ = 183ºC, т. е. температуре, соответствующей линии DCE. Ниже этой линии находится область двухфазных сплавов.
Выше линии ликвидус (линии ACB) сплавы представляют собой жидкие фазы — неограниченные растворы компонентов (свинца Pb и олова Sn) друг в друге в жидком состоянии.
Для диаграмм состояния сплавов III типа характерно то, что кристаллы сплавляемых компонентов в чистом виде ни в одном из сплавов системы не присутствуют.
Рассмотрим процесс кристаллизации сплава, содержащего 80% Pb и 20% Sn (рис. 2, 3).
Т,°С
350
327°С
 0
10 20 30 40 50 60 70 80 90 100%SnРЬ 100% 90 80 70 60
50 40 30 20 10 0
Кривая охлаждения двойногоt,
МИН
0
10 20 30 40 50 60 70 80 90 100%SnРЬ 100% 90 80 70 60
50 40 30 20 10 0
Кривая охлаждения двойногоt,
МИН
сплавa «80%Pb+20%Sn»
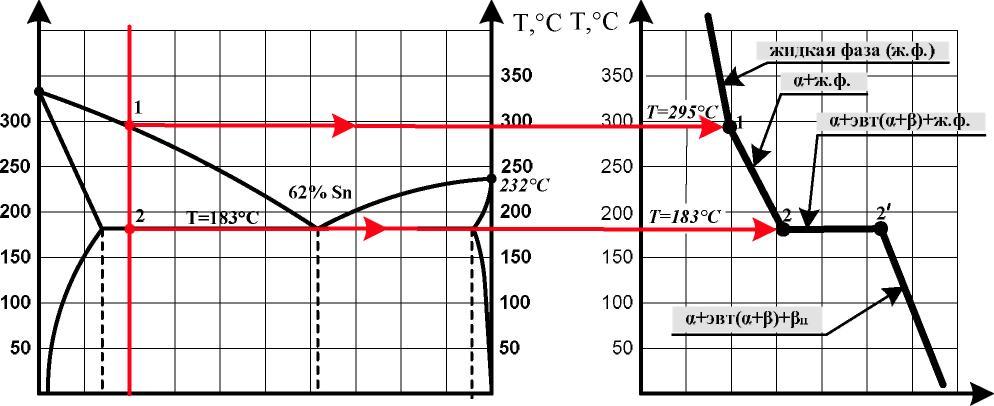
Рис. 2. Построение кривой охлаждения сплава «80% Pb + 20% Sn»
29

Рис. 3. Кривая охлаждения сплава «80% Pb + 20% Sn»
Построение кривой охлаждения сплава «80% Pb + 20%Sn» проводится в следующей последовательности:
а) через точку оси абсцисс, соответствующую составу сплава «80% Pb + 20%Sn», проводится вертикаль — линия сплава (рис. 1, 2);
б) точки пересечения линии сплава с линиями диаграммы обозначаются цифрами (рис. 2). Это — критические точки, указывающие критические температуры начала и конца процесса кристаллизации, перекристаллизации (если она имеется) данного сплава;
в) в соответствии с выявленными критическими температурами строится кривая охлаждения сплава в координатах «температура - время» (рис. 2, 3).
Согласно представленной на рис. 3 кривой охлаждения при кристаллизации сплава «80% Pb + 20%Sn» происходят следующие структурно-фазовые превращения.
При температуре выше точки 1 (T = 295ºC) сплав находится в жидком состоянии (жидкая фаза) и представляется собой неограниченный раствор компонентов (Pb и Sn) друг в друге. Соответственно, точка 1, лежащая на линии ликвидус A C, — температура начала кристаллизации данного сплава.
При охлаждении сплава ниже температуры точки 1 из жидкой фазы начинают выделяться кристаллы α-твёрдого раствора — кристаллы твёрдого раствора олова Sn в основном компоненте-растворителе свинце Pb состава, соответствующему абсциссе точки a, лежащей на линии солидус (линии ADCEB) диаграммы. Таким образом, при понижении температуры количественный состав выделяющихся из жидкой фазы первичных кристаллов α-твёрдого раствора изменяется по линии AD от точки A до D. При этом характер хода кривой охлаждения изменяется, процесс охлаждения замедляется,
что вызвано выделением скрытой теплоты кристаллизации при образовании кристаллов α-твёрдого раствора из жидкой фазы. Поэтому на кривой охлаждения наблюдается излом (участок 1 - 2). Фазовый состав сплава
30
При достижении температуры точки 2 (T = 183ºC, линия DCE диаграммы) возникает нонвариантная система (количество степеней свободы системы C = 0). То есть количество независимых внутренних и внешних параметров системы (температура, давление, концентрация), которые можно произвольно изменять без изменения количества фаз (равновесия) в системе, равно нулю. В данном случае при T = 183ºC (точка 2) в равновесии находятся одновременно три фазы:
жидкая фаза, соответствующая количественному составу точки C диаграммы (62% Sn + 38% Pb);
кристаллы α-твёрдого раствора, количественного состава, соответствующего точке D диаграммы (13% Sn + 87% Pb);
кристаллы β-твёрдого раствора, количественного состава, соответствующего точке E диаграммы (96% Sn + 4% Pb)
При температуре, соответствующей линии DCE — линии кристаллизации эвтектики (T = 183ºC), возникает эвтектическое превращение
LC → α d + βE .
Трём фазам соответствуют определённые количественные составы компонентов, характеризующиеся проекциями точек D, C и E, хотя температура их превращения постоянна.
При кристаллизации сплава между точками 2 и 2′ (T = 183ºC) кроме первичных кристаллов α-твёрдого раствора, образуется также эвтектика (α + β) — мелкодисперсная механическая смесь кристаллов α- и β-твёрдого раствора, количественного состава (62%Sn + 38% Pb). Температура кристаллизации эвтектики постоянна, независимо оттого, что дополнительной теплоты от внешней среды не поступает. Причиной постоянства температуры кристаллизации эвтектики также является выделение скрытой теплоты кристаллизации. В точке 2 эвтектика полностью находится ещё в жидком состоянии, между точками 2 и 2′ — в жидком и твёрдом состояниях, в точке 2′ — полностью в твёрдом состоянии. На участке 2 - 2′ кривой охлаждения фазовый состав сплава — первичные кристаллы α-твёрдого раствора, эвтектика (α + β) и жидкая фаза. В точке 2′ сплав полностью переходит в твёрдое состояние.
При дальнейшем охлаждении сплава ниже точки 2′ из первичных кристаллов α-твёрдого раствора выделяются вторичные кристаллы βII-твёрдого раствора. При обычных температурах кристаллы α-твёрдого раствора сплава имеют количественный состав компонентов, соответствующий точке m диаграммы (2,5%Sn + 97,5% Pb), а кристаллы βII-твёрдого раствора — соответствующий точке n диаграммы (99%Sn + 1% Pb). Причиной выделения вторичных кристаллов βII-твёрдого раствора из α-твёрдого раствора являются: 1) изменение параметров кристаллической решётки компонента-растворителя (свинца Pb), что приводит к снижению его растворяющей способности; 2) структурно-фазовые (полиморфные) превращения кристаллических решёток сплавляемых компонентов, что также приводит к снижению их взаимной растворимости друг в друге.
Окончательно охлаждённый сплав содержит только две фазы — кристаллы
31
α-твёрдого раствора и кристаллы β-твёрдого раствора. Каждый из этих видов кристаллов содержится как в мелкодисперсном состоянии в составе эвтектики (α + β), так и в виде более крупных фаз — α и β, равномерно распределённых по объёму сплава.
Для определения количественного соотношения структурно-фазовых составляющих при температуре 250ºC для сплава, содержащего 20% Sn и 80%
Pb, надо воспользоваться «правилом отрезков».
Для этого в замкнутой области ADC диаграммы на уровне температуры 250ºC проведём горизонтальную линию — коноду abf (рис. 1). Данная линия пересекает вертикальную линию, характеризующую состав сплава (линию сплава), в точке b.
Количество твёрдой фазы Qтв. (количество выпавших кристаллов α-твёрдого раствора) при T = 250ºC определим из соотношения:
bf 18
Q me = — х 100% = — х 100% = 58,06% .
af 31
Таким образом, количество твёрдой фазы Qтв. определяется отношением длины отрезка горизонтали (коноды), прилегающего к линии ликвидус ACB, ко всей длине горизонтали.
Количество жидкой фазы Qж при T = 250ºC определим из соотношения:
bf 13
Qж = — х 100% = — х 100% = 41,94%. af 31
Количество жидкой фазы Qж определяется отношением длины отрезка горизонтали (коноды), прилегающего к линии солидус ADCEB, ко всей длине горизонтали.
Количественный состав выделяющихся при кристаллизации сплава первичных кристаллов α-твёрдого раствора при T = 250ºC определяется абсциссой точки a — 8% Sn + 92% Pb.
Количественный состав жидкой фазы при T = 250ºC определяется абсциссой точки f — 38% Sn + 62% Pb.
Количество образующейся эвтектики при T = 183ºC в точке 2′ составит:
Dp 7
Qэвт = — х 100% = — х 100% = 14,3%
DC 49
Количество образующихся первичных кристаллов α-твёрдого раствора при T = 183ºC составит:
pC 42
Qтв.= — х 100% = — х 100% = 85,7%
DC 49
32


Рис. 4. Микроструктура сплава «80% Pb + 20% Sn»
33
Б) Вычертить диаграмму состояния сплавов системы «железо Fe-углерод C» (рис. П.7). Указать основные линии, точки и структурно-фазовый состав всех областей диаграммы. Для сплава, содержащего 1,2% углерода C, построить кривую охлаждения и описать происходящие при охлаждении структурно-фазовые превращения. Схематично изобразить и описать структуру заданного сплава.

34
На диаграмме железоуглеродистых сплавов (рис. 5) нанесены сплошные и пунктирные линии. Это связано с тем, что углерод в сплавах может находиться как в свободном виде (в виде графита), так и в виде химического соединения (цементита Fe3C). Поэтому, диаграмма состояния железоуглеродистых сплавов может быть:
система «Fe-Fe3C» (метастабильная);
система «Fe-C» (стабильная).
Характерные точки диаграммы:
А (Т= 1539ºC) — температура плавления чистого железа Fe;
В (Т= 1493ºC; 0,5%С) — состав жидкой фазы при перитектической реакции;
J (Т= 1493ºC; 0,18%С) — состав аустенита при перитектической реакции;
Н (Т= 1493ºC; 0,1%С) — состав феррита при перитектической реакции;
N (Т= 1392ºC) — температура полиморфного превращения железа Feα ↔ Feγ;
С (Т= 1147ºC; 4,3%С) — состав эвтектики (ледебурит = аустенит + цементит);
D (Т= 1600ºC; 6,67%С) — условная температура плавления цементита Fe3С;
Е (Т= 1147ºC; 2,14%С) — предельная растворимость углерода в γ-железе Fe;
G (Т= 911ºC) — температура полиморфного превращения железа Feγ ↔ Feα;
S (Т= 727ºC; 0,80%С) — состав эвтектоидного сплава (перлит = феррит + цементит);
Р (Т= 727ºC; 0,02%С) — предельная растворимость углерода в α-железе Feα;
К (Т= 727ºC; 6,67%С) — состав цементита;
Q (Т= 20ºC; 0,006%С) — минимальная растворимость углерода в железе.
Компоненты и фазы железоуглеродистых сплавов
Компонентами железоуглеродистых сплавов являются железо Fe, углерод C и цементит Fe3C.
Железо Fe — переходный металл серебристо-светлого цвета. Имеет высокую температуру плавления — 1539oС ± 5oС.
В твёрдом состоянии железо может находиться в двух модификациях. Полиморфные превращения происходят при температурах 911ºС и 1392ºС. При температуре ниже 911ºС существует α-железо (Feα), обладающее объёмно-центрированной кубической решёткой. В интервале температур 911÷1392ºС устойчивым является γ-железо (Feγ), обладающее гранецентрированной кубической решёткой. Выше 1392ºС железо имеет объёмно-центрированную кубическую решётку и называется (δ-железо (Feδ) или высокотемпературное a-железо (Fea). Высокотемпературная модификация α-железа (Feα) не представляет собой новой аллотропической формы. Критическую температуру 911ºС превращения Feα ↔ Feγ обозначают точкой А3, а температуру 1392ºС превращения Feδ ↔ Feγ — точкой А4.
35
При температуре ниже 768ºС железо ферромагнитно, а выше — парамагнитно. Точка Кюри железа 768ºС обозначается А2.
Железо технической чистоты обладает невысокой твёрдостью (80 НВ) и прочностью (предел прочности — σВ = 250 МПа, предел текучести — σТ = 120 МПа) и высокими характеристиками пластичности (относительное удлинение — δ = 50%, а относительное сужение — ψ= 80%). Свойства могут изменяться в некоторых пределах в зависимости от величины зерна.
Железо характеризуется высоким модулем упругости Е, которым характеризуются и сплавы на его основе, благодаря чему обеспечивается высокая жёсткость и прочность деталей из этих сплавов.
Железо со многими элементами образует растворы: с металлами — твёрдые растворы замещения, с углеродом, азотом и водородом — твёрдые растворы внедрения.
Углерод С относится к неметаллам. Он обладает явлением полиморфизма. В зависимости от условий образования углерод может существовать в форме графита с гексагональной слоистой кристаллической решёткой (температура плавления — 3500ºС, плотность — ρ = 2,25 г/см) или в форме алмаза со сложной кубической решёткой с координационным числом k = 4 (температура плавления — 5000ºС). Графит является мягким материалом и обладает низкой прочностью. Однако с увеличением температуры прочность графита аномально растёт: при 20ºC σВ = 20 МПа, а при 2500ºC σВ = 40 МПа. При 2500ºC графит прочнее всех тугоплавких металлов.
В сплавах с железом углерод образует либо твёрдые растворы внедрения, либо химическое соединение — цементит Fe3C. Также углерод может находиться в свободном состоянии в виде графита (в серых чугунах).
В случае образования твёрдых растворов растворимость углерода в железе зависит от его кристаллической структуры. Размеры пор ОЦК кристаллической решётки значительно меньше, чем размеры пор ГЦК решётки. Поэтому α-железо (Feα) способно растворять углерод в очень малом количестве, а растворимость углерода в γ-железе (Feγ) значительно больше.
В системе железо - углерод существуют следующие фазы: жидкая фаза, феррит, аусте-нит, цементит, графит.
Жидкая фаза. В жидком состоянии железо Fe хорошо растворяет углерод C в любых пропорциях с образованием однородной жидкой фазы.
Феррит (Ф) — твёрдый раствор внедрения углерода в a-железе Feα.
Феррит имеет переменную предельную растворимость углерода: минимальную — 0,006% при комнатной температуре (точка Q), максимальную — 0,02% при температуре 727ºС (точка P). Углерод располагается в дефектах кристаллической решётки железа.
При температуре выше 1392ºС существует высокотемпературный феррит с предельной растворимостью углерода С (0,1%) в δ-железе Feδ при температуре 1499ºС (точка H).
Свойства феррита близки к свойствам железа. Он мягок (твёрдость — 130 НВ, предел прочности — σв = 300 МПа) и пластичен (относительное удлинение — δ = 30%), обладает магнитными свойствами до 768ºС.
Аустенит (А)— твёрдый раствор внедрения углерода С в γ-железе Feγ.
В аустените углерод занимает место в центре гранецентрированной кубической ячейки. Аустенит имеет переменную предельную растворимость углерода: минимальную — 0,8% при температуре 727ºС (точка S), максимальную — 2,14% при температуре 1147ºС (точка Е).
36
Аустенит имеет твёрдость 200…250 НВ, пластичен (относительное удлинение его составляет — δ = 40… 50%), обладает парамагнитными свойствами.
И в феррите и в аустените могут растворяться многие легирующие элементы, образуя твёрдые растворы замещения и резко изменяя их свойства. Кроме того, легирование может значительно изменять температурные границы существования фаз.
Цементит (Ц) (Fe3C) — химическое соединение железа с углеродом (карбид железа), содержащее 6,67% углерода С.
Цементит не испытывает полиморфных превращений при изменении температуры. Кристаллическая решётка цементита состоит из ряда октаэдров, оси которых наклонены друг к другу.
Температура плавления цементита точно не установлена (по разным данным она составляет 1250ºС или 1550ºС). При низких температурах цементит слабо ферромагнитен. Магнитные свойства он теряет при температуре около 217ºС.
Цементит имеет высокую твёрдость (более 800 НВ, легко царапает стекло), но очень низкую, практически нулевую, пластичность. Такие свойства являются следствием сложного строения кристаллической решётки цементита. Цементит способен образовывать твёрдые растворы замещения. Атомы углерода C могут замещаться атомами неметаллов: азотом N, кислородом O; атомы железа Fe — металлами: марганцем Mn, хромом Cr, вольфрамом W и др. Такой твёрдый раствор на базе решётки цементита получил название легированный цементит.
Цементит — соединение неустойчивое и при нагреве распадается с образованием свободного углерода в виде графита. Этот процесс имеет важное практическое значение при структурообразовании чугунов.
В железоуглеродистых сплавах выделяют три вида цементита в зависимости от температуры образования: цементит первичный (ЦI), цементит вторичный (ЦII), цементит третичный (ЦIII). Химические и физические свойства этих фаз одинаковы. Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих фаз в сплавах. Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зёрен аустенита (при охлаждении — вокруг зёрен перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ зёрен феррита.
Характерные линии и области диаграммы
ABCD — линии ликвидус — линия начала процесса кристаллизации Выше линии ликвидус (область I) сплав находится в жидком состоянии и представляет собой однородную систему — жидкий раствор.
AHJECF — линия солидус — линия завершения процесса кристаллизации. Сплавы, лежащие ниже этой линии, находятся в твёрдом состоянии. При температурах между линиями ликвидус и солидус происходит кристаллизация сплавов. В период кристаллизации одновременно существуют две фазы — жидкий расплав и кристаллы твёрдых растворов.
37
Рассматривая линию ликвидус ABCD, можно отметить, что с увеличением содержания углерода С в железе до 4,3% температура плавления сплава понижается, а с дальнейшим повышением содержания углерода (участок CD) температура плавления сплава увеличивается.
На участке линии ликвидус АВ выделяются кристаллы δ-твёрдого раствора (феррита Ф), состав которых определяется линией АН. Состав жидкой фазы изменяется по линии АВ. Предельную растворимость углерода (0,1%) в δ-железе Feδ (феррите Ф) при температуре 1493°С показывает точка Н.
На участке АН заканчивается кристаллизация феррита Ф. На линии HJB при постоянной температуре 1499°С жидкая фаза, содержащая 0,5% С (точка В), реагирует с ранее выпавшими кристаллами δ-твёрдого раствора (феррита Ф), что приводит к образованию кристаллов нового вида. Реакцию подобного вида называют перитектической (перитектическое превращение). В результате этой реакции образуются кристаллы аустенита А, содержащего 0,18% С (точка J):
L + Ф(δ) → А.
По линии HN начинается превращение феррита Ф(δ) в аустенит А, обусловленное полиморфным превращением железа. По линии NJ заканчивается превращение феррита Ф(δ) в аустенит А.
По линии ВС при понижении температуры из расплава выпадают кристаллы аустенита А переменного состава, с меньшим содержанием углерода (от 0,5 до 2,14%), чем в жидкой фазе, из которой они выделяются. Изменение состава жидкой фазы с понижением температуры происходит по линии ВС (линия ликвидус), а выпавших кристаллов — по линии JE (линия солидус). На участке JЕ заканчивается кристаллизация аустенита А.
Таким образом, если сплавы содержат до 2,14% С, то их кристаллизация заканчивается при температуре выше 1147°С, где жидкая фаза обогащается углеродом до 4,3%. Одновременно из расплава выпадают кристаллы аустенита, содержащие 2,14% С (точка Е) и цементита, содержащего 6,67% С (точка F).
На участке ECF при постоянной температуре 1147ºС идёт эвтектическое превращение, заключающееся в том, что жидкость, содержащая 4,3% углерода превращается в эвтектическую смесь аустенита А и цементита первичного ЦІ:
L4,3 → эвт. (А + ЦI).
Ледебурит (Л) (точка С) — механическая эвтектическая смесь (эвтектика) кристаллов аустенита А и цементита Ц, содержащая 4,3% C. Эвтектика системы железо - цементит называется ледебуритом Л, по имени немецкого учёного Ледебура.
Сплавы, лежащие праве точки С, т. е. содержащие от 4,3 до 6,67% С, кристаллизуются по линии CD. В процессе их кристаллизации выделяется первичный цементит Fe3C (ЦI). По мере образования из жидкого расплава первичного цементита (Ц I) содержание углерода в жидкой фазе уменьшается.
При температуре 1147°С (линия CF) оставшийся расплав содержит 4,3% С и затвердевает с образованием ледебурита (эвтектики). В результате окончательно затвердевший сплав (ниже линии CF) состоит из первичного цементита (ЦI) и ледебурита Л.
Сплавы, находящиеся левее точки С, т. е. содержащие до 4,3% С, называются доэвтектическими, а сплавы находящиеся правее от точки С, т. е. содержащие более 4,3% С, — заэвтектическими. Между линиями ликвидус ABCD и солидус AHJECF (области II и III) железоуглеродистые сплавы состоят из жидкой и твёрдой фаз, причём с понижением температуру количество твёрдой фазы увеличивается.
38
Таким образом, непосредственно после окончания затвердевания структура доэвтектических сплавов состоит из аустенита А и ледебурита Л, структура эвтектического сплава — из ледебурита Л и структура заэвтектического сплава — из первичного цементита (Ц I) и ледебурита Л.
Ниже линии солидус AHJECF в затвердевших сплавах при понижении температуры наблюдается дальнейшее изменение их структуры, связанное с перекристаллизацией в твёрдом состоянии. Такие изменения называют вторичной кристаллизацией. С понижением температуры железо переходит из одной модификации в другую (Feγ → Feα) и растворимость углерода в γ-железе Feγ и α-железе Feα заметно уменьшается.
По линии PSK при постоянной температуре 727ºС идёт эвтектоидное превращение, заключающееся в том, что аустенит А, содержащий 0,8% углерода С, превращается в эвтекто-идную смесь феррита Ф и цементита вторичного ЦII:
А0,83 → эвт. (Ф + ЦII)
По механизму данное превращение похоже на эвтектическое, но протекает в твёрдом состоянии. Эвтектоид системы железо - цементит называется перлитом (П), он содержит 0,8% углерода С. Название такое эта фаза получила за то, что на полированном и протравленном шлифе наблюдается перламутровый блеск. Перлит может существовать в зернистой и пластинчатой форме, в зависимости от условий его образования.
Доэвтектические сплавы (до 2,14% С) в области IV состоят из одного аустенита А При охлаждении сплавов, содержащих менее 0,8% С (левее точки S), ниже линии GOS происходит распад аустенита А с выделением из него избыточного феррита Ф, что обусловлено полиморфным превращением железа Fe. Так как феррит Ф, выделяющийся при охлаждении аустенита А по линии GOS, содержит не более 0,02% С (предельная растворимость углерода в α-железе Feα, точка Р), аустенит А несколько обогащается углеродом С, изменяя состав по линии GS. Кристаллы феррита изменяют свой состав по линии GOS.
Такой процесс протекает до температуры 727°С. В точке S при 0,8% С аустенит А распадается на твёрдую эвтектоидную механическую смесь кристаллов феррита Ф и цементита Ц, называемую перлитом П. Пользуясь правилом отрезков по диаграмме состояния, можно определить соотношение феррита Ф и цементита Ц в перлите при 727°С
Qф/Qц = SK/PS = (6,67 - 0,8)/0,8 =7,3375,
где Q — количество вещества.
Внешне зерно перлита состоит из параллельных пластинок феррита и цементита. Чем грубее и крупнее выделения цементита, тем хуже механические свойства перлита.
Сплавы, содержащие 0,8% С называются эвтектоидными, содержащие менее 0,8% С — доэвтектоидными, и содержащие более 0,8% С — эаэвтектоидными.
При охлаждении сплавов, лежащих правее точки S и содержащих более 0,8% С, ниже линии SE происходит распад аустенита А с выделением из него вторичного цементита ЦII, обусловленный снижением растворимости углерода в аустените при понижении температуры. Так как выделяющийся вторичный цементит ЦII содержит 6,67% С, концентрация углерода в остающимся аустените А изменяются (уменьшается) по линии SE до состава точки S (0,8% С) при 727°С.
39
Таким образом, доэвтектоидные сплавы в области VIII состоят из аустенита А и феррита Ф, а в области IX — из феррита Ф и перлита П. Заэвтектоидные сплавы (0,8 - 2,14% С) в области V состоят из аустенита А и вторичного цементита ЦII, а в области Х — из вторичного цементита ЦII и перлита П.
Сплавы, содержащие от 2,14 до 4,3% С, выше линии PSK, но ниже линии ECF (область VI) состоят из аустенита А, вторичного цементита ЦII и ледебурита Л.
По линии PSK и ниже в этих же сплавах (область XI) происходит превращение аустенита А в перлит П; структура сплава состоит из перлита П, цементита Ц и вторичного ледебурита ЛII. Сплавы, соответствующие эвтектической точке С, ниже линии PSK имеют структуру одного ледебурита Л.
Сплавы, содержащие 4,3 - 6,7% С, ниже линии CF, но выше линии PSK (область VII) состоят из цементита Ц и первичного ледебурита ЛI; ниже линии PSK (область XII) сплавы сохраняют эту же структуру.
По линии PG происходит превращение аустенита А в феррит Ф заканчивается. Также в нижней левой части диаграммы линия PQ показывает уменьшение растворимости углерода в α-железе Feα (феррите Ф) с понижением температуры. По линии PQ из феррита Ф начинается выделение третичного цементита ЦІІІ, обусловленное снижением растворимости углерода в феррите при понижении температуры. Следовательно, сплавы между точками Р и Q состоят из феррита Ф и третичного цементита ЦІІІ.
Сплавы, находящиеся внутри области GPQ, состоят только из феррита Ф.
По линии МО при постоянной температуре 768ºС имеют место магнитные превращения сплава.
Температуры, при которых происходят фазовые и структурные превращения в сплавах системы железо - цементит, т. е. критические точки, имеют условные обозначения.
Обозначаются они буквой А (от французского arret — остановка):
А1 — линия PSK (727ºС) — превращение П ↔ А;
A2 — линия MO (768ºС, — точка Кюри — магнитные превращения);
A3 — линия GOS (переменная температура, зависящая от содержания углерода в сплаве) — превращение Ф ↔ А;
A4 — линия NJ (переменная температура, зависящая от содержания углерода в сплаве)
— превращение А ↔ Ф ( δ);
Acm — линия SE (переменная температура, зависящая от содержания углерода в сплаве)
— начало выделения цементита вторичного ЦІІ (иногда обозначается A3).
Так как при нагреве и охлаждении превращения совершаются при различных температурах, чтобы отличить эти процессы вводятся дополнительные обозначения. При нагреве добавляют букву с, т. е. Ас1, при охлаждении - букву r, т. е. Аr1.
Все сплавы, характеризующиеся диаграммой Fe-C, разделяют на: техническое железо (< 0,006% C), стали (0,006 < C < 2,14%) и чугуны (2,14 <C <6,67%).
Построим кривую охлаждения для сплава, содержащего 1,2% углерода С (см. рис. 6).
40
