
- •1.1.1 Рабочее тело
- •1.1.2 Состояние рабочего тела. Параметры состояния.
- •1.2. Газовые смеси Характеризуются законом Дальтона, который гласит:
- •1.3. Понятие о равновесном и обратимом процессах.
- •1.4. Теплоемкость газов.
- •1.5. Первый закон термодинамики.
- •1.5.1. Уравнение первого закона термодинамики.
- •1.6. Функции состояния и функции процесса.
- •1.7. Энтропия как параметр состояния идеального газа.
- •1.8. Работа газа при неравновесном процессе.
- •1.8. Исследование газовых процессов.
- •Политропные процессы
- •I Закон термодинамики для потока газа .
- •II-й закон термодинамики.
- •Круговые процессы (циклы).
- •Цикл Карно.
- •Т1 и т2 - температуры горячего и холодного источников тепла
- •Эквивалентный цикл Карно
- •Пример:
1.3. Понятие о равновесном и обратимом процессах.
Уравнение состояния справедливо для газа, находящегося в покое. Такое состояние называется равновесным, т.е. когда параметры одинаковы по всему объему.
Для выведения его из этого состояния, необходимо воздействие окружающей среды, т.е. необходим процесс. Процесс – любое изменение состояния рабочего тела.
В зависимости от взаимодействия со средой процесс может быть равновесным и неравновесным.
Равновесный термодинамический процесс – когда в любой момент рабочее тело находится в равновесном состоянии.
Первым условием равновесности термодинамического процесса можно считать бесконечно малую разность давлений рабочего тела и окружающей среды.
![]()
Бесконечно малая разность температур рабочего тела и окружающей среды.
![]()
Равновесный процесс должен протекать бесконечно медленно.
Для изменения направления равновесного процесса, достаточно только изменить знак у приращения давления и приращения температуры. dP и dT. При совершении такого процесса в одном, затем в другом направлении в системе не произойдет никаких изменений. Поэтому равновесный процесс при отсутствии трения называется обратимым процессом.
В теоретических циклах все процессы обратимы.
В реальных двигателях процессы считают равновесными или квазиравновесными, но в следствии трения этот процесс необратим.
1.4. Теплоемкость газов.
Теплоемкостью газа называется количество тепла, которое необходимо подвести к нему в данном процессе, чтобы поднять температуру единицы количества газа на один градус.
Cp – при изобарном процессе (p=const)
Cv – при изохорном процессе (V=const)
Обычно двух теплоемкостей достаточно, но процессов в технике очень много, столько же может быть и теплоемкостей.
Cp всегда больше Cv
![]() - уравнение Майера.
- уравнение Майера.
В зависимости от выбранной единицы количества газа различают:
Массовую теплоемкость
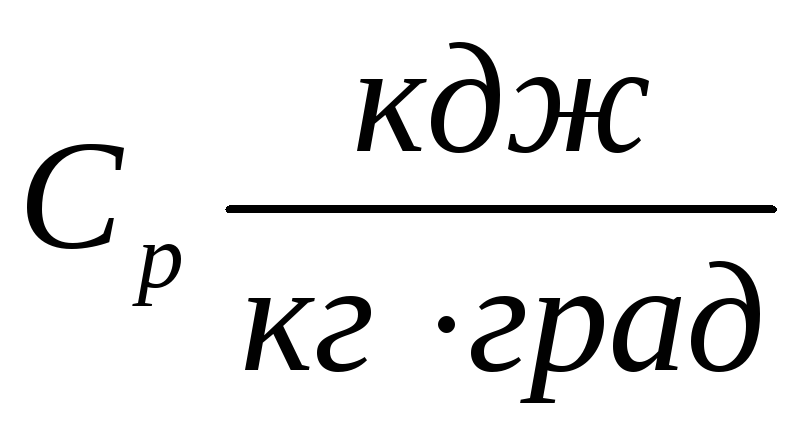
Объемную теплоемкость
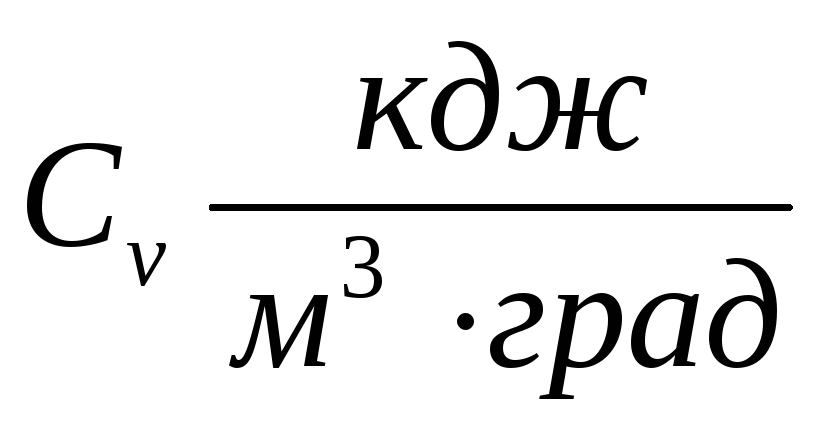
Мольную теплоемкость

Различают истинную и среднюю теплоемкости:
![]() - средняя теплоемкость
в процессе 1-2
- средняя теплоемкость
в процессе 1-2
![]() - истинная
теплоемкость в процессе 1-2
- истинная
теплоемкость в процессе 1-2
а) Массовая теплоемкость (Сv и Cvm; Cp и Cpm)
б) Объемная теплоемкость (С/v и C/vm; C/p и C/pm)
в) Мольная теплоемкость (Сv и Cvm; Cp и Cpm)
Зависимость между ними:
![]()
![]()
![]() - удельный объем
газа при нормальных условиях.
- удельный объем
газа при нормальных условиях.
![]()
Молекулярно-кинетическая теория вещества устанавливает следующие значения мольных теплоемкостей для идеального газа. В зависимости от атомности.
|
Газ |
ккал/моль град |
кдж/моль град |
| ||
|
|
|
|
| ||
|
Одноатомный Двухатомный Многоатомный |
3 5 7 |
5 7 9 |
12,6 20,9 29,3 |
20,9 29,3 37,8 |
1,67 1,40 1,29 |
К- показатель адиабаты.
Эти теплоемкости используются при грубых расчетах, т.к. теплоемкость здесь не зависит от других параметров.
В действительности теплоемкость газов зависит от температуры (а также и других параметров)
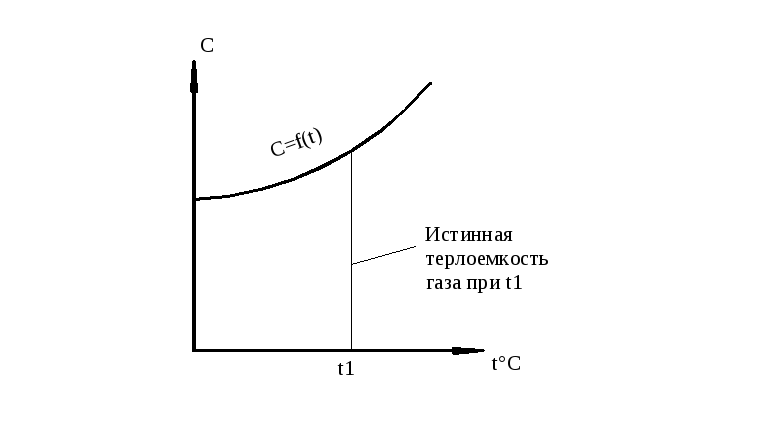
![]() полиномная
зависимость теплоёмкости от температуры
полиномная
зависимость теплоёмкости от температуры
Средняя теплоемкость газа. Расчет количества подведенного тепла.
![]()
![]()

Рис. Зависимость теплоёмкости от температуры.
![]()
В справочниках обычно представлены теплоемкости от нуля градусов до t.
![]() - средняя теплоемкость
в интервале от 0 до t2
- средняя теплоемкость
в интервале от 0 до t2
![]() -
средняя теплоемкость в интервале от 0
до t1
-
средняя теплоемкость в интервале от 0
до t1
При неточном
расчете (С=const),
то
![]()
Пример.
Определить массовую теплоемкость CO2 при P=const, считая C=const.
![]()
Пример.
Дано: V=const; m=5 кг; t1=15 град. Цельсия; t2=215 град. Цельсия; С=const; O2.
Найти: q=?
Решение:
![]()
![]()
![]()
