
ekzamenacionnye_voprosy
.docx«Утверждено»
Проректор по учебной работе
д.м.н., профессор
Ходжаян А.Б.
«_____»______________2014
. «Согласовано» декан лечебного факультета
к.м.н., доцент
Кошель И.В.
«___»______________2014г.
Экзаменационные вопросы по общей химии для студентов 1 курса на 2014 - 2015 учебный год
-
Первое начало термодинамики. Энтальпия. Эндотермические и экзотермические реакции, примеры
-
. Понятия о самопроизвольно протекающих процессах. Энтропия - как функция состояния системы. Зависимость энтропии от агрегатного состояния вещества, его природы и температуры.
-
Дайте определение понятиям: стационарное состояние, равновесное состояние, переходное состояние. Параметры системы и функции состояния.
-
Энергия Гиббса – критерий самопроизвольного протекания изобарно-изотермических процессов в закрытых системах. Экзэр- и эндэргонические процессы.
-
Энергия Гиббса. Прогнозирование направления самопроизвольно протекающих процессов в изолированных и закрытых системах. Термодинамические условия равновесия. Роль энтальпийного и энтропийного факторов.
-
Скорость гомогенных реакций. Средняя и истинная скорость химической реакции. Перечислите факторы, влияющие на скорость гомогенной реакции.
-
Зависимость скорости реакции от температуры. Правило Вант-Гоффа. Температурный коэффициент и его физический смысл.
-
Теория активных столкновений. Природа энергии активации. Переходное состояние. Ответ поясните, используя энергетический профиль течения экзотермической реакции.
-
Энергия активации реакции и взаимосвязь ее с константой скорости реакции. Уравнение Аррениуса
-
. Катализ. Общие положения. Положительный и отрицательный катализ. Гомогенный и гетерогенный катализ.
-
Ферментативный катализ. Химическая природа ферментов и их биологическая роль. Отличия ферментов от неорганических катализаторов. Специфичность ферментов.
-
Зависимость скорости ферментативной реакции от: а) температуры; б) рН среды; в) концентрации фермента. Ответ поясните с использованием графиков.
-
Особенности кинетики ферментативной реакции. Графическая зависимость влияния концентрации субстрата на скорость ферментативной реакции (при постоянной концентрации фермента). Уравнение Михаэлиса-Ментен и его анализ.
-
Общее положение теории сильных электролитов Дебая-Хюккеля. Активность и коэффициент активности ионов
-
Какие растворы называются: изотонические, гипотонические, гипертонические. Их роль в медицине.
-
Что такое осмос? Напишите формулы для расчета осмотического давления для электролитов и неэлектролитов
-
. Коллигативные свойства разбавленных растворов неэлектролитов. Закон Рауля и следствия из него: понижение температуры кристаллизации, повышение температуры кипения растворов, осмос
-
Что такое изотонический коэффициент Вант-Гоффа (i). Напишите формулу для его расчета, объясните его значение.
-
Дайте определение понятиям: осмос, осмотическое давление, онкотическое давление. Напишите формулы для расчета Росм. для неэлектролитов и электролитов, крови.
-
Дайте определение кислотам Бренстеда. Укажите типы кислот, приведите примеры. Для написанных вами кислот укажите сопряженные основания.
-
Объясните, что такое амфолиты согласно теории Бренстеда и Лоури на примере гидрокарбонат-аниона
-
Протолитические реакции. Основные положения протолитической теории кислот и оснований, молекулярные и ионные кислоы и основания. сопряженная протолитическая пара, амфолиты. Водородный показатель
-
Дайте определение водородному показателю, выведите его, исходя из ионного произведения воды.
-
Перечислите типы протолитических реакций, приведите пример реакции ионизации.укажите сопряженные кислотно-основные пары.
-
Буферное действие – главный механизм протолитического гомеостаза организма. Механизм буферного действия, количественные характеристики буферных систем. Расчет pH протолитических систем
-
Дайте определение понятию «буферная система». Приведите примеры катионной и анионной буферной систем.
-
Выведите рН буферных систем на примере гидрокарбонатного буфера (уравнение Гендерсона-Гассельбаха). Объясните, от каких факторов зависит рН буферного раствора.
-
Что называют буферной емкостью раствора? От каких факторов она зависит? Зона буферного действия
-
Перечислите буферные системы, функционирующие в цельной крови и плазме. Приведите сравнительную характеристику их емкости.
-
Приведите состав гидрокарбонатной буферной системы и покажите механизм ее действия.
-
Как называются состояния, характеризующиеся отклонением значения рН крови от нормы? Объясните, почему большинство буферных систем организма имеет буферную емкость по кислоте больше, чем по основанию?
-
Алкалоз, ацидоз, виды и причины возникновения
-
Объясните строение комплексных соединений согласно координационной теории Вернера. Для ответа используйте пример комплексного соединения, в состав которого входит комплексный анион
-
Какие свойства проявляют лиганды и комплексообразователь в комплексных соединениях? Какова степень окисления и координационное число комплексообразователя в комплексах [Pt(NH3)2Cl4] , [Cr(H2O)5Cl]Cl2.
-
Объясните с позиции принципа мягких и жестких кислот и оснований токсичность ионов тяжелых металлов.
-
Константы нестойкости комплексных ионов [Co(NH3)6]3+, [Fe(CN)6]4-, [Fe(CN)6]3- соответственно равны 6,2∙10-36, 1,0∙10-37, 1,0∙10-44. Какой из этих ионов является более прочным? Для этого иона напишите выражение константы нестойкости
-
Что называется дентантностью лиганда? Приведите примеры моно-, би- и полидентантных лигандов. Определите дентантность воды и щавелевой кислоты.
-
Физико-химические основы хелатотерапии. Приведите примеры препаратов, применяемых в хелатотерапии, напишите формулы и назовите их.
-
Регуляция образования костной ткани с помощью витаминов, гормонов и рН среды
-
В какой последовательности будут осаждаться малорастворимые электролиты AgCI, AgBr, AgI, если к раствору, содержащему ионы CI-,Br-, I- постепенно добавлять AgNO3 (Ks(AgCI)=1,8.10-10, (Ks(AgBr)=5,0.10-13, Ks(AgI)=8,3.10-17)? Ответ поясните
-
Константы растворимости Ks (Ag2SO4)=1,8 .10 -5 и Ks (CaSO4)=2,4. 10-5
величины одного порядка. Одинаковы ли молярные растворимости этих солей? Ответ обосновать с помощью расчетных формул
-
Явление изоморфизма: замещение в гидроксиапатите гидроксид-ионов на ионы фтора, ионов кальция на ионы стронция. Остеотропность металлов. Реакции, лежащие в основе образования конкрементов: уратов, оксалатов, карбонатов. Применение хлорида кальция и сульфата магния в качестве антидотов
-
Объясните, почему радионуклид Sr90 легко включается в состав костной ткани. Чем опасно замещение части ионов кальция на ионы Sr90 для организма? Стронциевый и бериллиевый рахит
-
Химизм процесса формирования костной ткани в остеобластах и факторы этому способствующие.
-
В чем заключается механизм возникновения окислительно-восстановительного потенциала? Какие факторы влияют на величину окислительно-восстановительного потенциала? Уравнение Нернста-Петерса
-
Объясните связь величин ЭДС и ΔG. Укажите может ли данная реакция протекать самопроизвольно:
-
SnCl2 + FeCl3
 SnCl4
+ FeCl2
, если φ0(Sn4+/Sn2+)
= +0,15 B;
φ0(Fe3+/Fe2+)
= +0,77 B.
Ответ поясните с помощью расчетов.
SnCl4
+ FeCl2
, если φ0(Sn4+/Sn2+)
= +0,15 B;
φ0(Fe3+/Fe2+)
= +0,77 B.
Ответ поясните с помощью расчетов. -
. Укажите направление реакции
-
2MnO2 + 3I2 + 8OH- ↔ 2MnO4- + 6I- + 4H2O при стандартных условиях, если φ0(MnO4-/MnО2) = +0,60 B; φ0(I2/2I-) = +0,54 B. Ответ поясните с помощью расчетов.
-
Можно ли окислить раствор бромоводорода с помощью раствора перманганата калия и дихромата калия, если φ0(Br2/2Br-) = +1,07 B; φ0(MnO4-/Mn2+) = +1,54 B; φ0(Cr2O72-/2Cr3+)=1,33 В? Ответ подтвердите расчетами
-
Какой из галогенид-ионов (хлорид, бромид, иодид) необходимо взять для осуществления реакции:
-
2KHal + 2FeCl3
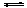 Hal2
+ 2KCl + 2FeCl2еслиφ0(Fe3+/Fe2+)
= +0,77 B; φ0(Cl2/2Cl-)
= +1,36 B; φ0(I2/2I-)
= +0,54 B; φ0(Br2/2Br-)
= +1,07 B? Ответ
подтвердите расчетом.
Hal2
+ 2KCl + 2FeCl2еслиφ0(Fe3+/Fe2+)
= +0,77 B; φ0(Cl2/2Cl-)
= +1,36 B; φ0(I2/2I-)
= +0,54 B; φ0(Br2/2Br-)
= +1,07 B? Ответ
подтвердите расчетом. -
Сформулируйте правило Дюкло-Траубе? Приведите примеры, иллюстрирующие это правило, с использованием изотермы поверхностного натяжения.
-
Поверхностная энергия Гиббса и поверхностное натяжение. Дайте определение, покажите их взаимосвязь
-
Что такое ПАВ? Как зависит поверхностное натяжение от концентрации ПАВ в растворе и расположения их в поверхностном слое? Изобразите графически.
-
Адсорбция газов на твердых телах. Уравнение Ленгмюра, его анализ. Изотерма Ленгмюра
-
Сформулируйте основные положения теории адсорбции Ленгмюра. Факторы влияющие на адсорбцию газов на твердом адсорбенте.
-
Сформулируйте правила Панета-Фаянса, и его практическое применение
-
Особенности энергетического состояния молекул в поверхностном слое и объеме фазы. Свободная поверхностная энергия, зависимость величины свободной поверхностной энергии от удельной свободной поверхностной энергии (поверхностное натяжение) и площади по-верхностного раздела фаз.
-
Изменение поверхностной активности в гомологических рядах (правило Траубе). Изотерма адсорбции. Ориентация молекул в поверхностном слое и структура биомембран. Поверхностное натяжение биожидкостей в норме и патологии
-
Какие молекулы называются ПАВ, ПИВ, ПНВ. Поведение этих молекул в полярных и неполярных растворителях
-
Физико-химические основы процесса гемосорбции.
-
Формирование поверхностного слоя в гетерогенных системах жидкость-газ. СЭП и пути её изменения.
-
Золь бромида серебра получен в избытке бромида калия. Изобразите схематически строение мицеллы, укажите составляющие компоненты.
-
Золь сульфита бария получен в результате реакции:
Ba(NO3)2 + K2SO3 → BaSO3↓ + 2KNO3. Изобразите схематически строение мицеллы и укажите знак и заряд гранулы, если стабилизатором будет K2SO3. Укажите составляющие компоненты.
-
Золь хлорида серебра получен реакцией ионного обмена в избытке хлорида натрия. Изобразите схематически строение мицеллы и укажите знак и величину заряда гранулы. Укажите составляющие компоненты.
-
Золь иодида серебра получен в избытке нитрата серебра. Представьте схематически строение мицеллы, и объясните, от чего зависит знак и величина заряда гранулы. Укажите составляющие компоненты.
-
Золь сульфата бария получен реакцией двойного обмена в избытке сульфата калия. Изобразите схематически строение мицеллы, укажите потенциалопределяющие ионы. Укажите составляющие компоненты.
-
Золь берлинской лазури Fe4[Fe(CN)6]3 получен в избытке К4[Fe(CN)6]. Представьте схематически строение мицеллы, и объясните, от чего зависит знак и величина заряда гранулы. Укажите составляющие компоненты.
-
Перечислите и охарактеризуйте конденсационные методы получения золей.
-
Классификация дисперсных систем
-
Виды устойчивости дисперсных систем. Какими факторами обуславливаются эти виды устойчивости?
-
Виды диализа. Применение диализа в биологии и медицине.
-
Всегда ли при протекании химической реакции образуется мицелла? Назовите основные условия получения неорганического коллоидного раствора. Объясните на конкретном примере образование и строение любой мицеллы.
-
На какие стадии делится процесс коагуляции? Опишите признаки каждой стадии.
-
Механизм и кинетика электролитной коагуляции. Нейтрализационная и концентрационная коагуляция.
-
Какие молекулярно-кинетические свойства характерны для дисперсных систем? Сравните интенсивность этих свойств в коллоидных и истинных растворах
-
Устойчивость дисперсных систем. Седиментационная, агрегационная и конденсационная устойчивость лиозолей
-
Свойства растворов ВМС. Особенности растворения ВМС как следствие их структуры. Форма макромолекул. Механизм набухания и растворения ВМС. Зависимость величины набухания от различных факторов.
-
Устойчивость растворов биополимеров. Высаливание биополимеров из растворов. Коацервация и ее роль в биологических системах. Застудневание растворов ВМС. Свойства студней: сенерезис и тиксотропия
-
Понятие о мембранном равновесии Доннана
-
Свойства растворов ВМС (набухание, застудневание, вязкость, осмо-тическое давление). Факторы, влияющие на набухание и застуднева-ние. Биологическое значение набухания, студней.
-
Нарушение устойчивости растворов ВМС: высаливание, денатурация, коацервация. Значение этих явлений в биологии и медицине.
Зав. кафедрой общей
и биологической химии К.С.Эльбекьян
