
- •Министерство образования и науки рф
- •Предмет коллоидной химии
- •Глава I.Дисперсные системы:
- •1.1 Основные свойства дисперсных систем
- •1.2 Классификация дисперсных систем
- •Классификация по степени дисперсности
- •Классификация по агрегатному состоянию
- •Классификация по структурно-механическим свойствам
- •Раздел II. Поверхностные явления. Адсорбция
- •2.1 Классификация поверхностных явлений
- •Классификация поверхностных явлений
- •2.2 Поверхностное явление – адсорбция
- •2.2.1 Основные понятия и определения
- •2.2.2 Адсорбция на границе жидкость-газ
- •2.2.3. Адсорбция на твердом адсорбенте
- •2.3 Адгезия и смачивание
- •Раздел III. Электрические свойства дисперсных
- •3.1 Возникновение электрического заряда
- •3.2 Современные представления о строении
- •3.3Строение мицеллы гидрофобного золя
- •3.4. Факторы, влияющие на электрокинетический потенциал
- •3.4.1 Влияние температуры
- •3.4.2 Влияние электролитов
- •3.4.3 Влияние рН среды
- •3.4.4 Влияние природы дисперсионной среды
- •3.5 Электрокинетические явления
- •3.5.1 Электрофорез
- •3.5.2 Потенциал седиментации
- •3.5.3 Электроосмос
- •3.5.4 Потенциал течения
- •Раздел IV. Устойчивость и нарушение устойчивости лиофобных золей
- •4.1. Седиментационная устойчивость
- •4.2 Агрегативная устойчивость и коагуляция
- •4.2.1 Теория устойчивости гидрофобных золей длфо
- •4.2.2 Факторы, определяющие агрегативную устойчивость
- •4.3. Коагуляция гидрофобных дисперсных систем
- •4.3.1 Коагуляция золей электролитами
- •Явление неправильных рядов
- •4.3.2 Кинетика коагуляции
- •Теория быстрой коагуляции Смолуховского
- •Константа скорости медленной коагуляции
- •Раздел V. Оптические свойства дисперсных систем
- •5.1. Рассеяние света
- •Теория светорассеяния Рэлея
- •5.2. Поглощение света и окраска золей
- •5.3. Оптические методы исследования коллоидных растворов
- •Раздел VI. Молекулярно-кинетические свойства
- •6.1. Броуновское движение
- •6.2. Диффузия
- •6.3. Осмос
- •Раздел VII. Виды дисперсных систем
- •7.1. Растворы высокомолекулярных соединений (вмс)
- •7.1.1. Классификация вмс
- •7.1.2. Особенности строения полимеров
- •7.1.3. Набухание вмс
- •Термодинамика набухания
- •Кинетика набухания
- •Факторы, влияющие на набухание
- •7.1.4. Свойства растворов вмс
- •7.2. Коллоидные пав. Мицеллообразование в растворах пав
- •Применение коллоидных пав
- •7.3. Эмульсии
- •7.3.1. Классификация эмульсий
- •7.3.2. Методы получения эмульсий
- •7.3.3. Устойчивость эмульсий
- •Типы эмульгаторов
- •7.3.4. Применение эмульсий
- •7.4. Пены
- •7.4.1. Основные характеристики и классификация пен
- •7.4.2. Устойчивость пен
- •7.4.3. Методы разрушения пен
- •7.4.4. Практическое применение пен
- •7.5. Золи и суспензии
- •7.6. Порошки
- •7.6.1. Основные свойства и устойчивость порошков
- •7.6.2. Практическое применение порошков
- •Раздел VIII. Структурообразование в дисперсных системах
- •8.1. Типы структур в дисперсных системах
- •8.2. Особенности структурообразования в растворах вмс. Студни и студнеобразование
4.2.2 Факторы, определяющие агрегативную устойчивость
коллоидных систем
Адсорбционно-ионный фактор.
Обусловлен наличием на поверхности частиц двойного электрического слоя и -потенциала. Чем больше силы отталкивания, тем выше потенциальный барьер, и тем более устойчива коллоидная система. Силы отталкивания обусловлены одноименным зарядом частиц, величина которого определяется электрокинетическим потенциалом. Следовательно, чтобы увеличить силы отталкивания необходимо повысить-потенциал. (см п. «Влияние различных факторов на-потенциал).
Электрокинетический потенциал тем выше, чем шире ДЭС и выше потенциал ядра φ0.
Для того, чтобы увеличить φ0-потенциал, необходимо ввести в золь стабилизатор, т.е. неиндифферентный электролит, повышающий потенциал ядра, а следовательно, и-потенциал. Например, в золь
![]()
можно добавить небольшое количество NaCl. Так как Сl–иI–изоморфные ионы, то Сl–будет адсорбироваться на поверхности агрегатаAgI, в результате φ0и-потенциал увеличатся.
Для повышения -потенциала при неизменном φ0-потенциале необходимо увеличить толщину диффузного слоя, которая пропорциональна:
![]() .
.
Из уравнения видно, что толщина диффузного слоя увеличивается с повышением температуры и понижением ионной силы раствора.
Следовательно, для увеличения устойчивости системы необходимо уменьшить концентрацию противоионов, что достигается при очистке золя. При этом происходит дезагрегация коллоидных частиц (уменьшение размера) или, если выпал осадок, переход его в коллоидное состояние (пептизация).
При повышении температуры усиливается броуновское движение частиц, в результате чего устойчивость также увеличивается.
Структурно-механический фактор.
Заключается в том, что в систему вводят стабилизаторы – высокомолекулярные соединения, ПАВ, которые адсорбируются на поверхности частиц, образуя 3-х-мерную защитную оболочку, не позволяющую частицам сближаться на критическое расстояние.
В качестве стабилизаторов в пищевой промышленности применяют желатин и другие белки. Однако введение стабилизаторов не всегда способствует повышению устойчивости. Необходимо правильно подбирать необходимую концентрацию стабилизатора. Если добавить недостаточное количество стабилизатора, то его макромолекула своими концами может адсорбироваться сразу на нескольких частицах, связывая их мостиками (рис. 40).
В
Рис. 40.
Образование флокул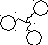
4.3. Коагуляция гидрофобных дисперсных систем
Коагуляция – процесс слипания частиц дисперсной фазы с образованием крупных агрегатов.
Коагуляция является следствием нарушения агрегативной устойчивости лиофобных золей. В результате коагуляции система теряет свою седиментационную устойчивость, так как частицы становятся слишком крупными и не могут участвовать в броуновском движении. Разрушение коллоидной системы идет в следующей последовательности:
Нарушение Нарушение
агрегативной → Коагуляция → седиментационной
устойчивости устойчивости
Коагуляция идет самопроизвольно, так как приводит к уменьшению межфазной поверхности, а следовательно, и к снижению свободной поверхностной энергии (Gпов = S).
Различают две стадии коагуляции:
медленная (скрытая) коагуляция: частицы укрупняются, но не теряют седиментационной устойчивости;
быстрая (видимая) коагуляция:частицы теряют седиментационную устойчивость, при этом, если плотность частиц больше плотности дисперсионной среды, образуется осадок.
Количественной характеристикой
коагуляции является скорость
коагуляции. Скорость коагуляции vк
– это изменение
концентрации коллоидных частиц
![]() в единицу времени τ при постоянном
объеме системы:
в единицу времени τ при постоянном
объеме системы:
![]() .
.
Знак “–“ стоит перед производной, так как концентрация частиц со временем уменьшается, а скорость всегда положительна.
Чтобы началась коагуляция, частицы должны преодолеть потенциальный барьер ΔUк. Для этого необходимо уменьшить-потенциал. Экспериментально установлено, что коагуляция начинается при30 мВ.
Как можно уменьшить -потенциал?
1) снизить температуру;
2) добавить электролиты.
Рассмотрим механизм коагуляции гидрофобного золя электролитами.
