
- •Синтез органического соединения
- •Цель работы и полученное задание.
- •II Синтез заданного органического соединения
- •III Расчет количеств исходных веществ, необходимых для синтеза
- •Примечание:
- •Отчет должен быть написан на бумаге стандартного формата а4. Левое поле страницы - не менее 30 мм. Номера страниц – по центру внизу страницы.
- •2.1. Расчет основных исходных веществ
- •2.2) Расчет количества вспомогательных веществ
2.2) Расчет количества вспомогательных веществ
Рассчитываем количество вспомогательных веществ по пропорции, исходя из заданного количества исходного в-ва.
В данном синтезе в качестве вспомогательных веществ применяются кальций хлорид безводный (количество не указано, рассчитывать не требуется), а также дистиллированная вода в количестве 20 см3.
Из условия методики данного синтеза известно, что
для 29 см3 этилового спирта необходимо 20 см3 Н2О дистиллированной воды,
а для 50 см3 этилового спирта ––––– Х см3,
тогда
VН2О = (50х20)/29 = 34,5 см3
Таким образом, для синтеза бромистого этила необходимо:
50 см3 96% этилового спирта,
50,74 г бромистого калия,
54,89 см3 98% серной кислоты.
34,5 см3 дистиллированной воды.
Полученные данные заносим в таблицу 2.3.
Таблица 2.3. – Количество исходных веществ, применяемых в синтезе
|
Реагент |
Число моль |
Избыток, % |
В граммах |
Объем, см 3 |
|
|
химически чистого |
раствора |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Запишем новое мольное соотношение: С2Н5ОН : KBr : Н2SО4 = 0,82 : 0,43 : 1,01.
д) Расчет теоретического выхода
Для расчета теоретического выхода бромистого этила (БЭ), необходимо определить в-во, которое находится в недостатке. Из нового мольного соотношения видно, что KBr находится в недостатке. Из уравнения реакции следует, что из 0,43 моль бромида калия (продукт, взятый в недостатке) должно быть получиться 0,43 моль бромистого этила. Поэтому теоретический выход бромистого этила равен:
ТВЭBr = 0,43109 = 46,9 г
е) Ожидаемый выход бромистого этила можно рассчитать по пропорции, учитывая, что по этой методике (стр.18) из 30 г бромистого калия образуется 22 г бромистого этила:
30 г КВr 22 г бромистого этила (БЭ), тогда из
51,2 г KBr Х г БЭ
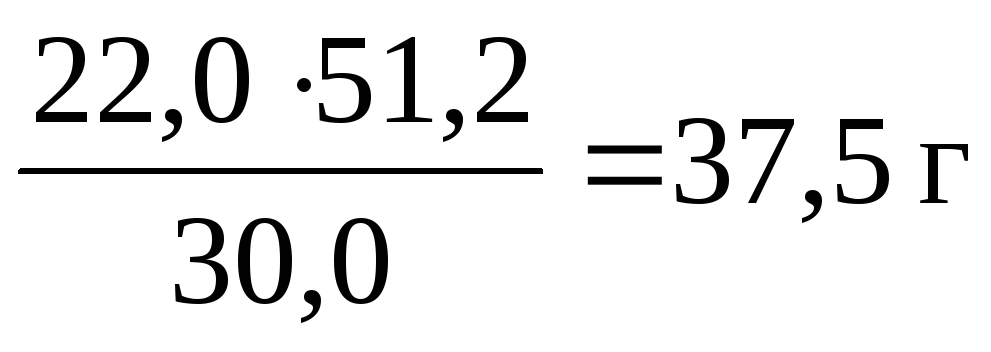
Тогда процентный выход ожидаемый от теоретического будет составлять:
![]()
ж) Практический выход определяется после окончания синтеза и очистки бромистого этила.
