
Проблемы экологии автотранспорта / volume1
.pdf
1-НИТРО- И 1-БРОМ-1-НИТРО-3,3,3-ТРИХЛОРПРОПЕНЫ В РЕАКЦИИ С 2,3-ДИМЕТИЛ-1,3-БУТАДИЕНОМ
Слободчикова Е.К., Анисимова Н.А., Берестовицкая В.М.
ФГБОУ ВП «Российский государственный педагогический университет имени А.И. Герцена», 191186, Россия,
г. Санкт-Петербург, наб. р. Мойки, 48, kohrgpu@yandex.ru
Циклогексеновое кольцо входит в состав многих природных соединений (терпенов, гормонов, алкалоидов, витаминов и др.), а также синтетических лекарственных средств. Поэтому разработка методов синтеза новых функционализированных шестичленных карбоциклов является важной задачей не только с теоретической точки зрения, но и в прикладном аспекте.
Нами исследовано химическое поведение 1-нитро- и 1-бром- 1-нитро-3,3,3-трихлорпропенов (1,2) в реакциях диенового синтеза с представителем алифатических диенов – 2,3-диметил- 1,3-бутадиеном.
Наблюдение за ходом реакции с использованием спектроскопии ЯМР1Н показало, что реакция начинается уже при комнатной температуре в первые часы взаимодействия и продолжается в течение 30 дней. Увеличение температуры реакции (80оС) путем кипячения реакционной смеси в бензоле позволяет сократить время реакции до 1 часа.
В результате получены 1-нитро- и 1-бром-1-нитро-2,3- диметил-6-трихлорметил-3-циклогексены (3,4) с количественными выходами (95-98%). Строение синтезированных нитроциклогексенов установлено на основании анализа их ЯМР1Н и ИК спектров.
181
ВЛИЯНИЕ ФОНА НА РАВНОВЕСИЯ В РАСТВОРАХ ОРГАНИЧЕСКИХ КИСЛОТ
Смирнов А.К., Смирнова Л.Г., Аль Ансари С.В.
ФГБОУ ВПО «Марийский государственный университет”, 424000, Россия, г. Йошкар-Ола, пл. Ленина, 1; aksmi@yandex.ru
В настоящей работе была поставлена задача оценки значимости ионной силы (I = 0,1-3,0) и природы фонового электролита (KCl, KBr, KI, KNO3, NaNO3) при определении констант кислотности на примере биологически актуальных α- кетоглутаровой и янтарной кислот потенциометрическим методом.
Титрование проводили стандартным раствором гидроксида натрия, содержащим фоновый электролит для устранения изменения ионной силы в процессе титрования за счет разбавления. Измерения ЭДС цепи
Ag, AgCl|HCl|стекло|H2L, фон|KCl|AgCl,Ag
проводили при 293 (±0,1) К на иономере pH-150М с комбинированным стеклянным электродом. Анализ экспериментальных результатов выявил следующее:
-ионная сила оказывает значимое влияние на расчётные значения констант равновесия;
-значения pki проходят через минимум, соответствующий
I=0,6–0,7;
-применимость метода Шварценбаха для рассматриваемых систем ограничивается растворами с I > 1,5;
Ограниченность модели Дебая-Хюккеля, используемая при описании подобных систем, не позволяет объяснить природу и положение экстремумов зависимостей констант ионизации, что требует постановки дополнительных экспериментов и корректировки её модельных представлений.
Работа выполнена при финансовой поддержке Федерального агентства по образованию (Темплан НИР ГОУВПО “МарГУ” на 2010-2012 гг.)
182
ОЗОНОЛИЗ ЦИКЛОМУСАЛЕНОНА И ЕГО ПРОИЗВОДНЫХ
Смирнова И.Е.,1 Биктимирова Л.Ф.,2 О.Б. Казакова,1* Куковинец О.С.2
1Федеральное бюджетное научное учреждение Институт органической химии Уфимского научного центра Российской академии наук, 450054, РФ, Уфа, пр. Октября, 71, e-mail: smirnova@anrb.ru
2 ФГБОУ ВПО «Башкирский государственный университет»
Источником циклоартанового нортритерпеноида цикломусаленона (сyclomusalenone) 1 является кожура банана растений видов Musa sapientum, Musa balbisiana и Musa errans.
Обнаружено, что цикломусаленон обладает гипогликемическим эффектом на моделях диабета у крыс (в дозе 2.62 мг/кг снижает уровень глюкозы на 45%). Для изучения зависимости структура
– свойство представляет интерес проведение трансформаций цикломусаленона, включая окислительные. В настоящей работе осуществлен ряд новых трансформаций цикломусаленона 1, который выделяли произрастающего во Вьетнаме растения
Musa balbisiana colla.
Низкотемпературный озонолиз цикломусаленона 1 затрагивал двойную связь в положении С25(27) с образованием (24S)-24-метил-29-нор-циклоарт-3,25-диона 2. Взаимодействием цикломусаленона 1 с солянокислым гидроксиламином синтезировали кетоксим 3, полученный согласно данным спектров ЯМР, в виде одного изомера.
В реакции совместного озонолиза по Грисбауму О- метилкетоксима цикломусаленона 4 в качестве карбонильной компоненты использовали метилтрифторметилкетон. В результате получили смесь четырех стереоизомерных 1,2,4- триоксоланов 5 и N-метоксилактама 6 с выходами 23 и 58%, соответственно.
Структура всех соединений подтверждена спектрами ЯМР, структура соединения 2 определена методом РСА.
183

|
|
|
a |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
1 |
b |
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
O |
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
3' O |
O 3 |
|
O 3 |
|
|
RON |
|
c |
1' |
O |
|
N |
|
|
|
CF3 |
|
|
H3CO |
|
|||
|
|
|
CH3 |
|
|
|||
|
3 R = H |
|
|
|
|
|
||
|
|
|
2' |
|
5 |
|
6 |
|
|
4 R = CH3 |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
Условия: a. O3, CH2Cl2, -40ºC; b. NH2OH·HCl, пиридин или
CH3ONH2·HCl, пиридин-метанол (1:1), кипячение, 6 ч; с. O3, CH2Cl2-циклогексан (1:1), F3CCOCH3, 0ºC.
Таким образом, впервые проведены окислительные превращения циклоартанового нортритерпеноида цикломусаленона с использованием озона. Синтезированы новые производные цикломусаленона с ацетатным, 1,2,4- триоксолановым и N-метоксилактамным фрагментами.
ИЗУЧЕНИЕ СОРБЦИОННЫХ ПРОЦЕССОВ В МАГНИТВОСПРИИМЧИВЫХ СИСТЕМАХ
Смирнова Л.Г., Аль Ансари С.В., Смирнов А.К.
ФГБОУ ВПО «Марийский государственный университет”, 424000, Россия, г. Йошкар-Ола, пл. Ленина, 1; aksmi@yandex.ru
Важнейшей особенностью современной химии является использование новых физико-химических и физических методов исследования. Одним из них является магнетохимический метод, основанный на определении магнитной восприимчивости веществ.
Целью настоящей работы явилось использование метода магнитной восприимчивости для количественной
184
характеристики процессов сорбции на катионообменниках марок КБ-4, KУ-1 и KУ-2-8. Для изучения процессов сорбции Fe(II) в статических условиях использовались растворы FeSO4 (0,1 - 0,5 моль/л). Навески сорбентов помещались в растворы и выдерживались до установления сорбционного равновесия в течение суток. После достижения равновесного состояния, концентрация ионов Fe(II) в исследуемых растворах определялась перманганатометрически. По полученным данным были рассчитаны величины удельной сорбции (NS). Параллельно с химическим методом определения концентрации ионов железа (II) в растворе проводились измерения величины магнитной восприимчивости растворов солей железа (II) и катионитов с сорбированными ионами магнетометром.
Полученные уравнения концентрационной зависимости силы магнитного взаимодействия (магниnной восприимчивости), как растворов, так и исследуемых сорбентов указываюn на возможность использования магнитометрического метода для количественной характеристики сорбционных процессов.
Работа выполнена при финансовой поддержке Федерального агентства по образованию (Темплан НИР ГОУВПО “МарГУ” на 2010-2012 гг.)
ФУНКЦИОНАЛИЗИРОВАННЫЕ 1,3-БЕНЗОДИОКСОЛЫ
Стукань Е.В., Макаренко С.В., Берестовицкая В.М.
ФГБОУ ВПО “Российский государственный педагогический университет им. А.И. Герцена”,
191186, Россия, Санкт-Петербург, наб.р.Мойки, д. 48. e-mail: kohrgpu@yandex.ru
Цикл 1,3-бензодиоксола является структурным фрагментом ряда природных (берберина бисульфат [1а], оксолиниевая кислота [1б]) и синтетических (сафразин и пароксетин [2])
лекарственных средств.
Нами осуществлен синтез ранее неизвестных 2-(нитрометил)- 2-(трихлорметил)-1,3-бензодиоксолов на основе реакции 1- бром-1-нитро-3,3,3-трихлорпропена (1) с пирокатехином и его замещенными (2-4); конденсация идет успешно при 18-20ºС в
185

этаноле в присутствии ацетата калия, выход продуктов (5-7) достигает 82%.
Cl3C |
|
|
Br |
|
|
|
Cl3C |
Br |
|
Cl3C |
|
|
R1 |
|
||||||
H 1 |
NO2 |
EtOH/AcOK, |
|
|
|
|
|
|||||||||||||
1 |
|
|
R1 |
|
|
|
|
O |
CCl3 |
|||||||||||
|
|
|
|
|
|
|
|
|
20oC, 24 ч |
O |
NO2 |
O |
NO2 |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
+ |
|
|
|
|
|
R |
-HBr |
|
|
NO2 |
|||||||||
|
|
|
|
|
|
|||||||||||||||
|
|
|
OH |
|
|
|
|
|
OH |
OH |
|
|
|
O |
||||||
R1 |
|
|
|
OH |
|
R2 |
|
|
|
R2 |
5-7 |
|||||||||
|
|
|
R2 |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
R2 |
|
|
|
|
|
|
|
|
|
|
||
2-4 |
R1 = R2 = H (2, 5); R1 = R2 = Br (3, 6); R1 = H, R2 = OH (4, 7). |
|
||||||||||||||||||
|
|
|||||||||||||||||||
Вероятно, этот однореакторный процесс протекает по пути образования продукта нуклеофильного присоединения, его последующего дегидробромирования и дальнейшей гетероциклизации за счет нуклеофильного присоединения свободной гидроксигруппы к нитроэтеновому фрагменту.
Строение полученных веществ (5-7) установлено методами ИК, ЯМР 1Н, 13С (HMQC, HMBC) спектроскопии с привлечением рентгеноструктурного анализа.
[1]Машковский М.Д. Лекарственные средства. Изд.12. Т.1. М.: Медицина. 1998. a) С. 513. б) С. 312.
[2]База данных Американского центра биотехнологий www.ncbi.nlm.nih.gov
ФОТО-КОНТРОЛИРУЕМЫЕ ДИНАМИЧЕСКИЕ СИСТЕМЫ НА ОСНОВЕ АМФИФИЛЬНОГО ТЕТРА(ВИОЛОГЕН)КАВИТАНДА
Султанова Э.Д., Кудряшова Ю.Р., Захарова Л.Я., Зиганшина А.Ю., Коновалов А.И.
Федеральное государственное бюджетное учреждение науки Институт органической и физической химии им. А.Е. Арбузова Казанского научного центра Российской академии наук;420088,
г. Казань, ул.Арбузова,8; elzaskagirl@mail.ru.
В последние годы большое внимание уделяется созданию супрамолекулярных ансамблей, способных контролируемо связывать молекул-гостей в связи с потенциальной
186
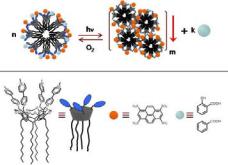
возможностью их применения в доставке лекарственных средств.
Нами создана новая динамическая супрамолекулярная система, в которой контроль связывания/высвобождение биологически-активных веществ осуществляется действием света. Динамическая система состоит из амфифильного тетра(виологен)кавитанда (1) и фотосенсибилизатора (4-PSA). В водной среде 1 и 4-PSA образуют супрамолекулярные ассоциаты мицелярного строения, способные связывать молекул-гостей виологеновыми фрагментами кавитанда. Действие света приводит к восстановлению виологеновых фрагментов, изменению организации супрамолекулярных ассоциатов и высвобождению молекул-гостей.
СИНТЕЗ ПРОИЗВОДНЫХ ИЗОХИНОЛИНА, ИМЕЮЩИХ В СВОЕЙ СТРУКТУРЕ КИСЛОРОДОСОДЕРЖАЩИЕ ГЕТЕРОЦИКЛЫ
Сурикова О.В., Михайловский А.Г., Вахрин М.И.
ГОУ ВПО Пермская государственная фармацевтическая академия, 614990, г. Пермь, Полевая, 2; neorghim@pfa.ru
Соединения, содержащие в своей структуре одновременно изохинолин и кислородосодержащие гетероциклы, до настоящего времени малоизвестны, хотя представляют собой новые потенциальные синтоны.
187

Так, известно, что широкие возможности в получении изохинолинового цикла имеет реакция Риттера [1]. При использовании в качестве нитрильной составляющей 2- цианофурана, нами были получены соединения, содержащие одновременно изохинолиновый и фурановый циклы.
|
|
|
|
|
|
Схема 1 |
|
R2 |
|
|
R1 |
|
R2 |
R1 |
|
|
|
R2 |
||
R2 |
+ |
CN |
|
|
||
|
R1 |
|
N |
|||
R1 |
OH |
|
O |
|
|
|
|
|
|
|
|
|
|
|
1a - e |
|
|
|
2a - e |
O |
|
|
|
|
|
|
1, 2а: R1 = H, R2 = CH3; 1, 2b: R1 = H, R2- R2 = (CH2)5; 1, 2c: R1 = CH3O,
R2 = CH3; 1, 2d: R1 = CH3O, R2 = C2H5; 1, 2e: R1 = CH3O, R2- R2 = (CH2)4;
Классическим методом построения системы пирроло[2,1- a]изохинолина является реакция Чичибабина, которая заключается во взаимодействии 1-метилизохинолина с β- галогенкетонами [2]. В качестве β-галогенкетонов здесь заслуживают внимания 3-бромацетил-кумарины, т.к. в этом случае предполагается образование системы, состоящей из двух самостоятельных гетероциклических фрагментов – пирроло[2,1- a]изохинолина и кумарина.
Схема 2
Me |
|
O |
Me |
|
|
Me |
|
|
Br |
Me |
|
+ |
|
N |
|
||
N |
|
|
|
|
|
Me |
|
O O |
|
|
O |
|
|
|
|
||
|
|
|
|
|
|
3 |
|
|
4 |
|
O |
|
|
|
|
||
Продолжая |
исследования |
в области реакций |
2,3- |
||
диоксопирроло[2,1-a]изохинолинов с бинуклеофилами, мы обнаружили, что данные соединения при кипячении с о- аминофенолом в среде 2-пропанола раскрывают диоксопирролиновый цикл с образованием енаминокетонов, содержащих остаток бензоксазола. Реакции с о-аминофенолами протекают в отсутствие кислот. Возможно, что здесь каталитическое действие проявляет достаточно кислый
188

фенольный гидроксил. Следует также учитывать образование ароматической системы бензоксазола, что энергетически выгодно. Предложенный метод открывает новые возможности в области их синтеза и практического применения.
|
|
|
O H |
|
Схема 3 |
|
|
|
|
|
|
|
|
|
N H 2 |
|
N |
|
|
|
|
|
H |
R |
1 |
R 2 |
3 |
|
O |
|
R 2 |
R |
|
|
|
|
|
R 4 |
O |
N |
|
R |
1 |
N |
O |
||
|
|
|
|
|
|
|
|
R 3 |
O |
|
|
|
|
5 a - d |
6 a - d |
|
R 4 |
|
|
|
|
||
5, 6а: R1 = H, R2 = CH3, R3 = H, R4 = H; 5, 6b: R1 = CH3O , R2 = CH3, R3 = |
|||||
H, R4 = H; 5, 6c: R1 = H, R2 = CH3, R3 = H, R4 = CH3; 5, 6d: R1 = H, R2- R2 |
|||||
= (CH2)4, R4 = CH3; |
|
|
|
||
[1]Krimen, L.I. The Ritter reaction / L.I. Krimen, D.J. Kota // Organic reaction. – New York: J. Wiley, 1969. – Vol.17. – P.213 – 325.
[2]Вацуро, К.В., Именные реакции в органической химии / К.В. Вацуро, Г.Л. Мищенко – М.: Химия, 1976. – 528с.
СЕЛЕКТИВНОЕ ВОССТАНОВЛЕНИЕ НИТРОГРУППЫ 3,5-ДИНИТРО-2-ОКСИПИРИДИНА
Сурова И.И., Атрощенко Ю.М.
ФГБОУ ВПО «Тульский государственный педагогический университет им. Л.Н.Толстого», 300026 ,Россия, г. Тула, пр.
Ленина, 125; irine.surova@gmail.com
Аминонитропиридины, используемые в качестве прекурсоров лекарственных средств и гербицидов, обычно получают нитрованием аминопиридинов [1] или аммонолизом галогеннитропиридинов [2]. Менее изученным остается вопрос о селективном восстановлении одной из нитрогрупп в динитропиридинах.
189

Нами было осуществлено восстановление одной из нитрогрупп в 3,5-динитро-2-оксипиридине сульфидом натрия. Реакцию проводили при 100°С в 25%-ном водном растворе хлорида аммония. По данным ТСХ процесс завершался в течение 30 мин.
Осадок гидрохлорида 3-амино-5-нитро-2-оксипиридина отделяли, растворяли в воде, нейтрализовали гидроксидом натрия и экстрагировали этилацетатом. После отгонки растворителя вещество перекристаллизовывали из пропанола-2. Выход продукта составил 68%. Строение 3-амино-5-нитро-2- оксипиридина было доказано данными ИК- и ЯМРспектроскопии.
Полученное соединение может быть использовано для синтеза пиридоаннелированных оксазолов, оксазинов, оксазепинов и др. Кроме того, оставшаяся нитрогруппа после легко подвергается дальнейшей модификации восстановления в аминогруппу.
[1] Mizzoni R. H., Abramovitch R. A. // Chemistry of Heterocyclic Compounds: Pyridine and Its Derivatives: Supplement, P. III, 2008, Vol. 14, Chapter VIII. , P. 45.
[2] De Bie D.A., Geurtsen B., Van der Plas H. C. // J. Org. Chem., 1985, Vol. 50 (4), P. 484–487.
ЦИАН- И ЭПОКСИСОДЕРЖАЩИЕ НЕПРЕДЕЛЬНЫЕ КРЕМНИЙОРГАНИЧЕСКИЕ МОНОМЕРЫ
Тарвердев Ш.А., Байрамов Г.К., Мамедова Р.И., Насирова И.М., Ширинов П.М.
Сумгайытский государственный университет, AZ5000, Азербайджан,г.Сумгайыт, 43-й кварт., penahsirinov@mail.ru
Исследована реакция присоединения дигидридов кремния типа R2SiH2 (где R–органические радикалы) к циан – и эпоксисодержащим соединением пропаргильного ряда в присутствии платинохлористоводородной кислоты [1]. Установлено, что указанная реакция приводит к образованию
190
