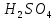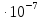- •Электрический баланс ванны электроэкстракции Никеля
- •Введение
- •Электродные реакции
- •1.2 Суммарная электрохимическая реакция
- •2.Составы электролитов для электроэкстракции никеля
- •2.1 Сульфатный электролит
- •3.Расчет электрического баланса ванны электроэкстракции
- •3.1Исходные данные для расчета электрического баланса. Расчет электрического баланса
- •3.1.1 Расчет равновесных электродных потенциалов анодной и катодной реакций
- •3.1.2 Расчет перенапряжений катодной и анодной реакции
- •3.1.3 Расчет падения напряжения в электролите
- •3.1.4 Расчет падения напряжения в диафрагме
- •3.1.5 Расчет падения напряжения в теле электрода
- •3.1.6 Расчет напряжения на ванне с учетом падения напряжения в контактах
1.2 Суммарная электрохимическая реакция
С
учетом вышеизложенного в электролизере
протекает суммарная электрохимическая
реакция: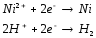
К: Вт
(1-
Вт)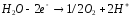
А:
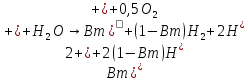
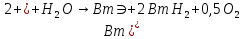
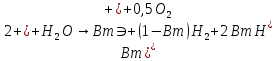
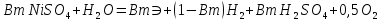
2.Составы электролитов для электроэкстракции никеля
2.1 Сульфатный электролит
Самое широкое распространение на сегодняшний день имеют сульфатные электролиты. Они обладают рядом существенных преимуществ перед хлоридными и аммонийными. Это простота, хорошая электропроводность и отсутствие выделения ядовитых газов на электродах и необходимости их отвода. Выход по току в таких электролитах колеблется в пределах от 70 до 96 % .
В состав сульфатных электролитов обязательно входит сульфат никеля и серная кислота. В качестве добавок в некоторых электролитах используют борную кислоту и сульфат натрия. Увеличение концентрации ионов никеля увеличивает выход по току и снижает удельный расход электроэнергии. Так, например, при увеличении концентрации ионов никеля с 60 до 130 г/л выход по току увеличивается на 12 %, а удельный расход электроэнергии снижается на 17%. Но слишком высокая концентрация сульфата никеля может привести к его кристаллизации.
Серная кислота оказывает благотворное влияние на электропроводность и исключает гидратообразование на катоде, однако её избыток снижает выход по току никеля и усиливает выделение водорода.
Серная кислота используется для доведения уровня pH.
Существует 3 типа сульфатных электролитов для электроэкстракции никеля:
• электролиты, содержащие сульфат никеля и серную кислоту;
• электролиты, содержащие сульфат никеля, сульфат натрия и серную кислоту;
• электролиты, содержащие сульфат никеля, сульфат натрия, серную и борную кислоты.
3.Расчет электрического баланса ванны электроэкстракции
Составление электрического баланса ванны электроэкстракции позволяет определить максимальное напряжение. Результаты электрического баланса позволяют выбрать выпрямительный агрегат для обслуживания ванны.
3.1Исходные данные для расчета электрического баланса. Расчет электрического баланса
Исходные данные для расчета электрического баланса ванны представлены в таблицах 2- 6:
Таблица 2 – Состав электролита на входе в ванну
|
Ионы
цинка
|
130 |
|
Серная
кислота
|
2,66 |
|
pH |
2,5 |
|
|
-0,25 |
|
α |
0,5 |
|
|
2∙ |
|
|
|
Таблица 3 – Состав электролита на выходе из ванны, г/л
|
Ионы
цинка
|
100 |
|
Серная
кислота
|
50 |
Таблица 4 - Параметры технологического процесса
|
Температура электролита, °С |
65 |
|
Плотность
тока (катодная),
|
300 |
|
Катодный выход по току, % |
96 |
|
Анодный выход по току, % |
100 |
|
Длина ванны, мм |
6010 |
|
Ширина ванны, мм |
1160 |
|
Высота ванны, мм |
1390 |
Таблица 5 – Параметры катодов
|
Высота катода, мм |
1020 |
|
Ширина катода, мм |
1020 |
|
Толщина катода, мм |
30 |
|
Количество катодов, шт |
52 |
|
Расстояние между электродами, мм |
110 |
|
ρFe,
|
1,52 |
Таблица 6 – Параметры анодов
|
Высота анода, мм |
1000 |
|
Ширина катода, мм |
1000 |
|
Толщина анода, мм |
10 |
|
Количество анодов, шт |
53 |
|
ρPb,
|
2,45 |
Электролизная ванна представляет собой железобетонную конструкцию с внутренней футеровкой из ПВХ (рисунок 1). Внутренние размеры ванны: 6010*1160*1390 мм [2].
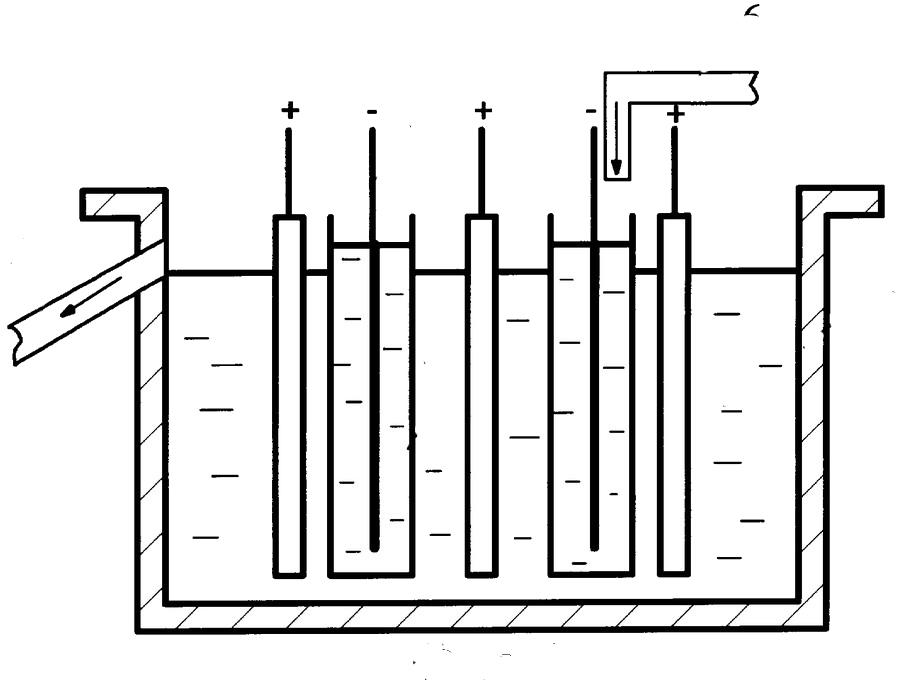
Рисунок 1 - Эскиз ванны электролиза [4]
Зная габаритные размеры ванны, можно высчитать объем ванны по формуле:
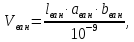 (3.1)
(3.1)
где
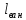 – длина ванны, мм
– длина ванны, мм
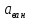 -
ширина ванны, мм
-
ширина ванны, мм
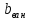 –высота
ванны, мм
–высота
ванны, мм

Для расчета напряжения на ванне используем формулу (3.2):
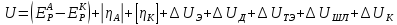 ,
(3.2)
,
(3.2)
где
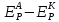 – разность равновесных электродных
потенциалов анодной и катодной
реакций, В[3]
– разность равновесных электродных
потенциалов анодной и катодной
реакций, В[3]
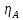 ,
,
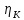 – перенапряжение для анодной и катодной
реакций, В
– перенапряжение для анодной и катодной
реакций, В
 –падение
напряжения в электролите, В
–падение
напряжения в электролите, В
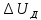 –падение
напряжения в диафрагме, В
–падение
напряжения в диафрагме, В
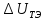 –падение
напряжения в теле электродов, В
–падение
напряжения в теле электродов, В
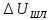 –падение
напряжения в шламе, В
–падение
напряжения в шламе, В
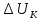 –падение
напряжения в контактах, а также в
токоподводящих шинах до источника
питания постоянным током, В
–падение
напряжения в контактах, а также в
токоподводящих шинах до источника
питания постоянным током, В

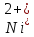 ,
г/л
,
г/л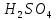 ,
г/л
,
г/л ,
В
,
В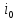 ,
,
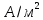
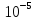
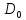 ,
,