
фотохимия
.pdf
S1
T1
S0
Фосфоресценция
Донор
Интеркомбинационная
конверсия
Поглощение |
|
|
|
|
|
|
ц |
и |
я |
конверсия |
|||
|
|
|
|
|
|
|
|
е |
н |
|
|
Внутренняя |
|
|
|
|
|
|
|
|
ц |
|
|
|
|||
|
|
|
|
|
|
с |
|
|
|
|
|||
|
|
|
|
|
е |
|
|
|
|
|
|
||
|
|
|
|
р |
|
|
|
|
|
|
|
||
|
|
|
о |
|
|
|
|
|
|
|
|
||
|
л |
у |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|||
Ф |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Акцептор
S1
S0
Рис. 4.6. Схема электронных переходов в комплексе с переносом заряда.
Образовавшийся при возбуждении комплекс растрачивает свою энергию в нескольких процессах. Возможны: обратный излучательный переход с переносом заряда из S1 акцептора в S1 донора (флуоресценция КПЗ), внутренняя конверсия в КПЗ, а также фотохимическое необратимое изменение молекул, входивших в КПЗ. Если триплетный уровень донора имеет меньшую энергию, чем возбужденный синглетный уровень акцептора, то может произойти интеркомбинационная конверсия с последующим излучением фосфоресценции донора (рис. 4.6). Считают, что КПЗ легко образуются между кислородом и различными полимерами (такому КПЗ приписывают полосу поглощения полиэтилена, простирающуюся вплоть до 400 нм), а также кислородом и многими ароматическими соединениями, например бензолом. Электронный переход с переносом заряда с определенной вероятностью заканчивается окислением органических молекул. Типичными акцепторами электрона в КПЗ являются хиноны, полинитроароматические соединения и т.д.; типичные доноры – ароматические углеводороды, диеновые структуры и т.д. Предполагается, что фотохимические реакции некоторых сенсибилизаторов протекают с участием КПЗ. Например, показано, что триплетные возбужденные состояния 8-метоксипсоралена (8-МОП) реагируют с 3,4- диоксифенилаланином (ДОФА) по механизму переноса заряда. В результате образуются свободные радикалы 8-МОП и ДОФА. В отсутствие кислорода этот процесс обратим, в присутствии О2 он завершается окислением ДОФА. Предполагают, что генерация синглетного кислорода триплетными состояниями фотосенсибилизаторов происходит через стадию образования комплекса с переносом заряда. Эти комплексы участвуют в передаче энергии от молекулы сенсибилизаторов на молекулу кислорода.
11
Донорно-акцепторные комплексы с переносом заряда между возбужденной и невозбужденной молекулами разных веществ называют эксиплексами. Образование эксиплексов может проявляться в том, что в спектрах флуоресценции ароматических соединений в присутствии доноров или акцепторов электрона появляется новая полоса, смещенная в длинноволновую сторону.
4.5 Методы изучения первичных фотопродуктов
Первичные продукты фотохимических реакций (молекулы в электронновозбужденных состояниях и свободные радикалы), как правило, химически неустойчивы и быстро переходят либо в исходные вещества, либо в более устойчивые фотопродукты (новые молекулы). Поэтому концентрация первичных фотопродуктов в обычных условиях облучения в жидких растворах бывает настолько низкой, что их не удается исследовать обычными физико-химическими методами.
Рассмотрим эту ситуацию количественно. Упрощенно фотохимическая реакция может быть представлена схемой
A →освещение (k1 ) A' →k B ←k 3
2
где A` – первичный лабильный фотопродукт; В – стабильный фотопродукт; k1, k2 и k3 – константы скоростей мономолекулярных реакций, идущих при освещении (k1) или независимо от освещения (k2 и k3). Для таких систем накопление продукта A' во времени описывают кинетическим дифференциальным уравнением
d [A'] |
= k1 [A]−(k2 +k3 ) [A'] |
(4.8) |
|
dt |
|||
|
|
В стационарных условиях облучения концентрация А’ постоянна, т.е. d[A']/ dt = 0 откуда
[A'] |
= |
|
k1 |
(4.9) |
|
[A] |
|
k2 |
+ k3 |
||
В разбавленных растворах скорость световой реакции образования A’ может быть выведена из предыдущих уравнений:
d [A'] |
= k1 |
[A]= J0Qs [A]= J0σ [A] |
(4.10) |
|||||
|
|
|
|
|
||||
|
|
|
||||||
dt |
обр |
|
|
|||||
откуда |
|
|
|
|
|
|
|
|
[A'] |
= |
|
|
J0σ |
|
|
||
[A] |
|
. |
|
(4.11) |
||||
k2 +k3 |
|
|||||||
|
|
|
|
|
|
|
12 |
|
Из (4.11) очевидно, что увеличить относительную концентрацию неустойчивого фотопродукта A' можно либо увеличением интенсивности действующего света J0, либо замедлением скорости темновых процессов (т.е. уменьшением k2 и kз).
4.5.1 Импульсный фотолиз
Первый способ реализуется в методе импульсного фотолиза, разработанном Р.Г.В. Норишем и Г.Б. Портером в 1949г. Метод основан на освещении образца очень яркой вспышкой света, при которой в возбужденное состояние переходит одновременно значительная доля молекул исследуемого вещества. Как следствие этого сразу после вспышки лабильные фотопродукты образуются в достаточно высоких концентрациях, что позволяющих проводить их спектральное определение. Уже через несколько микроили миллисекунд эти фото продукты вновь исчезают. Обнаружение и идентификация лабильных продуктов основана на измерении спектров их поглощения (переходных спектров) и определении времени жизни продуктов по кинетике исчезновения («выцветания») их переходных спектров поглощения.
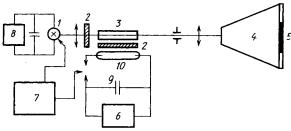
Рис. 4.7. Спектрографическая установка импульсного фотолиза: 1 — спектроскопическая лампа; 2 — светофильтры; 3 — кювета; 4 — спектрограф; 5 — фотопластинка; 6 — зарядное устройство; 7 — блок временной задержки; 8 — питание импульсной спектроскопической лампы; 9
— конденсатор; 10 — импульсная лампа.
В настоящее время используют в основном два типа установок импульсного фотолиза – кинетическую и спектрографическую (рис. 4.7). Кинетическая установка позволяет получить непосредственно кинетическую кривую гибели промежуточного продукта при одной длине волны регистрации. При помощи спектрографической установки регистрируется весь спектр промежуточных продуктов через определенный промежуток времени после фотолитической вспышки. Разрешающее время обычных установок импульсного фотолиза, в которых применяют импульсные лампы, 10–6–10–5 c. С развитием лазерной техники путем использования импульсных лазеров удалось уменьшить это время до пикосекунд и даже фемтосекунд (10–15 с) .
Метод импульсного фотолиза позволяет непосредственно следить за кинетикой гибели не только радикалов или других химических продуктов реакции, но и
13
триплетных молекул в растворе при обычных температурах. Так как триплет– триплетные переходы не запрещены (нет ограничений по спину), то поглощение при этих переходах характеризуется такими же высокими значениями молярных коэффициентов поглощения, как и при синглет–синглетных переходах.
4.5.2 Импульсный радиолиз
При импульсном радиолизе образец облучают пучком электронов или других ионизирующих частиц. Регистрирующие системы идентичны применяемым при импульсном фотолизе. Под действием самих падающих частиц или в результате реакций радикалов растворителя, например воды, образующихся при радиолизе, молекулы растворенного соединения могут превращаться в те же продукты, что и при фотохимических реакциях, например в катионили анионрадикалы, а также возбужденные молекулы вещества в синглетном или триплетном сотсоянии. Любопытно, что в некоторых случаях триплетные состояния образуются, минуя синглетное возбужденное состояние. Поэтому радиолиз удобен для изучения триплетных состояний веществ, имеющих низкую или равную нулю константу скорости интеркомбинационной конверсии, например, каротиноиды.
4.5.3 Изучение фотохимических реакций при глубоком охлаждении
Альтернативным импульсному радиолизу при изучении нестойких промежуточных продуктов фотохимических реакций можно считать метод стабилизации этих продуктов за счет понижения температуры, (замораживания образцов жидким азотом). Глубокое охлаждение не влияет заметно на первичный фотохимический акт (как правило, это образование свободных радикалов), но приводит к резкому торможению темновых превращений первичных фотопродуктов; последнее означает, что константы сколростей k2 и k3 в уравнении (4.11) резко уменьшаются. Поэтому в охлажденных и замороженных образцах первичные продукты удается накопить в количествах, достаточных для исследования спектрофотометрическими или радиоспектроскопическими методами. Так, при 77 K спектры триплеттриплетного поглощения в УФ-облученных ароматических аминокислотах удается измерять непосредственно в процессе облучения обычными (не импульсными) источниками возбуждающего света. Свободные радикалы, находящиеся в замороженном растворителе при таких низких температурах, могут долго храниться после выключения возбуждающего света, что позволяет изучать их методами спектрального анализа или ЭПР.
При использовании техники глубокого охлаждения необходимо помнить, что при низких температурах могут измениться и сами фотохимические реакции, протекающие в системе. Одна из интересных особенностей низкотемпературной фотохимии заключается в том, что время жизни молекул в триплетных возбужденных состояниях T1 в твердой замороженной среде может повыситься настолько, что они успевают за время своей жизни поглотить второй квант света и перейти в более высокое триплетное состояние T2. Из высоких триплетных
14
состояний легко осуществляется фотоионизация ароматических аминокислот, фурокумаринов и др. В жидких растворах при использовании обычных источников света такие двухфотонные процессы невозможны из-за малого времени жизни триплетных состояний (и, как следствие, их низкой концентрации).
4.5.4 Использование метода электронного парамагнитного резонанса (ЭПР)
Несмотря на сравнительно высокую чувствительность метода ЭПР (в водных растворах при положительных температурах удается обнаруживать 10–8 моль л–1 свободных радикалов), обнаружить радикалы при протекании фотохимических реакций в водных растворах при обычных температурах обычно не удается из-за исклюбчительно высокой реакционной способности радикалов и, следовательно, их низкой концентрации в каждый данный момент времени.. Поэтому спектры ЭПР продуктов фотохимических реакций реально удается измерить, как правило, лишь при облучении объектов, замороженных жидким азотом.
В последнее время были все же разработаны методы обнаружения свободных радикалов в жидких растворах основанные на использовании методов импульсного фотолиза или радиолиза и специальных малоинерционных ЭПР-спектрометров. В таких исследованиях спектры ЭПР строят на основании серии кинетических измерений сигналов ЭПР при различных фиксированных значениях напряженности магнитного поля H. В этих работах по импульсному ЭПР удалось измерять сигналы свободных радикалов, существующих всего в течение 1 мкс после вспышки света или импульса ионизирующего излучения.
Широкое распространение для обнаружения свободных радикалов при обычных (физиологических) температурах получил метод спиновых ловушек,
рассмотренный в разделе Error! Reference source not found..
4.5.5 Ингибиторный анализ
Во многих случаях идентифицировать фотопродукты, обладающие определенными переходными спектрами при импульсном фотолизе или радиолизе, помогает использование ловушек (перехватчиков) радикалов или тушителей триплетных состояний. Эти вещества, естественно, уменьшают или полностью подавляют фотохимическое действие света и носят общее название ингибиторов фотохимической реакции или фотобиологического процесса в целом. Так, например, молекулярный кислород тушит триплетные возбужденные состояния органических молекул. Таким же свойством обладают парамагнитные ионы (Mn2+, Ni2+, Со2+, Fe2+ и др.), тогда как непарамагнитные (Ca2+, Zn2+ и др.) тушат триплетные состояния гораздо хуже. Эффективным тушителем триплетов является β-каротин. Действие этих соединений на переходные спектры и накопление фотопродуктов указывает на появление в системе триплетных молекул и их участие в фотохимической реакции.
15
Были предложены разного рода ловушки первичных свободно-радикальных продуктов. Так, цистеин, цистин, KNO3, N2O имеют высокое сродство к электрону и поэтому эффективно ингибируют реакции с участием сольватированных электронов, захватывая последние. Трет-бутанол и другие спирты перехватывают ОН-радикалы. Угнетающее действие ловушек на накопление конечных продуктов фотохимической реакции может служить указанием на то, что данные радикалы действительно участвуют в процессе.
Ингибиторный анализ бывает полезен при изучении механизма патологических процессов в таких сложных системах, как кожа и другие органы и ткани, в которых прямое обнаружение первичных фотопродуктов физико-химическими методами крайне затруднено. Например, антиоксиданты ионол, витамин Е и другие имеют низкий потенциал ионизации, легко отдают электрон свободным радикалам, тем самым ингибируя свободнорадикальные реакции.
4.6 Молекулярно-клеточные механизмы действия низкоинтенсивного лазерного излучения
Около 40 лет тому назад вскоре после изобретения лазеров возникла и стала развиваться новая медицинская технология лечения широкого круга различных воспалительных и онкологических заболеваний, основанная на использовании низкоинтенсивного лазерного излучения (НИЛИ) (рис. 4.8); одним из направлений применения НИЛИ стала фотодинамическая терапия опухолей, второе, при котором внешние сенсибилизаторы не использовались, получило более широкое название – лазеротерапия.
Хирургический «скальпель»
Высокоинтенсивное лазерное излучение
Низкоинтенсивное лазерное излучение
• Рост активности фагоцитов
• Усиление пролиферации
клеток Лазеротерапия • Вазодилатация и
улучшение циркуляции крови
В сочетании с фотосенсибилизаторами
фотодинамическая терапия опухолей
Рис. 4.8. Использование лазерного излучения в медицине.
16
В основе метода фотодинамической терапии лежит применение экзогенных (внешних) фотосенсибилизаторов, которые после введения в организм больного преимущественно локализуются в опухолевых клетках. Последующее лазерное облучение опухоли с адсорбированными фотосенсибилизаторами в полосе поглощения красителя сопровождается массированной продукцией свободных радикалов и синглетного кислорода 1О2, которые в свою очередь инициируют вторичные свободнорадикальные реакции с участием липидов, белков и нуклеиновых кислот, что и является основной причиной поражения раковых клеток при фотодинамической терапии опухолей.
Лазеротерапия, основанная на стимулирующем действии лазерного облучения в отсутствие внешних сенсибилизаторов также получила широкое распространение. До последнего времени механизмы стимулирующего действия НИЛИ были не раскрыты, хотя было предложено немало гипотез, как правило, довольно умозрительных. Главный вопрос, который долгое время оставался неясным, — это природа хромофора, поглощающего действующее излучение и механизм первичных реакций, приводящих к формированию физиологического ответа организма.
Перед обсуждением возможных механизмов и эффектов перечислим некоторые достоверно установленные факты, касающиеся действия лазерного излучения на биологические объекты.
1.Излучение с длиной волны 400–600 нм и около 600 нм вызывает ускорение деления клеток ряда микроорганизмов, а также увеличение белкового синтеза; при этом наблюдается колокол-образная зависимость стимулирующего действия от дозы.
2.при облучении изолированных митохондрий печени светом He–Ne лазера в них увеличивается содержание АТФ, возрастает величина электрического потенциала на внутренних мембранах и pH в матриксе, а также наблюдаются небольшие изменения формы матрикса.
3.Облучение фибробластов человека светом He–Ne лазера существенно увеличивает скорость роста популяции клеток в экспоненциальной фазе и адгезию клеток на подложке (в случае эмбриональных фибробластов).
4.Лазерное облучение клеток, выделенных из эпителия сетчатки, приводит к увеличению митотического индекса.
5.Облучение светом He–Ne лазера обычно не вызывает бласттрансформацию изолированных лимфоцитов, но заметно увеличивает бласттрансформацию, вызванную фитогемагглютинином, а также приводит к увеличению митотического индекса на третий и четвертый день после облучения низкими дозами лазерного излучения.
17
6.Под действием облучения He–Ne лазера увеличивается содержание внутриклеточного кальция в лейкоцитах, интенсивность окрашивания нуклеиновых кислот в клетках флуоресцирующим красителем акридиновым оранжевым и изменяется морфологическая структура хроматина. По всем параметрам действие лазерного излучения в оптимальной дозе было сходным с действием фитогемагглютинина.
7.При облучении крови непосредственно в кровеносных сосудах наблюдается расширение сосуда выше и ниже места облучения (вазодилатация); этот эффект исчезает при замене крови физиологическим раствором. Вазодилатация приводит к улучшению кровоснабжения органов.
Все эти факты свидетельствуют о том, что наблюдаемые в клинике эффекты (противовоспалительное действие лазерного облучения, ускорение регенерации поврежденных тканей и улучшение кровоснабжения органов) могут быть связаны с тремя эффектами лазерного облучения, полученными в эксперименте:
рост активности фагоцитов; усиление пролиферации клеток;
улучшение циркуляции крови по сосудистому руслу вследствие вазодилатации.
Все эти данные позволили сформулировать гипотезы о молекулярных механизмах действия лазерного излучения.
4.7Три гипотезы о механизмах действия НИЛИ
В1994 году на основании анализа имевшихся в то время данных литературы и собственных опытов Ю.А. Владимиров сформулировал три гипотезы о механизме действия низкоинтенсивного лазерного излучения на клетки и организм человека. Биологическое действие лазерного излучения в видимой области света и его клиническое применение основано на трех эффектах:
—фотодинамическое действие на мембраны, сопровождаемое увеличением внутриклеточного кальция и стимуляцией клеток;
—фотореактивация Cu-Mn-супероксиддисмутазы;
—фотолиз металлокомплексов NO с высвобождением этого вазодилататора.
Эти три эффекта лежат в основе непрямого бактерицидного, регенеративного и вазодилатационного действия лазерного облучения. В последнее время было получено много данных, подтверждающих существование этих трех механизмов действия низкоинтенсивного лазерного излучения. Рассмотрим эти данные.
18
4.7.1 Механизм 1: фотодинамическое действие лазерного излучения на биологические объекты.
Гипотеза о фотодинамическом механизме действия лазерного излучения основывалась на четырех известных к тому времени фактах:
1.При действии НИЛИ на клетки животных организмов, такие как лимфоциты, наблюдается увеличение концентрации ионов кальция в цитоплазме.
2.При облучении изолированных мембранных структур в присутствии гематопорфирина происходит липидная пероксидация.
3.Липидная пероксидация приводит к подавлению активного транспорта ионов кальция в мембранах эндоплазматического ретикулума и митохондрий, а также к увеличению проницаемости мембран для этих ионов.
4.При действии на лейкоциты крови продуктов липидной пероксидации наблюдается прайминг (предстимуляция) этих клеток, что проявляется в более мощном респираторном взрыве в ответ на действие стимула, например, активированного зимозана.
Согласно этой гипотезе, последовательность событий при действии лазерного излучения на клетки может быть представлена в следующем виде:
1)Поглощение фотонов фотосенсибилизаторами. Известно, что чистые фосфолипиды, составляющие основу всех клеточных и внутриклеточных мембран, не поглощают свет в видимой и ИК области спектра. Добиться поглощения лазерного излучения можно при наличии фотосенсибилизаторов (веществ, обладающих интенсивным поглощением в требуемой области спектра), в частности, гематопорфирин и фталоцианин.
2)Перекисное окисление липидов в мембранах клеток и митохондрий. Поглощение лазерного излучения сопровождается окислением липидов и образованием перекисей. Фотопероксидация липидов наблюдается при лазерном облучении суспензии клеток и митохондрий иногда даже без фотосенсибилизатора. Повидимому, в определенных условиях в организме накапливаются природные фотосенсибилизаторы (возможно, те же порфирины, содержащиеся в крови человека и животных при неблагоприятных условиях).
3)Увеличение концентрации ионов кальция в клетках. Последствия перекисного
окисления фосфолипидного слоя сводятся к нескольким эффектам: избирательно увеличивается проницаемость для ионов H+ и/или OH–; увеличивается проницаемость для ионов Ca2+; снижается электрическая стабильность бислоя и может наступить самопроизвольный «пробой» мембран собственным электрическим потенциалом. В клеточных мембранах помимо этого происходит
окисление SH групп и повреждение кальциевого насоса. В результате происходит повышение концентрации внутриклеточного Ca2+.
19
4) Активация внутриклеточных процессов:
Биологические последствия увеличения концентрации ионов кальция в цитоплазме клетки различаются в зависимости от облучаемых клеток. При облучении крови существенно действие излучения на лейкоциты, а именно, вызванная облучением предстимуляция фагоцитов, т.е., двух–трехкратное увеличение продукции активных форм кислорода в ответ на действие стимула.
—стимуляция клеточного деления;
—другие эффекты.
Представление об определяющей роли увеличения концентрации Ca2+ в цитоплазме при действии НИЛИ позволило объяснить хорошо известный факт о стимулирующем действии малых доз лазерного облучения и подавляющем действии высоких доз, равно как и зависимость эффективности лазерного облучения от физиологического состояния клеток.
4.7.2 Механизм 2: фотореактивация супероксиддисмутазы
Явление фотореактивации клеточной супероксиддисмутазы (Cu-Mn-СОД) было обнаружено в результате анализа данных, полученных при изучении действия гелий-неонового лазера на заживление ран. Это действие лазерного излучения уже довольно давно используется в некоторых клиниках для лечения долго незаживающих ран и трофических язв. Было сделано предположение, что действие лазерного облучения уменьшает образование свободных радикалов в ране. Подтверждением такого предположения могли служить опыты, в которых изучалась интенсивность хемилюминесценции раневых экссудатов в присутствии добавленной к ним перекиси водорода. Свечение было связано с образованием супероксидного радикала из перекиси водорода при ее разложении экссудатом: добавление к экссудату фермента супероксиддисмутазы (СОД), удаляющего супероксидные радикалы, равно как и добавление каталазы, удаляющей перекись водорода, подавляло вспышку хемилюминесценции. Облучение экссудата светом гелийнеонового лазера также подавляло свечение; таким образом, свет лазера действовал как каталаза или супероксиддисмутаза. Поскольку за несколько секунд облучения вряд ли могло произойти образование новой каталазы или супероксиддисмутазы в экссудате, то было естественно предположить, что исходно в силу каких-то условий активность каталазы или супероксиддисмутазы была в экссудате понижена, а лазерное облучение реактивировало один из этих ферментов. Заметим, что оба фермента обладают поглощением при длине волны света HeNe-лазера - 633 нм. Однако в случае каталазы никакого действия лазерного облучения на фермент получить не удалось.
20
