
фотохимия
.pdf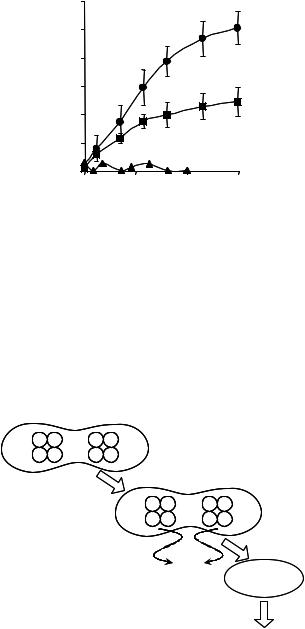
Кинетика образования NO при облучении NO гемоглобина в растворах, гемолизатах эритроцитов и в самих эритроцитах представлена на рис. 4.19.
Концентрация ИНР, ммоль/л
0.12
0.1
0.08
0.06
0.04
0.02
0 |
0 |
50 |
100 |
150 |
Доза облучения, кДж/м |
2 |
||
Рис. 4.19. Кинетика образования NО при облучении нитрозильных комплексов HbNO в растворе (треугольники), в эритроцитах (кружки) и гемолизате (квадраты) в присутствии спиновой ловушки ИНР. Концентрация HbNO ≈
0,45 ммоль/л, интенсивность излучения
190 Вт/м2.
Во всех случаях фотолиз NOгемоглобина сопровождался высвобождением свободного оксида азота. Полученные данные говорят о том, что нитрозильные комплексы гемоглобина могут служить донором NO, а низко-интенсивное лазерное излучение, индуцируя распад HbNO, высвобождает NO, которое в условиях организма, возможно, будет способствовать улучшению микроциркуляции крови. Данный механизм может функционировать как в нормальных физиологических условиях (уровень HbNO в крови достигает 1 нмоль/л), так и в условиях патологии, в особенности при ишемии, когда оксигенация ткани снижается, а образование NO возрастает и создаются условия для деоксигенации и нитрозилирования гемоглобина (рис. 4.20).
α β –ON α β –ON NO– β α NO– β α
hν |
α |
β |
α |
β |
|
||||
|
β |
α |
β |
α |
|
|
|
NO |
Гуанилат |
|
|
|
|
|
|
|
|
|
циклаза |
Рис. 4.20. Схема механизма расслабления кровеносных сосудов в результате фотолиза нитрозильных комплексов гемоглобина в эритроцитах под действием лазерного излучения с последующим выделением свободного оксида азота и активацией растворимой гуанилатциклазы.
Расслабление сосудов
Фотохимические реакции нитрозильных комплексов цитохрома с.
31
Цитохром с реагирует с NO как в ферро- (cyt c (Fe2+)) так и в ферри- (cyt c (Fe3+)) состояниях, однако нитрозильные комплексы восстановленной формы (cyt c (Fe2+)– NO) более стабильны и обладают парамагнитными свойствами. Спектр ЭПР cyt c (Fe2+–NO) имеет форму одиночной асимметричной линии с g-фактором 2,00 и полушириной около 100 Гс (рис. 4.21А).
50 Гс |
g = 2,00 |
|
1 |
|
0 Вт/м2 |
|
|
|
|
|
|
|
|
||
|
ед.отнNO,. |
|
|
|
|
|
|
|
сигналаЭПР |
0,8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,6 |
|
80 Вт/м2 |
|
|
8 кДж/м2 |
Амплитуда |
cytc |
|
|
|
|
|
0,2 |
|
|
|
|
|||
|
|
- |
|
|
|
|
|
|
|
2+ |
0,4 |
|
|
|
|
облучение |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
200 Вт/м2 |
|
|
без |
|
|
0 |
|
|
|
|
облучения |
|
|
0 |
1 |
2 |
3 |
4 |
|
|
|
|
Время, мин |
|
||
|
А |
|
|
|
Б |
|
|
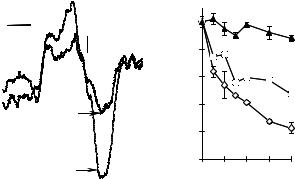
Рис. 4.21. Фотолиз комплексов оксида азота с феррицитохромом c. А — влияние лазерного излучения на ЭПР спектр cyt с(Fe2+-NO), концентрация сyt c 0,3 ммоль/л, интенсивность излучения 230 Вт/м2, доза 8 кДж/м2; Б — кинетика изменений амплитуды спектра ЭПР cyt с(Fe2+–NO) при облучении He– Cd лазером, концентрация сyt c 0,3 ммоль/л.
Изменения сигнала ЭПР cyt с (Fe2+–NO) под действием излучения He–Cd лазера представлены на рис. рис. 4.21Б. Хорошо видно, что амплитуда ЭПР сигнала уменьшается вдвое в течение 30 сек или 1 мин, в зависимости от использованной интенсивности лазерного света. Эти данные говорят о том, что од действием излучения лазера происходит фотодиссоциация комплексов цитохрома c с NO:
cyt с (Fe2+–NO) → cyt с (Fe2+) + NO
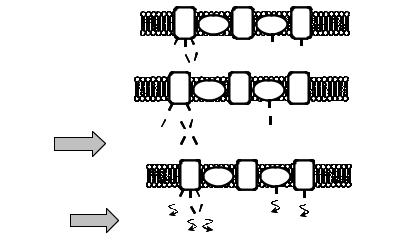
В самое последнее время появились сообщения о том, что окись азота, образующаяся в митохондриях благодаря активности митохондриального фермента NO-синтазы, тормозит работу дыхательной цепи благодаря образованию комплексов NO с цитохромами, цитохромоксидазой и железо-серными центрами, причем светочувствительностью обладают в той или иной степени все эти комплексы NO c железо-содержащими переносчиками электронов (см. схему на рис. 4.22).
32
Внутренняя |
I |
Q |
III |
Cc |
IV |
А |
мембрана |
||||||
митохондрий |
HS S |
S |
|
Fe |
a3(Fe) |
|
|
|
|
|
|||
|
|
Fe |
|
|
|
|
|
I |
Q |
III |
Cc |
IV |
Б |
+ NO
|
|
S |
Fe a |
|
(Fe) |
||
S S |
3 |
||||||
NO |
Fe |
NO |
|
|
|
||
NO |
|||||||
|
|||||||
NO NO
|
I |
|
Q III Cc |
IV |
В |
+ Лазер |
S S |
S |
Fe |
a3(Fe) |
|
NO |
Fe |
NO |
NO |
|
|
|
|
|
|||
|
NO |
|
NO |
|
|
Рис. 4.22. Иллюстрация действия NO на митохондриальную цепь транспорта электронов: А — элементы внутренней мембраны митохондрий до взаимодействия с NO; Б — NO ингибирует гемовые ферменты цитохром с и цитохром с оксидазу. Вследствие этого снижается потребление кислорода, синтез АТР и повышается продукция свободных радикалов; В — лазерное излучение вызывает фотолиз нитрозильных комплексов элементов митохондриальной электрон-транспортной цепи и восстанавливает дыхание и синтез АТФ.
Низкоэнергетические лазеры широко применяются в практической медицине, однако до последнего времени не были известны первичные фотохимические реакции, лежащие в основе терапевтического действия лазерного облучения. В самое последнее время были получены данные о том, что существует как минимум три таких реакции: (1) фотодинамическое перекисное окисление липидов (ФЛПО),
(2) фотореактивация Cu-Zn-супероксиддисмутазы и (3) фотолиз NO-геминовых комплексов.
Один из ранних эффектов ФЛПО — модификация Ca-АТФазы, которая
превращается из насоса в канал, через который ионы Ca2+ проникают в цитоплазму, тем самым активируя клетку. При облучении крови гелий-неоновым лазером (633 нм) ФЛПО приводит к предстимуляции (priming) фагоцитов, что может объяснить антимикробный и сосудорасширяющий эффекты облучения крови He–Ne-лазером. Реакция фотореактивации супероксиддисмутазы может обеспечить защиту NO от связывания супероксидным радикалом, а фотолиз NOгеминовых комплексов – привести к высвобождению NO. Все это в конечном итоге приводит к расслаблению стенок кровеносных сосудов, которое является одним из наиболее изученных проявлений действия лазерного облучения крови. Действие лазерного излучения может приводить также к активации работы дыхательной цепи митохондрий за счет отщепления оксида азота от переносчиков электронов,
33
таких как цитохром с и цитохромоксидаза. Отдаленное действие лазерного облучения связано с активацией биосинтеза ряда ферментов, которая опосредована первичными механизмами улучшения биоэнергетики и кальций-зависимой активацией клеточных процессов.
В заключение обобщим системные эффекты низкоинтенсивных оптических излучений
Первичные системные эффекты НИЛИ:
Увеличение бактерицидности,
Индукция синтеза белков: индуцибельной NO-синтазы, цитокинов, супероксиддисмутазы, коллагена,
Активация пролиферации клеток;
Вторичные системные эффекты НИЛИ:
Ускорение заживления ран,
Улучшение микроциркуляции крови за счёт вазодилатации микрососудов, уменьшения агрегационных свойств клеток крови, формирования новых микрососудов.
34
