
- •Введение в обмен веществ
- •Основные особенности разных фаз метаболизма
- •Глава I. Энергетический обмен
- •1.1. Свободная энергия и законы термодинамики
- •1.1. Макроэргические соединения
- •Стандартная свободная энергия гидролиза органических фосфатов
- •1.1.2. Пути синтеза атф и его роль
- •1.1.3. Окислительно – восстановительное равновесие, окислительно –восстановительный потенциал
- •Стандартные потенциалы некоторых окислительно- восстановительных систем
- •1.2. Биологическое окисление
- •1.2.1. Характеристика биологического окисления
- •Строение комплексов полиферментного ансамбля дыхательной цепи митохондрий
- •1.2.2. Сопряжение биологического окисления и окислительного фосфорилирования
- •1.2.3. Регуляция скорости дыхания митохондрий
- •1.2.4. Разобщение дыхания и фосфорилирования
- •Краткая характеристика некоторых ионо(протоно)форов
- •1.2.5. Патология биоэнергетических процессов
- •II. Наследственные и приобретенные дефекты в работе промежуточных переносчиков этц:
- •III. Недостаток кислорода (гипоксия):
- •IV. Наличие разобщителей биологического окисления и фосфорилирования.
- •1.2.6. Механизмы защиты от токсического действия кислорода
- •А) Антиоксиданты ферментативной природы
- •Б) Антиоксиданты неферментативной природы
- •Роль катионов металлов с переменной валентностью в свободно-радикальных реакциях
- •В) Антиоксиданты внеклеточных жидкостей
- •1.3. Микросомальное окисление
- •Глава II
- •2.1.2. Регуляция процесса окисления пирувата
- •2.1.3. Патология декарбоксилирования пирувата
- •2.2. Цикл трикарбоновых кислот
- •2.2.1. Последовательность реакций цтк
- •2.2.2. Энергетическая ценность процесса
- •Образование макроэргических соединений в цтк
- •2.2.3. Участие витаминов в цтк
- •2.2.4. Биологические функции цикла Кребса
- •2.2.5. Регуляция превращений цитрата
Глава I. Энергетический обмен
1.1. Свободная энергия и законы термодинамики
Жизнь существует и развивается за счет поступающей извне свободной энергии. Энергетический обмен животной клетки относится к органотрофному (у растений - фототрофный) типу, при котором накопление энергии происходит в результате деградации органических веществ. Сущность биоэнергетики составляет процесс превращения химической энергии органических соединений, поступающих из пищи, в различные формы полезной энергии (механическую, электрическую, световую, химическую, тепловую и т.д.).
Энергетический обмен живого организма подчиняется законам термодинамики.
Первый закон сохранения энергии утверждает, что энергию нельзя ни создать, ни уничтожить, она может только переходить из одной формы в другую.
В торойзакон
термодинамики позволяет предсказать
направление биохимических
реакций. Согласно ему все процессы идут
в
направлении возрастания общей энтропии
(меры разупорядоченности)
системы и окружающей среды. Увеличение
энтропии препятствует возврату к
исходному состоянию. Поэтому все реакции,
которые сопровождаются увеличением
разупорядоченности, необратимы, и для
их протекания необходимы затраты
дополнительной энергии. Часть энергии
системы, которая может использоваться
для совершения работы при постоянных
температуре
и давлении, называется свободной.
Если ее значения имеют
отрицательный знак, то реакция происходит
самопроизвольно с выделением добавочной
энергии (экзэргоническая
реакция),
а положительные цифры показателя
свидетельствуют о необходимости затрат
энергии (эндэргоническая
реакция).
Если система находится в состоянии
равновесия (А В), то количество
свободной энергии равно нулю. Ее величины
обычно выражают в джоулях на моль или
калориях на моль вещества (Дж/моль или
кал/моль).
торойзакон
термодинамики позволяет предсказать
направление биохимических
реакций. Согласно ему все процессы идут
в
направлении возрастания общей энтропии
(меры разупорядоченности)
системы и окружающей среды. Увеличение
энтропии препятствует возврату к
исходному состоянию. Поэтому все реакции,
которые сопровождаются увеличением
разупорядоченности, необратимы, и для
их протекания необходимы затраты
дополнительной энергии. Часть энергии
системы, которая может использоваться
для совершения работы при постоянных
температуре
и давлении, называется свободной.
Если ее значения имеют
отрицательный знак, то реакция происходит
самопроизвольно с выделением добавочной
энергии (экзэргоническая
реакция),
а положительные цифры показателя
свидетельствуют о необходимости затрат
энергии (эндэргоническая
реакция).
Если система находится в состоянии
равновесия (А В), то количество
свободной энергии равно нулю. Ее величины
обычно выражают в джоулях на моль или
калориях на моль вещества (Дж/моль или
кал/моль).
1.1. Макроэргические соединения
В изучении процессов биоэнергетики большую роль сыграл Ф. Липман, который ввел представление о «богатых энергией фосфатах» и «богатой энергией фосфатной связи». Ученый предложил символ ~Р, свидетельствующий о наличии высокоэнергетической (макроэргической) фосфатной связи. Значок ~ (греческая буква «тильда») означает, что перенос группы, присоединенной указанной связью, на подходящий акцептор сопровождается одномоментным выделением большого количества свободной энергии. Стандартная свободная энергия гидролиза ряда биохимически важных органических фосфатов приведена в таблице 2.
Таблица 2
Стандартная свободная энергия гидролиза органических фосфатов
-
Соединение
Стандартная энергия гидролиза (∆G0)
кДж/ моль
ккал/моль
Фосфоенолпируват
Карбамоилфосфат
1,3-Дифосфоглицерат
Креатинфосфат
А
 ТФ
АДФ + Рi
ТФ
АДФ + РiА
 ДФ
АМФ
+ Рi
ДФ
АМФ
+ РiПирофосфат
Глюкозо-1-фосфат
Фруктозо-6-фосфат
АМФ
Глюкозо-6-фосфат
Глицерол-3-фосфат
-61, 9
-51,4
-49,3
-43,1
-30,45
-27,6
-27,6
-20,9
-15,9
-14,2
-13,8
-9,2
-14,8
-12,3
-11,8
-10,3
-7,3
-6,6
-6,6
-5,0
-3,8
-3,4
-3,3
-2,2
Самой многочисленной группой макроэргов являются фосфаты, хотя имеются представители и других классов:
Органические фосфаты:
а) нуклеозидполифосфаты: АТФ, УТФ, ГТФ и др.
б) ацилфосфаты: в) амидинфосфаты: г) енолфосфаты:
Фосфоенолпируват
Тиоэфиры –
активные
формы различных кислот, полученных в
результате взаимодействия с НSКоА:
Ониевые
соединения –
из всех
макроэргов
обладают самым малым запасом свободной
энергии, которая обычно используется
только в виде химической (например,
S-аденозилметионин): Креатинфосфат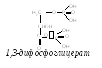
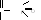
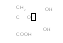
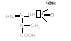
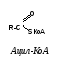
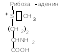
S-аденозилметионин
Д
среди них особое
положение занимает аденозинтрифосфат
(АТФ): во
всех живых клетках данный макроэрг
выступает в качестве депо для
кратковременного хранения и переноса
химической энергии на молекулярном
уровне. В самых общих чертах можно
получить представление об этой функции
АТФ при рассмотрении схемы, показывающей
взаимопреобразования АТФ и АДФ.
Химическая природа этих превращений
очень проста: разрыв фосфоангидридной
связи в результате гидролиза
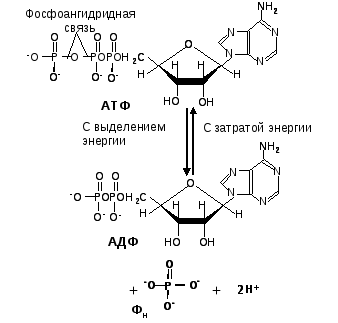
клетках данный макроэрг выступает в качестве депо для кратного хранения и переноса химической энергии на молекулзультате гидролиза АТФ или ее образование в ходе фосфорилирования (синтез АТФ). Однако такой подход односторонен. Для полного понимания необходимо рассмотреть энергетику двух процессов. Следует иметь в виду, что АТФ гораздо менее стабильная молекула, чем аденозиндифосфат (АДФ). Другими словами, АТФ более высокоэнергетическое соединение, чем АДФ.
П
 ревращение
АТФ АДФ + Фн
сопровождается
освобождением
энергии, а обратная реакция АДФ + Фн
АТФ
– требует её затраты. Аналогичные
соображения применимы для описания
гидролиза АТФ до АМФ и пирофосфата
(ФФн).
ревращение
АТФ АДФ + Фн
сопровождается
освобождением
энергии, а обратная реакция АДФ + Фн
АТФ
– требует её затраты. Аналогичные
соображения применимы для описания
гидролиза АТФ до АМФ и пирофосфата
(ФФн).
О братимый
процесс АТФ АДФ +Фн
(или АМФ + ФФн)
составляет молекулярную основу переноса
химической энергии внутри
всех живых клеток.
братимый
процесс АТФ АДФ +Фн
(или АМФ + ФФн)
составляет молекулярную основу переноса
химической энергии внутри
всех живых клеток.
Когда разрушается высокоэнергетический компонент пищи, например, углевод, освобождающаяся энергия используется для образования АТФ. Если клетка нуждается в энергии (для таких процессов, как биосинтез, сокращение мышцы или транспорт соединений через мембраны), АТФ гидролизуется с её выделением (рис. 3).

Рис. 3. Пути использования энергии макроэргов
