
- •1. Алканы
- •Введение
- •1. Классификация органических соединений
- •2. Классификация органических реакций
- •3. Способы образования ковалентной связи
- •4. Гибридизация атомных орбиталей и форма органических молекул
- •4.1. Sp3-Гибридизация
- •4.2. Sр2-Гибридизация
- •4.3. Sp-Гибридизация
- •5. Алканы
- •Гомологический ряд алканов. Число структурных изомеров
- •5.1. Физические свойства
- •5.2. Химические свойства
- •5.2.1. Галогенирование
- •Зависимость реакционной способности галогенов от энергии связи h–Hal
- •5.2.2. Нитрование
- •5.3.4. Декарбоксилирование карбоновых кислот
- •6.2. Плоскополяризованный свет. Оптическая активность
- •6.3. Строение молекул и оптическая активность
- •6.4. Обозначение конфигураций
- •7. Циклоалканы
- •7.1 Номенклатура. Изомерия
- •7.2. Физические свойства
- •7.3. Типы напряжения
- •7.4. Строение
- •Теплоты сгорания и энергии напряжения циклоалканов
- •7.4.1. Особенности пространственного строения некоторых циклоалканов
- •7.5. Химические свойства
- •7.6. Способы получения
- •8.1. Физические свойства
- •Физические свойства алкенов
- •8.2. Химические свойства
- •8.2.1. Присоединение галогенов
- •8.2.1.1. Механизм реакции
- •8.2.1.2. Реакционная способность галогенов в реакции АdЕ
- •8.2.2. Присоединение галогеноводородов
- •8.2.2.1. Механизм реакции
- •8.2.2.2. Направление электрофильного присоединения
- •8.2.2.3. Реакционная способность и селективность
- •8.2.2.4. Перегруппировка
- •Механизм реакции
- •8.2.3. Присоединение бромистого водорода в присутствии
- •1. Инициирование:
- •2. Рост цепи:
- •3. Обрыв цепи:
- •8.2.4. Присоединение серной кислоты
- •8.2.5. Гидратация алкенов. Присоединение спиртов
- •8.2.6. Гидроборирование алкенов
- •8.2.7. Алкилирование алкенов
- •8.2.8. Гидрирование. Теплота гидрирования
- •8.2.9. Теплота гидрирования и устойчивость алкенов
- •8.2.10. Окисление
- •8.2.11. Полимеризация алкенов
- •8.2.12. Реакция аллильного замещения. Галогенирование
- •8.3. Способы получения алкенов
- •9.1. Устойчивость сопряженных диенов
- •9.2. Химические свойства
- •9.2.1. Электрофильное присоединение
- •9.2.2. 1,2- И 1,4-Присоединение. Кинетический контроль, термодинамический контроль
- •9.2.3. Диеновый синтез. Реакция Дильса-Альдера
- •9.2.4. Полимеризация
- •9.3. Способы получения
- •10. Алкины
- •Характеристики химических связей в молекуле алкинов
- •10.1. Физические свойства
- •10.2. Химические свойства
- •10.2.1. Реакции присоединеня
- •10.2.1.1. Каталитическое гидрирование и восстановление
- •10.2.1.2. Реакции электрофильного присоединения Галогенирование
- •Гидрогалогенирование
- •Гидратация
- •10.2.1.3. Нуклеофильное присоединение
- •10.2.2. Кислотность алкинов
- •Константы кислотности некоторых соединений
- •10.2.3. Взаимодействие алкинов с карбонильными соединениями
- •10.2.4. Окисление алкинов
- •10.2.5. Радикальное присоединение бромоводорода
- •10.3. Способы получения
- •11. Арены
- •11.1. Сравнение свойств бензола со свойствами алкенов
- •11.2. Теплота гидрирования. Энергия резонанса
- •11.3. Строение бензола
- •11.4. Ароматичность
- •11.5. Физические свойства
- •Физические свойства аренов
- •11.6. Химические свойства
- •11.6.1. Электрофильное замещение
- •11.6.2. Свободнорадикальное замещение в боковой цепи аренов
- •11.6.3. Реакции окисления
- •11.7. Методы синтеза аренов
- •12.1. Влияние заместителей на реакционную способность бензольного кольца
- •12.2. Влияние заместителя на выбор места электрофильной атаки
- •13. Многоядерные ароматические соединения
- •13.1. Нафталин
- •13.2. Антрацен и фенантрен
- •14. Гетероциклические соединения
- •14.1. Пятичленные гетероциклы
- •14.1.1. Строение
- •14.1.2. Химические свойства
- •14.1.3. Способы получения
- •14.2. Пиридин
- •14.2.1. Строение пиридина
- •14.2.2. Химические свойства
- •14.3. Хинолин
- •15. Галогеналканы
- •15.1. Нуклеофильное замещение
- •15.1.1. Бимолекулярное нуклеофильное замещение
- •15.1.2. Мономолекулярное нуклеофильное замещение
- •15.1.3. Сравнение реакций sn 1 и sn 2
- •15.2. Реакции отщепления (элиминирование)
- •15.2.1. Бимолекулярное отщепление е2
- •15.2.2. Мономолекулярное отщепление е1
- •15.2.3. Сравнение реакций нуклеофильного замещения и элиминирования
- •15.3. Методы синтеза галогеналканов
- •16.2. Нуклеофильное замещение, протекающее через стадию образования дегидробензола, - отщепление - присоединение
- •16.3. Бимолекулярное нуклеофильное замещение sn2Ar
- •16.4. Ориентация при нуклеофильном замещении в ароматическом кольце
- •17. Магнийорганические соединения
- •17.1. Получение и строение магнийорганических соединений
- •17.2. Синтез спиртов и кислот
- •Библиографический список
- •Оглавление
- •Часть 1
Теплоты сгорания и энергии напряжения циклоалканов
|
Размер цикла |
Теплота сгорания на группу СН2, кДж/моль |
Энергия напряжения на группу СН2, кДж/моль |
Отклонение от угла 109о28при плоском расположении атомов |
Вид напряжения |
|
1 |
2 |
3 |
4 |
5 |
|
Ациклические соединения |
659,0 |
|
|
Напряжение отсутствует |
|
Малые 3 4 |
697,6 686,7 |
38,5 27,7 |
24о44 9о44 |
Угловое напряжение |
|
Нормальные 5 6 7 |
664,5 659,0 662,8 |
5,5 0,0 3,8 |
0о44 -5о16 -9о33 |
Угловое напряжение (невелико) и торсионное напряжение (невелико) |
|
Средние 8 9 10 11 |
664,1 664,9 664,1 663,2 |
5,1 5,9 5,1 4,2 |
-12о46 -15о16 -17о16 -18о54 |
Угловое и торсионное напряжение, трансанулярные взаимодействия* |
|
Большие 12 13 14 |
659,9 660,7 659,0 |
0,9 1,7 0,0 |
-20о16 -21о25 -22о25 |
Напряжение отсутствует, сравнимы с н-алканами с длинными цепями |
*Трансанулярное взаимодействие – отталкивание ковалентно несвязанных атомов, расположенных на противоположных сторонах цикла.
7.4.1. Особенности пространственного строения некоторых циклоалканов
В циклопропане угол между углерод-углеродными связями С-С-С равен 60о. Атомы углерода не могут располагаться так, чтобы позволить sp3-орбиталям быть направленными друг к другу. В этом случае перекрывание sp3-орбиталей меньше, связь слабее, чем в случае обычной С-С-связи ациклического соединения (рис. 7.2).
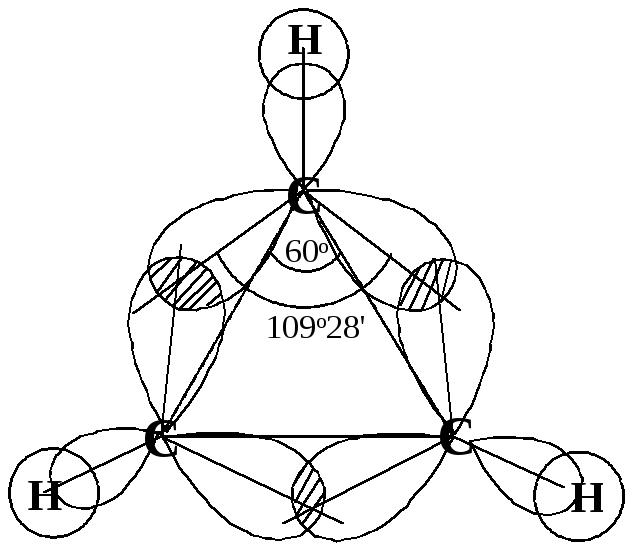
Рис. 7.2. Молекула циклопропана. Оси sp3-гибридных облаков лежат вне линий, соединяющих ядра атомов («банановая» связь)
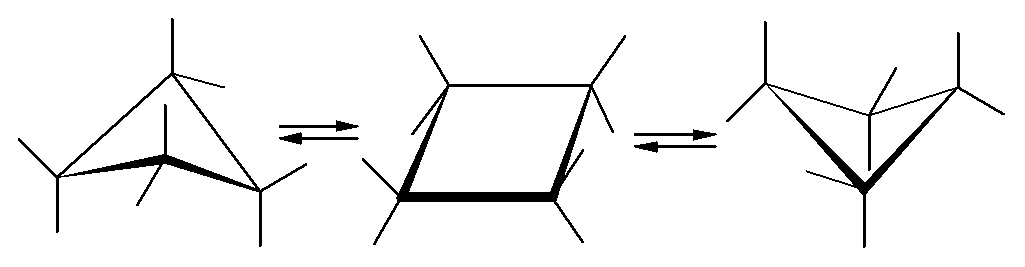
Конформации циклобутана. Циклобутан - слегка изогнутая молекула, но поскольку степень изогнутости молекулы циклобутана мала, а барьер перехода от одной конформации к другой низок, то производные циклобутана можно считать практически плоскими.
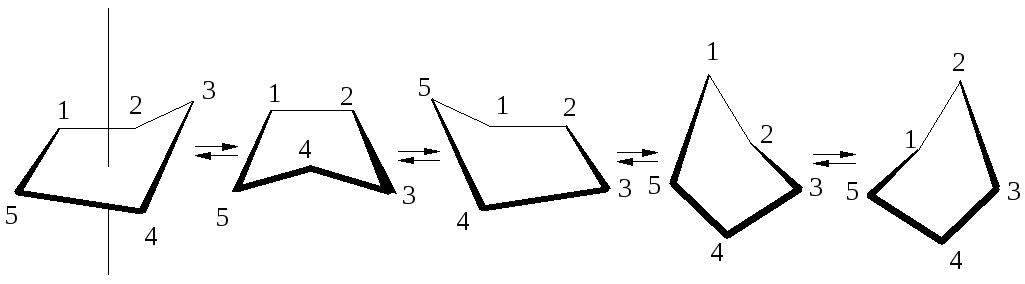
Конформации циклопентана. Молекула циклопентана изогнута (форма конверта). Эта изогнутость может перемещаться по кольцу в результате движения одного атома вверх, а соседнего с ним атома – вниз. Каждый атом в молекуле совершает такие последовательные движения, которые в целом можно представить как вращение кольца вокруг верикальной оси. Этот процесс называется псевдовращение.
Конформации циклогексана. Циклогексан в противоположность другим циклоалканам с размером цикла до С12 существует в виде почти ненапряженных конформеров. Наиболее стабильной является форма кресла. В этом конформере все углы между связями равны тетраэдрическим (109°28), следствием чего является отсутствие углового напряжения.
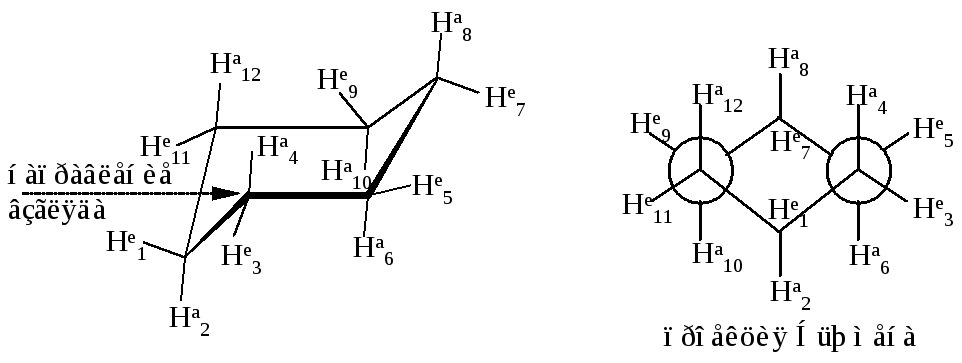
Если посмотреть вдоль любой из углерод-углеродных связей, то в каждом случае имеется идеальная заторможенная конформация, это означает, что конформация кресла свободна и от торсионного напряжения.
В молекуле циклогексана в форме кресла двенадцать связей С -Н различают по положению в пространстве: шесть аксиальных связей (символ “а”) направлены параллельно главной оси попеременно вверх и вниз. Другие шесть связей направлены к “экватору” молекулы и так же - вверх и вниз, их называют экваториальными (символ “е”).
В монозамещенном циклогексане группа G может занимать аксиальное или экваториальное положение. Аксиальный конформер из-за отталкивания между заместителями у атома С1 и у атомов С3 и С5 (напряжение Ван-дер-Ваальса) богаче энергией, чем экваториальная форма. Различие в энергиях таких форм зависит от характера заместителя.
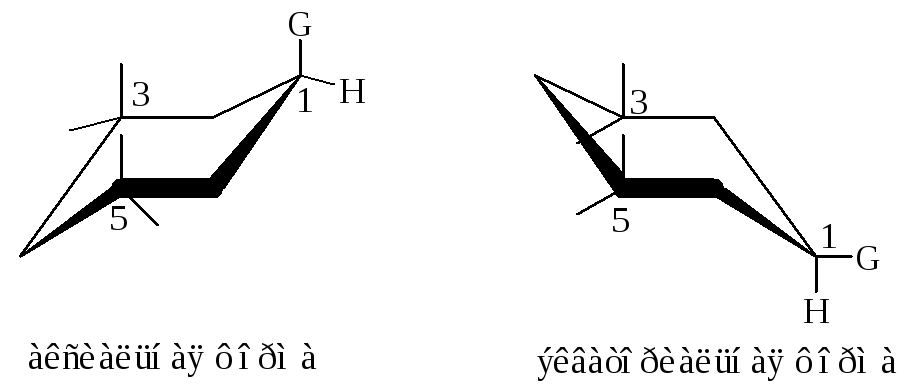
Так, экваториальная конформация метилциклогексана более устойчива, чем аксиальная, различие в энергии составляет 7,1 кДж/моль. При температуре 25 оС 95 % молекул метилциклогексана находится в экваториальной конформации и лишь 5 % - в аксиальной.
