
- •Министерство образования российской федерации
- •1. Ациклические неразветвленные углеводороды
- •2. Моноциклические незамещенные углеводороды
- •3. Ациклические разветвленные углеводороды
- •4. Моноциклические замещенные ароматические углеводороды
- •5. Конденсированные полициклические углеводороды
- •6. Органические соединения с характеристическими группами, содержащими углерод, водород, кислород, азот, галогены, серу
- •6.1. З а м е с т и т е л ь н а я н о м е н к л а т у р а (номенклатура замещения).
- •7. Дополнения к разделам 1...6
- •Исходные ониевые ионы (не обязательно способные к независимому существованию)
- •8. Органические соединения с хиральным центром ( r,s - номенклатура )
- •Убывание старшинства некоторых атомов в зависимости от убывания атомного номера элемента
- •Приложение 1 сохраняемые тривиальные названия (предпочтительны при употреблении)
- •Приложение 2 наиболее употребительные радикалы
- •Cписок использованных источников
- •Оглавление
- •Учебное издание
8. Органические соединения с хиральным центром ( r,s - номенклатура )
8.1. Атом, связанный с четырьмя разными атомами (группами), называют асимметрическим.
Асимметрический атом можно назвать центром хиральности, поскольку он находится в центре хиральной тетраэдрической структуры.

8.2. Названия хиральных соединений уточняют добавлением к названию символов R и S, выбираемых в соответствии с правилом последовательности.
8.3. Правило последовательности служит для установления старшинства атомов или групп атомов. Оно выражается сдедующим образом: a > b > c > d, где знак “>“ означает старше.
8.4. Атом с большим атомным номером является старшим относительно атома с меньшим атомным номером (табл. 5).
Т а б л и ц а 5
Убывание старшинства некоторых атомов в зависимости от убывания атомного номера элемента
|
Химический символ элемента |
I |
Br |
Cl |
S |
F |
O |
N |
C |
H |
|
Атомный номер элемента |
53 |
35 |
17 |
16 |
9 |
8 |
7 |
6 |
1 |
![]()
убывание старшинства
П р и м е р :

17 8 6 1
Cl > O > C > H
8.5. Если рассматриваемые атомы одинаковы, то сопоставляют старшинство последующих атомов.
П р и м е р :

|
R |
Атомы, связанные с атомом углерода
|
|
|
|
Благодаря
тому , что атом
![]() в
изопропиле связан с двумя атомами
углерода и одним атомом водорода, он
является старше атома
в
изопропиле связан с двумя атомами
углерода и одним атомом водорода, он
является старше атома
![]() в метиле, в
котором углерод связан с тремя атомами
водорода.
в метиле, в
котором углерод связан с тремя атомами
водорода.


Углеродный атом со свободной валентностью в радикале изостроения всегда старше аналогичного атома в радикале нормального строения.
8.6. Изображают тетраэдрическую схему молекулы таким образом, чтобы младший атом (или группа) (в данном случае d) располагался всегда на вершине тетраэдра.

8.7. Опрокидывают гипотетический тетраэдр о т с е б я через одно из ребер основания (в данном случае через ребро ac) так, чтобы младший атом (или группа) (в данном случае d) был закрыт хиральным центром.

Младший атом (или группа) d удален от наблюдателя и расположен за плоскостью листа. Глаз наблюдателя расположен перед плоскостью листа.
Данное соединение существует в виде двух энантиомерных форм.
Если старшинство атомов (или групп) убывает по часовой стрелке, то это R-конфигурация (лат. rectus - правый). Если старшинство атомов (или групп) убывает против часовой стрелки, то это S-конфигурация (лат. sinister - левый).
|
|
|
|
a > b > c R-конфигурация |
c < b < a S-конфигурация |
Символы R и S помещают перед названием соединения и заключают их в скобки. После них ставится дефис.
П р и м е р:
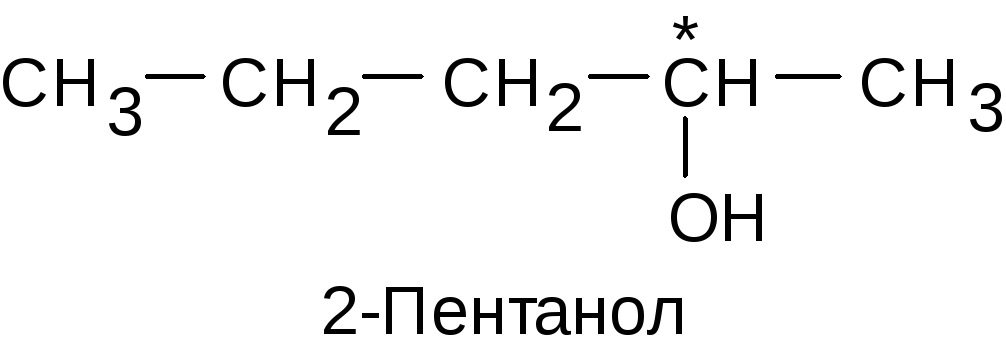
|
Старшинство групп |
|
|
Хиральная тетраэдрическая структура с младшим атомом на вершине |
|
|
Основание опрокинутого о т с е б я тетраэдра (атом водорода скрыт за хиральным центром) |
|
Энантиомерные формы и их названия:
|
|
|
|
|
|
|
(R)-2-Пентанол |
(S)-2-Пентанол |
8.8. Соединения с хиральным центром могут быть представлены с помощью проекций Фишера. В этом случае для изображения молекулы используются пересекающиеся горизонтальные и вертикальные линии; точка пересечения этих линий обозначает хиральный центр, находящийся в плоскости бумаги. Атомы (группы), находящиеся сверху или снизу от центрального атома, располагаются за плоскостью бумаги, а атомы (группы), находящиеся справа и слева - перед плоскостью бумаги. При этом главную цепь располагают вертикально, а ее старшую группу - вверху.
|
|
|
При таком изображении молекулы для определения R,S-конфигурации необходимо видоизменить проекцию Фишера таким образом, чтобы младший атом (или группа) был расположен вверху или внизу этой проекции. Для этого в проекции Фишера надо переместить по или против часовой стрелки т р и атома (или группы), включая младший, таким образом, чтобы последний оказался внизу или вверху проекции. Затем посмотреть, как убывает старшинство трех других атомов (групп): по часовой стрелке (R-конфигурация) или против часовой стрелки (S-конфигурация).
П р и м е р:


Проекция Фишера
Младший атом (группа): H

|
П е р е м е с т и т ь группы H, CH2OH, Cl по часовой стрелке, не трогая группы CH3 |
П е р е м е с т и т ь группы H, CH3 , Cl против часовой стрелки, не трогая группы CH2OH |
|
|
|
|
|
|
Старшинство трех других групп: Cl > CH2OH > CH3
Cтаршинство убывает по часовой стрелке.
Полное название предложенной проекции Фишера:
(R)-2-Хлоро-1-пропанол
9. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ОДНУ ДВОЙНУЮ УГЛЕРОД-УГЛЕРОДНУЮ СВЯЗЬ (E,Z - номенклатура)
9.1. Рассматривают расположение атомов или групп, находящихся у двоесвязанных атомов, относительно некоторой воображаемой плоскости, которая называется плоскостью сравнения. Обычно принято, что эта плоскость совпадает с плоскостью двойной связи и перпендикулярна плоскости бумаги. При этом атомы, связанные непосредственно с двоесвязанными атомами, расположены в плоскости бумаги.
9.2. В названиях соединений расположение атомов или групп вокруг одной двойной связи обозначается символами Z и E, основанными на правиле последовательности.
9.3. В соответствии с правилом последовательности (разд. 8.3...8.5) определяют старшинство атомов (или групп) у каждого из двоесвязанных атомов.
П р и м е р:

-
Старшинство групп у каждого из двоесвязанных атомов углерода

9.4. Рассматривают взаимное расположение обоих старших по правилу последовательности атомов (или групп), стоящих у двоесвязанных атомов углерода, относительно плоскости сравнения. Если оба старших атома (или группы) находятся по одну сторону плоскости сравнения, то для обозначения этой конфигурации используется буква Z (нем. Zusammen - вместе). Если же оба старших атома (или группы) находятся по разные стороны плоскости сравнения, то для обозначения этой конфигурации используется буква E (нем. Entgegen - напротив). Префиксы E и Z, заключенные в скобки, с дефисом после них обычно ставятся перед названием.
П р и м е р ы:

|
Старшинство групп у каждого из двоесвязанных атомов углерода: |
|
|
Расположение старших групп относительно плоскости сравнения: |
Группы
находятся по разные стороны плоскости сравнения |
Полное название: (Е)-2,4-Диметил-3-гексен

|
Старшинство групп у каждого из двоесвязанных атомов углерода: |
|
|
Расположение старших групп относительно плоскости сравнения: |
Атом Сl и группа CN расположены по одну сторону плоскости сравнения |
Полное название: (Z)-2-Хлорометакрилонитрил
9.5. E,Z-номенклатура используется для названия геометрических изомеров. При этом возможно использование классических цис- и транс- обозначений для определения пространственного расположения одинаковых или сходных групп относительно плоскости сравнения.
|
цис-положение для групп а, а |
транс-положение для групп а, а |
П р и м е р :

|
Старшинство групп у каждого из двоесвязанных атомов углерода: |
|
Полное название: (Е)-3-Метил-2-этил-2-пентеновая кислота
В этом соединении два этильных радикала находятся в цис-положении.















