
- •Ведение
- •Тема 1. Химические и физические свойства природных вод
- •Тема 2. Морфологические и динамические характеристики ледников
- •Средние высоты снеговой границы по широтным поясам северного полушария
- •Тема 3. Залегание и движение грунтовых вод
- •Тема 4. Морфология русла и гидродинамические характеристики потока
- •Тема 5. Построение гидрографа и его генетический анализ
- •Тема 6. Характеристики речного стока
- •Тема 7. Морфометрические характеристики озера
- •Тема 8. Термический режим озер умеренного пояса
- •Тема 9. Строение водохранилища и его заиление
- •Тема 10. Болота и их водный баланс
- •Тема 11. Мировой океан и его части
- •Тема 12. Закономерности распределения температуры, солености и плотности на поверхности и в глубине мирового океана
- •Часть 1. Реки:
- •Часть 2. Озера и водохранилища:
- •Часть 3. Мировой океан:
Ведение
Методические указания к выполнению лабораторных работ по курсу «Общая гидрология» предназначены для студентов-географов и экологов дневной и заочной форм обучения. Они составлены в соответствии с действующей программой и с учетом новейших достижений науки. Тематика и содержание приведенных лабораторных работ ориентированы на работу с подготовленным для географов профильным учебником «Общая гидрология» (авт. Михайлов В.Н., Добровольский А.Д., 1991). В то же время учтена необходимость максимальной активизации самостоятельности студентов.
Методические указания построены таким образом, чтобы студенты получили общие сведения о масштабах и разнообразии различных гидрологических явлений и объектов, закономерностях их распространения, роли в природе и жизни человека, научились определять гидрографические и гидрометрические характеристики и элементы стока, анализировать и обрабатывать любую информацию о водах разного генезиса в различных уголках земного шара.
Методические указания охватывают 12 тем, включающих 22 задания, для выполнения которых необходимо использование картографических и литературных источников, приведенных в библиографическом списке. Каждая тема состоит из двух частей: теоретической и практической. В первой из них приводится необходимый минимум основных понятий и определений, которые обеспечивают возможность успешного выполнения практической части работ. Наличие 2-3 заданий в отдельных темах позволяет более гибко подходить к изучению рассматриваемого раздела, улучшить условия индивидуального подхода в обучении студентов с различным уровнем усвояемости материала. Кроме того, это позволяет углубить и расширить диапазон возможных направлений исследования.
Для успешного выполнения лабораторных работ рекомендуется соблюдать следующие требования:
Задания аккуратно выполняются в отдельной тетради;
Обязательно указываются тема, задание, приводятся табличные и графические материалы, перечисляются этапы выполнения работы, пишется вывод;
Графические материалы выполняются в тетради на миллиметровке или кальке простым карандашом с указанием масштабов, необходимых индексов, легенды, нумерации и подписи к рисункам (выполняется снизу). Готовые графики подклеиваются в тетрадь;
Таблицы нумеруются и подписываются сверху.
Одним из условий прочного усвоения гидрологической науки является знание географической номенклатуры. Ее список, приведенный в конце методических указаний, состоит из трех частей: речной, озерной и морской. Каждая часть включает перечень гидрографических объектов, упомянутых в профильном учебнике, знание которых обязательно.
Выполнение указанных условий и требований в комплексе с самостоятельным творческим подходом к выполнению лабораторных работ обеспечит высокий уровень теоретических знаний и практических умений и навыков у студентов.
Тема 1. Химические и физические свойства природных вод
Материалы и оборудование:
- Миллиметровка (15 х 15 см) – 2 шт;
Простой карандаш, ластик, линейка, циркуль;
Калькулятор.
Понятия и определения.
Вода (Н2О) – слабый электролит, молекула которого состоит из одного водородного (Н+) и одного гидроксильного (ОН-) ионов. Вода является хорошим растворителем химических соединений. Суммарное содержание в воде растворенных неорганических веществ выражают в виде минерализации (М, мг/л, г/л) либо в виде солености (S, 0/00).
По содержанию солей (минерализации или солености) природные воды подразделяют на 4 группы: пресные – менее 10/00, солоноватые – 1-250/00, соленые (морской солености) – 25-500/00, высокосоленые (рассолы) – более 500/00.
К числу главных ионов солей, находящихся в природных водах, относятся отрицательно заряженные ионы (анионы) – НСО3- - гидрокарбонатный, SO4-2 – сульфатный, Cl- - хлоридный и положительно заряженные ионы (катионы) – кальция Са+2, магния Mg+2, натрия Na+, калия К+.
Вода в природе может находиться в твердом (лед), жидком (собственно вода) и газообразном (водяной пар) агрегатных состояниях. Температура, при которой происходит кристаллизация воды, называется температурой замерзания. Изменения температуры замерзания воды связаны с влиянием давления и/или солености. Температура, при которой вода имеет максимальную плотность, называется температурой наибольшей плотности. Она составляет 3,980С. Увеличение солености на каждые 100/00 снижает температуру наибольшей плотности примерно на 20С. Соотношения между температурами наибольшей плотности и замерзания влияют на характер процесса охлаждения воды и вертикальной конвекции.
Задание 1. С помощью круговой диаграммы и прямоугольника Роджерса (рис. 1, А, Б) изобразить в тетради химический состав воды, приведенный в таблице 1.
Таблица 1
Данные о химическом составе природных вод
|
Вариант |
Катионный состав, %экв. |
Анионный состав, %экв. | ||||
|
Са+2 |
Mg+2 |
Na++K+ |
HCO3- |
SO4-2 |
Cl- | |
|
1 |
80 |
10 |
10 |
60 |
25 |
15 |
|
2 |
66 |
30 |
4 |
57 |
21 |
22 |
|
3 |
12 |
49 |
39 |
22 |
63 |
15 |
|
4 |
4 |
70 |
26 |
30 |
70 |
- |
|
5 |
42 |
42 |
16 |
33 |
42 |
25 |
|
6 |
- |
17 |
83 |
61 |
17 |
22 |
|
7 |
75 |
25 |
- |
44 |
56 |
- |
|
8 |
29 |
42 |
29 |
14 |
72 |
14 |
|
9 |
55 |
- |
45 |
15 |
10 |
75 |
|
10 |
20 |
25 |
55 |
25 |
40 |
35 |
|
“б” |
5 |
90 |
5 |
5 |
5 |
90 |
Методические указания.
Для показа химического состава воды на круговой диаграмме (рис. 1, А) следует разделить окружность на две равные части горизонтальной линией, проходящей через ее центр. В верхней части полукруга показать катионный состав, в нижней – анионный.
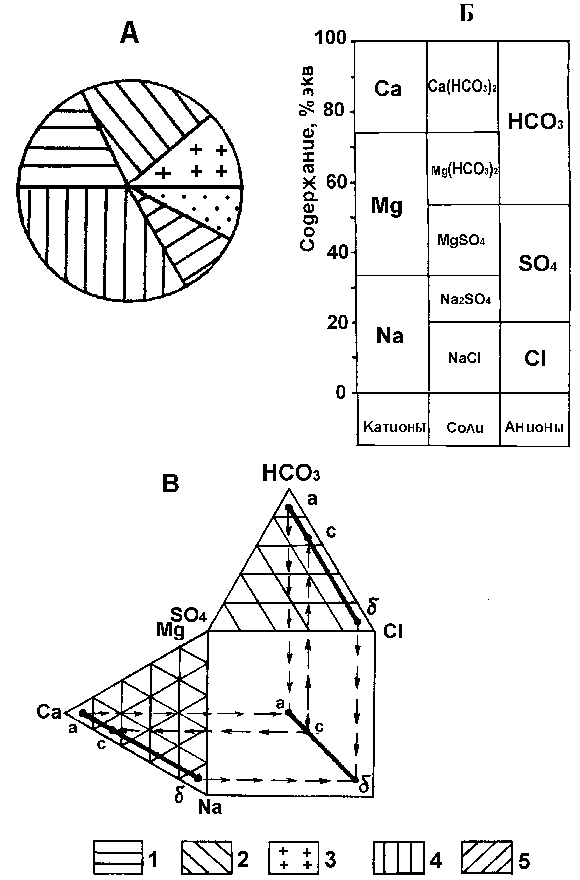
Рис. 1. Графические методы показа химического состава воды
А – круговая диаграмма, Б – прямоугольник Роджерса, В – график Дурова. Катионы: 1 – Са, 2 – Mg, 3 – Na+K. Анионы: 4 – HCO3, 5 – SO4, 6 – Cl
Каждое из полукружий разбить на три части пропорционально процентному составу катионов и анионов. Следует помнить, что 100% катионов или анионов на диаграмме соответствуют 1800 или 1% - 1,80.
Выделенные на диаграмме сектора заштриховать согласно самостоятельно разработанной легенде.
При построении прямоугольника Роджерса в первом и третьем столбцах расположить катионы и анионы снизу вверх в последовательности, определяемой относительной реактивной силой (рис. 1, Б).
Во втором столбце прямоугольника Роджерса указать состав солей в воде, выписать их процентное содержание.
Задание 2. С помощью графика Дурова (рис. 1, В) определить химический состав смеси, образующейся при смешивании воды «а» (один из вариантов таблицы 1) с водой «б» (табл. 1) в пропорции 1:1.
Построить на миллиметровке макет графика Дурова (рис. 1, В).
На катионном и анионном треугольниках определить местоположение точек «а», соответствующих химическому составу воды выбранного варианта.
Спроецировать положения точек на квадрат путем проведения горизонтального пунктира из катионного и вертикального пунктира из анионного треугольников.
Аналогично определить на квадрате положение точки «б».
Исходя из пропорции смешивания 1:1 найти положение точки «с» (смеси вод «а» и «б»), для чего соединить «а» и «б» отрезком и разделить его пополам.
Из точки «с» провести пунктирные проекции на отрезки «а-б» в катионном и анионном треугольниках и определить химический состав полученной смеси, выписав в тетради процентное содержание основных ионов.
Задание 3. По данным таблицы 3 построить график изменения температуры замерзания и температуры наибольшей плотности воды в зависимости от солености и проанализировать его, объяснив различия в ходе замерзания пресной и соленой воды.
Таблица 3
Данные для построения графика Хелланд-Хансена
|
Соленость, S, 0/00 |
0 |
5 |
10 |
15 |
20 |
25 |
30 |
35 |
|
Температура замерзания, tз, 0С |
0,00 |
-0,27 |
-0,54 |
-0,81 |
-1,08 |
-1,35 |
-1,62 |
-1,89 |
|
Температура наибольшей плотности, tп, 0С |
3,98 |
2,93 |
1,85 |
0,77 |
-0,30 |
-1,37 |
-2,45 |
-3,53 |
Методические указания.
На оси абсцисс отложить значения солености, на оси ординат – температуры замерзания и наибольшей плотности. Масштабы выбрать самостоятельно.
По данным таблицы 3 отстроить точки и провести через них прямые. Найти координаты точки пересечения прямых.
Показать на графике область распространения пресных, солоноватых и соленых морских вод.
Используя материалы учебника [13, с.25, 28-35] и лекционный материал объяснить различия в ходе замерзания солоноватых и соленых морских вод, изложив их в тетради.
