
- •Количественное определение спирта этилового в фармацевтических препаратах
- •Глицерол (глицерин)
- •Получение глицерола
- •Чистота
- •Отсутствие мышьяка.
- •Сульфатная зола.
- •Количественное определение
- •Методы, применяемые для количественного определения глицерина и его однокомпонентных растворов (препаратов).
- •Условия метода:
- •Методы, применяемые для количественного определения глицерина в составе многокомпонентных препаратов.
- •Действие. Применение.
- •Формы выпуска
Продолжение лекции по теме «Спирты»
Количественное определение спирта этилового в фармацевтических препаратах
1. По плотности отгона спирта из препарата. Приведен в ОФС ГФ XI издания, выпуск 1, с. 26-29.
Из препарата методом перегонки отгоняют спирт, предварительно ЛП подвергают специальной обработке:
-
Если ЛП содержит летучие вещества (эфир, хлороформ, камфору), то перед перегонкой проводят обработку соответствующими реактивами.
-
Жидкости, содержащие свободный йод, перед дистилляцией обрабатывают цинковой пылью или рассчитанным количеством натрия тиосульфата до обесцвечивания. Летучие кислоты нейтрализуют раствором щелочи, летучие основания – фосфорной или серной кислотой.
Плотность отгона определяют пикнометром. По алкоголеметрическим таблицам находят соответствующее содержание спирта в препарате.
Метод дает достаточно точные результаты, но длителен и
многопроцедурен.
-
Метод ГЖХ. Разработаны методики определения количества спирта в некоторых спиртосодержащих ЛП.
Например, в препарате «Раствор йода 5% спиртовой» должно быть 40% спирта. Йод титруют натрия тиосульфатом, затем вносят навеску в газовый хроматоргаф. Параллельно вносят навеску стандарта - С2H5OH .
По площади пиков рассчитывают содержание спирта этилового в ЛП.
Достоинтства метода:
-
Быстрый
-
Точный
-
Очень чувствительный
Недостаток:
-
Требует специальной аппаратуры и специальной разработки методик для каждого ЛП
3. По температуре кипения ЛП. Применяется для определения спирта в настойках. Приведен в ГФXI, вып. 1, с. 26-29.
Существует зависимость между содержанием спирта в настойке и ее t кипения. В ОФС приведены таблицы, в которых отражается данная зависимость.
Определяют t кипения настойки; по таблице определяют содержание в ней спирта.
Метод менее точный, чем метод 1.
-
Дихроматный метод. Используется для определения малых количеств этанола (около 1%). Предложен для определения примеси этанола в некоторых субстанциях. Применяется редко, считается устаревшим.
Глицерол (глицерин)
МНН: Glycerol
ЛН: Glycerinum
![]()
1, 2, 3-Пропантриол
Получение глицерола
-
Синтетический метод – из пропилена. Основной метод получения глицерина. Пропилен – один из газообразных продуктов крекинга нефти.
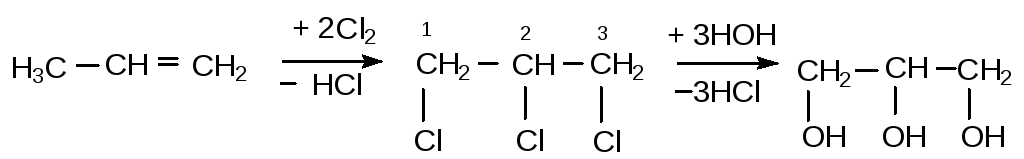
пропилен 1,2,3-трихлорпропан глицерин
(пропен)
-
Из жиров – метод гидролиза в присутствии катализаторов или под давлением перегретого пара при повышенном давлении (220оС и 25 атм).

Очистка глицерина
-
Глицерин подвергают перегонке. Получают глицерин дистиллированный с концентрацией 95-98%.
-
Такой глицерин является хорошим дегидратирующим (водоотнимающим) средством, но в медицине применяться не может, т.к. очень сушит кожу и вызывает ожоги.
-
Поэтому к глицерину дистиллированному прибавляют воду до получения концентрации глицерина 84-88%.
Описание
Прозрачная, бесцветная, сиропообразная жидкость сладкого вкуса, без запаха. Гигроскопичен.
Растворимость
Смешивается с водой и спиртом 95% во всех соотношениях; очень мало растворим в эфире, практически нерастворим в жирных маслах. Плотность от 1,223 до 1,233.
Подлинность
-
Реакция образования акролеина. К глицерину прибавляют водоотнимающее средство – калия гидросульфат и нагревают; появляется неприятный раздражающий запах акролеина. Протекает реакция дегидратации.
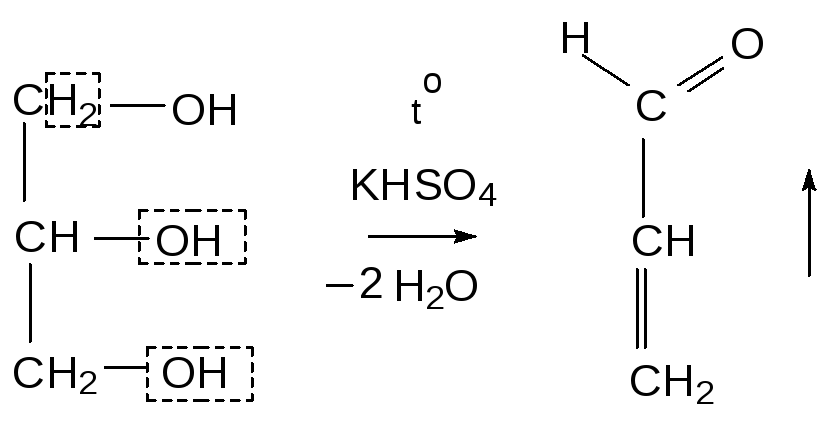
Акролеин
(акрилальдегид)
Акролеин можно доказать по альдегидной ФГ с реактивом Несслера и др. реактивами. Смачивают реактивом фильтровальную бумагу и помещают над пробиркой. На бумаге должно появиться черное пятно (Hg). Реакцию см. в теме «Альдегиды» (Химические свойства).
-
Реакция комплексообразования с меди (II) сульфатом в среде NaOH (см. химические свойства спиртов).
