
Добавил:
Vasya
Опубликованный материал нарушает ваши авторские права? Сообщите нам.
Вуз:
Предмет:
Файл:kinetika_Eakt_kinet_modeli.ppt
X
- •ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- •Я. Х. Вант- Гофф
- •Зависимость скорости реакции от температуры
- •Зависимость ln k от 1/T.
- •Изменение энергии реагирующей системы:
- •ТЕОРИЯ
- •Распределение молекул по скоростям при данной температуре
- •КИНЕТИЧЕСКИЕ МОДЕЛИ ДЛЯ БИОЛОГИЧЕСКИХ СИСТЕМ
- •ОСОБЕННОСТИ КИНЕТИКИ БИОЛОГИЧЕСКИХ СИСТЕМ (БС)
- •Модель Мальтуса.
- •Модель Ферхюльста. Рост популяции, ограниченный ресурсами
- •Вито
- •Совместное существование жертв и хищников
- •ФЕРМЕНТАТИВНЫЙ
- •ОСОБЕННОСТИ ФЕРМЕНТОВ
- •АКТИВНЫЙ ЦЕНТР ФЕРМЕНТА –ЭТО
- •АКТИВНЫЙ ЦЕНТР
- •АКТИВНЫЙ ЦЕНТР АЦЕТИЛХОЛИНЭСТЕРАЗЫ
- •Фермент -химотрипсин
- •Синтезированная модель ключевого элемента активного центра фермента цитохромоксидазы (По
- •РОЛЬ ФУНКЦИОНАЛЬНЫХ ГРУПП
- •ЧАСТО АКТИВНЫЙ ЦЕНТР РАСПОЛОЖЕН НА СТЫКЕ ДОМЕНОВ, ЛИБО В СТАНДАРТНО РАСПОЛОЖЕННОЙ «ВМЯТИНЕ»
- •СУБСТРАТ ОКРУЖЕН МНОГИМИ БОКОВЫМИ ЦЕПЯМИ БЕЛКА
- •МОДЕЛИ АКТИВНОГО ЦЕНТРА ФЕРМЕНТА
- •МОДЕЛЬ «КЛЮЧ – ЗАМОК» (Г.Э.ФИШЕР)
- •ТЕОРИЯ
- •ТЕОРИЯ
- •Изменения структуры активного центра, вызванные субстратом, согласно модели «индуцированного соответствия» Д. Кошланда
- •ИНДУЦИРОВАННОЕ
- •1.ДО СВЯЗЫВАНИЯ С СУБСТРАТОМ ФЕРМЕНТ НАХОДИТСЯ В
- •ЭТАПЫ
- •Генри
- •В реальных системах ни субстрат, ни фермент не являются жесткими молекулами. При связывании
- •ТЕРМОДИНАМИЧЕСКАЯ СУЩНОСТЬ
- •Катализ приводит к ускорению достижения равновесия за счет снижения энергии активации (Еа), часто
- •Разложение перекиси водорода
- •МЕХАНИЗМ ФЕРМЕНТАТИВНОЙ РЕАКЦИИ
- •ТИПЫ ВЗАИМОДЕЙСТВИЙ МЕЖДУ АКТИВНЫМ ЦЕНТРОМ ФЕРМЕНТА И СУБСТРАТОМ
- •Прямые доказательства существования фермент-
- •ВЫВОД УРАВНЕНИЯ
- •Леонор МИХАЭЛИС
- •Допущения:
- •ЗАВИСИМОСТЬ СКОРОСТИ ФЕРМЕНТАТИВНОЙ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ СУБСТРАТА
- •РАССМОТРИМ ФЕРМЕНТАТИВНУЮ РЕАКЦИЮ
- •РАССМОТРИМ ПРИНЦИП ЗАКРЫТОСТИ
- •ВЫРАЗИМ [ES]
- •ОТНОШЕНИЯ КОНСТАНТ СКОРОСТЕЙ
- •ПОЛУЧИМ
- •УЧТЕМ, ЧТО
- •В ИТОГЕ ПОЛУЧИМ УРАВНЕНИЕ
- •Константа Михаэлиса измеряется
- •ЛИНЕЙНЫЕ
- •УРАВНЕНИЕ ЛАЙНУИВЕРА - БЕРКА
- •УРАВНЕНИЕ ЛЭНГМЮРА используется, если отклонения от линейности наблюдаются при высоких концентрациях субстрата
- •УРАВНЕНИЕ ИДИ - ХОФСТИ
- •Зависимость скорости ферментативной реакции (V) от температуры
- •Зависимость скорости ферментативной реакции (V) от рН среды.
- •Оптимальные значения рН для некоторых ферментов
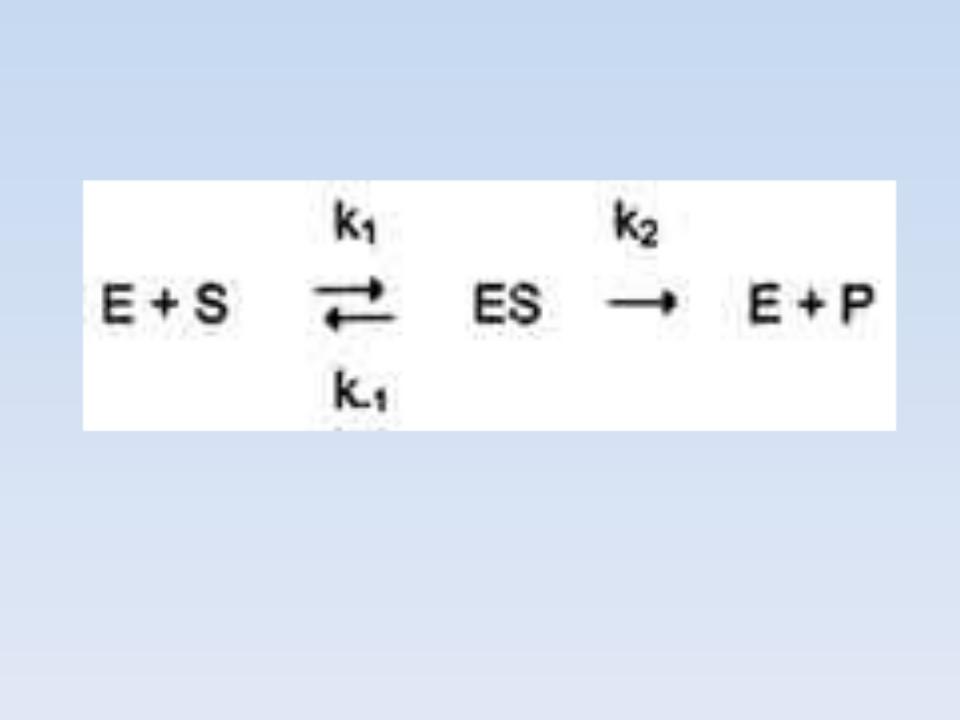
РАССМОТРИМ ФЕРМЕНТАТИВНУЮ РЕАКЦИЮ
1
Е1 – свободный фермент S – субстрат
Р - продукт

РАССМОТРИМ ПРИНЦИП ЗАКРЫТОСТИ
СИСТЕМЫ:
E E1 ES
ОТСЮДА
E1 E ES
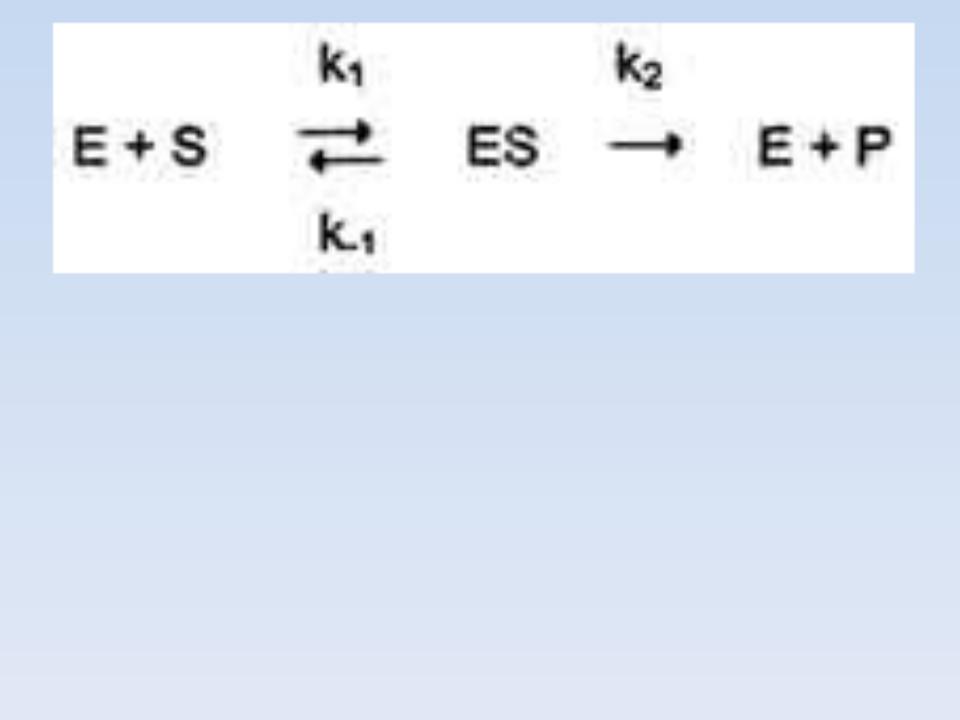
1
V1 |
СКОРОСТЬ ОБРАЗОВАНИЯ И |
РАСЩЕПЛЕНИЯ ФЕРМЕНТ- |
|
|
СУБСТРАТНОГО КОМПЛЕКСА |
V1 d ES k1 E1 S k 1 k2 ES dt

В СТАЦИОНАРНОМ СОСТОЯНИИ V1 =0, ТОГДА
k1 E1 S k 1 k2 ES 0
E1 E ES

k1 ( E [ES ]) S k 1 k2 ES 0

ВЫРАЗИМ [ES]
E S
ES k 1 k 2 S k1

ОТНОШЕНИЯ КОНСТАНТ СКОРОСТЕЙ
k 1 k2 K M k1
ТОГДА ES E S
KM S

1
ЗАПИШЕМ СКОРОСТЬ ФЕРМЕНТАТИВНОЙ РЕАКЦИИ КАК СКОРОСТЬ ОБРАЗОВАНИЯ
ПРОДУКТА
V d P k2 ES dt
ПОДСТАВИМ ВЫРАЖЕНИЕ ДЛЯ ES

ПОЛУЧИМ
V d P |
k2 ES k2 |
E S |
|
KM S |
|||
dt |
|

УЧТЕМ, ЧТО
Vmax k2 E
В ЭТОЙ СИТУАЦИИ ВЕСЬ ФЕРМЕНТ ПОШЕЛ НА ОБРАЗОВАНИЕ ФЕРМЕНТ-СУБСТРАТНОГО КОМПЛЕКСА.
Соседние файлы в предмете Биофизика
