
- •Специфика органической химии
- •Теория гибридизации
- •Типы гибридных орбиталей
- •Первое валентное состояние атома углерода Гибридизация sp3
- •Мезомерный эффект (эффект сопряжения) [±m]
- •Понятие сопряжения
- •Эффекты сопряжения
- •Правило Морковникова
- •Донорно-акцепторные связи. Семиполярные связи
- •Водородная связь
- •Названия ненасыщенных и ароматических углеводородов
- •Номенклатура гетероциклических соединений
- •Номенклатура июпак для производных различных классов органических соединений
- •Изомерия органических соединений
- •Структурная изомерия
- •Изомерия положения
- •Геометрическая изомерия (зеркальная, цис- транс- изомерия)
- •Оптическая изомерия
- •Устройство поляриметра
- •Диастереомеры
- •Номенклатура стереоизомеров
- •Номенклатура Кана, Ингольда, Прелога (кип)
- •Номенклатура стереоизомеров Потапова в.М., Терентьева а.П. И сотрудников
- •2(Ρ),3-диоксипропаналь
- •3(Ρ),4-дихлорпентен-4-аль
- •Классификация органических реакций и реагентов
- •По способу разрыва (образования) химических связей.
- •Классификация реакций по типу превращений в органических веществах
- •Свободные радикалы
- •Понятие о граничных структурах
- •Алканы (парафины)
- •Физические свойства
- •Промышленная переработка алканов (нефти)
- •Некоторые лабораторные способы получения алканов
- •Нитрование алканов
- •Строение малых циклов (циклопропан, циклобутан)
- •Некоторые закономерности реакции отщепления
- •Дегидратация спиртов (отщепление воды)
- •Дегалогенирование дигалогенпроизводных
- •Восстановление алкинов (ацетиленов)
- •Расщепление четвертичных аммонийных солей по Гофману
- •Присоединение галогенов
- •Строение диенов
- •Химические свойства диенов
- •Реакции присоединения
- •Механизм реакции [ae] для сопряженных диенов
- •Некоторые аспекты применения сопряженных диенов
- •Алкины (ацетилены)
- •Способы получения ацетилена
- •Некоторые способы получения гомологов ацетилена
- •Общая характеристика реакционной способности ацетиленов
- •Физические свойства ацетилена
- •Химические свойства
- •Реакции присоединения
- •Реакции нуклеофильного присоединения к ацетиленам
- •Некоторые свойства виниловых эфиров
- •Ароматические углеводороды
- •Признаки ароматичности
- •Направление реакций ароматических соединений
- •II стадия:
- •Мнемоническое правилосмещения электронной плотности под действием заместителя в ядре
- •Нуклеофильное замещение в ароматических системах (snAr)
- •Механизм реакции snAr
- •Галогенпроизводные углеводородов
- •Методы получения галогенпроизводных
- •Замещение водорода на галоген в условиях радикальных процессов (прямое галогенирование алканов)
- •Галогенирование непредельных углеводородов
- •Получение галогенпроизводных из непредельных углеводородов
- •Общая характеристика реакционной способности галогенпроизводных
- •Важнейшие реакции галогенпроизводных
- •Образование металлорганических соединений
- •Содержание
Изомерия органических соединений
Структурная изомерия
Структурными изомерами называют соединения, имеющие одинаковый состав, но различающиеся строением углерод-углеродного скелета. Например:
н-бутан
изо-бутан
Для циклических:
 циклогексан,
циклогексан, метилциклопентан,
метилциклопентан,
 1,3-диметилциклобутан,
1,3-диметилциклобутан, триметилциклопропан
триметилциклопропан
Изомерия положения
Изомерами положения могут быть замещенные алканы, циклоалканы и непредельные соединения:
![]() 1,1-дихлорэтан,
1,1-дихлорэтан,![]() 1,2-дихлорэтан
1,2-дихлорэтан
Циклические соединения:
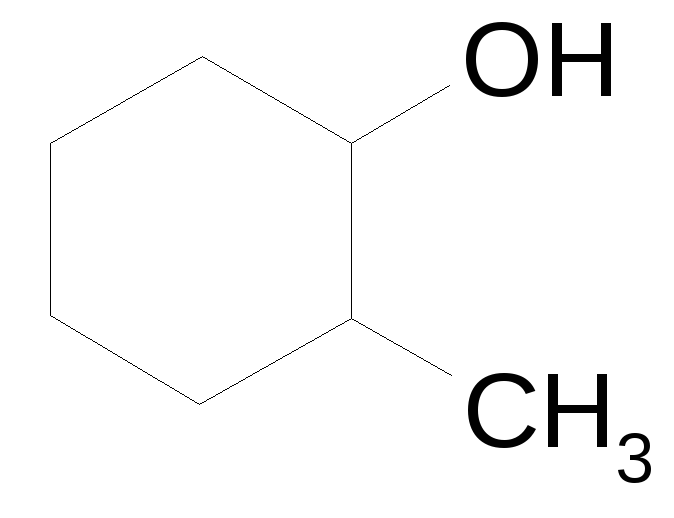 1-метилциклогесанол,
1-метилциклогесанол, 3-метилциклогексанол
3-метилциклогексанол
![]() бутен-2,
бутен-2,![]() бутен-1.
бутен-1.
Геометрическая изомерия (зеркальная, цис- транс- изомерия)
Например, для бутена-2:

 транс-бутен-2,
транс-бутен-2, цис-бутен-2
цис-бутен-2
Изомеры этилендикарбоновой кислоты:
 транс– бутендиовая-1,4 кислота
(фумаровая кислота),
транс– бутендиовая-1,4 кислота
(фумаровая кислота),
 цис– бутендиовая-1,4 кмслота
(малеиновая кислота)
цис– бутендиовая-1,4 кмслота
(малеиновая кислота)
Цис- и транс- изомерия используется , как правило, в тех случаях, когда при двойной связи имеются два атома водорода и два заместителя, причем у каждого атома углерода при двойной связи должны быть различные заместители. Так, метиленмалоновая кислота:
 не является объектом рассмотрения
геометрической (цис-транс) изомерии.
Геометрические изомеры существуют в
дизамещенных циклоалканах. Для
хлорциклопентанола:
не является объектом рассмотрения
геометрической (цис-транс) изомерии.
Геометрические изомеры существуют в
дизамещенных циклоалканах. Для
хлорциклопентанола:
 транс
(OH, Cl) цис (OH, Cl)
транс
(OH, Cl) цис (OH, Cl)
Цис-транс изомерия является частным случаем Z,Eи ε, τ изомерии. Они отличаются только системой определения старшинства заместителей. Формально -Z(цис),E(транс); ε (цис), τ (транс). В общем случае при определенном изменении старшинства заместителей, для алкена заданной структуры существует ряд изомеров:

При R>R’>R’’>R’’’ соединение имеетε(Z)конфигурацию двойной связи.
При R>R’’’>R’’>R’ соединение является(Е)-изомером.
Система старшинства ε,τ-изомерии
Основана В.М. Потаповым и сотр. в 60-х гг. в МГУ. Суть системы - использованиеноменклатуры ИЮПАК.Например:

Главная цепь содержит 8 атомов углерода. Она расположена по разным сторонам плоскости -связи, поэтому данное соединение являетсяτизомером (понятие цис- транс- изомерии здесь неприемлемо!)
Система старшинства Z,E-изомерии

Система старшинства по Z,Eтипуоснована на периодической системе элементов Д.И. Менделеева.(по порядковому номеру элементов)

4-бромметил-2,5-диметилоктен-4 (Z)

I слой. Все заместители (атомы углерода) равны между собой
II слой.CH2Br>xилиy>CH3(порядковых номеровCH2Brравна: 6+2+35=43. ДляCH3– 6+3=9)
III слойi-Bu>н-Bu(т.к. дляi-Bu, по третьему слою: 6+6+1=13, для н-Bu: 6+1+1=8). Где:i-Buизобутил, н-Buн-бутил.
Таким образом, уменьшение старшинства заместителей имеет вид: CH2Br>i-Bu>н-Bu>CH3.Следовательно, рассматриваемое соединение является Z изомером.
Оптическая изомерия
Проявляется в тех случаях, когда изомеры одного и того же соединения, в свзи с различным расположением заместителей у определенного центра,не совместимы в пространстве. Для производных алифатического ряда изомерия связана со стереохимическими особенностямиsp3гибридного атома углерода.
Еще Ле-Бель в конце 18 века предположил тетраэдрическую структуру атома углерода. В том случае, если атом углерода соединен с четырьмя различнымизаместителями, появляется возможность существования 2-х изомеров, являющихся зеркальным отражением друг друга.
Атом углерода, имеющий все различные заместители называют асимметрическим илихиральнымцентром («хирос»рука).
Рассмотрим на примере перспективных формул:

Стереоизомеры IиIIне совместимы в пространстве, являются антиподами или оптическими изомерами (энантиомерами, стереомерами).
Проекционные формулы Фишера
Рассмотрим перспективные формулы в другой плоскости.
Расположим асимметрический центр (атом углерода) в плоскости листа; заместители aиbза плоскостью листа (отнаблюдателя); заместителиfиdнад плоскостью листа (ближекнаблюдателю) – в соответствии со стрелками, указывающими направление взгляда наблюдателя. Получим взаимно перпендикулярное направление связей с хиральным центром. Такое построение изомеров называют проекционными формулами Фишера.

Таким образом, в проекционных формулах Фишера заместители, расположенные по горизонтали, направлены к наблюдателю, по вертикали за плоскость листа.
При построении проекционных формул наиболее объемные заместители располагают по вертикали. Если заместителями являются атомы или малые группы, не имеющие отношения к главной цепи, то их располагают по горизонтали. Для 2-бромбутана

существуют два антипода:

Энантиомеры, антиподы, стереомеры практически неразличимы по свойствам (tкипения,tплавления и т.д.), а также имеют сходные термодинамические константы. В то же время у них есть различия:
- твердые антиподы кристаллизуются с образованием зеркально похожих друг на друга кристаллов, но не совместимых в пространстве.
- антиподы вращают плоскость поляризованного света на одинаковый угол, но в различные стороны. Если угол вращения света положителен (по часовой стрелке), то антипод называют правовращающим, если отрицателен (против часовой стрелки), то - левовращающим.
Угол оптического вращения плоскополяризованного света обозначают [αD]. Если [αD]= -31.2, то исследовался левовращающий антипод.
