
- •Органічна
- •Організаційно-методичні вказівки Мета викладання дисципліни
- •Задачі вивчення дисципліни
- •Взаємозв’язок дисципліни із іншими дисциплінами навчального плану
- •Особливості вивчення курсу органічної хімії. Методи роботи над навчальним матеріалом
- •Список літератури
- •Вуглеводні відкритої будови
- •Похідні вуглеводневих радикалів
- •Карбонові кислоти
- •Сполуки, що містять азот, сірку, фосфор та кремній
- •Гетерофункціональні похідні вуглеводнів та природні сполуки
- •Гетероциклічні сполуки
- •Завдання для контрольної роботи
- •Будова та номенклатура органічних сполук
- •Завдання для самостійного розв’язування
- •Вуглеводні відкритої будови. Алкани.
- •Завдання для самостійного розв’язування
- •3. Вуглеводні відкритої будови. Алкени.
- •Завдання для самостійного розв’язування.
- •Вуглеводні відкритої будови. Алкадієни.
- •Завдання для самостійного розв’язування
- •Вуглеводні відкритої будови.
- •Завдання для самостійного розв’язування.
- •Циклічні Вуглеводні. Неароматичні Вуглеводні
- •Завдання для самостійного розв’язування
- •Циклічні Вуглеводні. Ароматичні Вуглеводні
- •Завдання для самостійного розв’язування
- •Галогенохідні вуглеводневих радикалів
- •Завдання для самостійного розв’язування
- •9. Спирти
- •Завдання для самостійного розв’язування
- •10. Етери
- •Завдання для самостійного розв’язування
- •Органічна хімія
Завдання для самостійного розв’язування
Напишіть рівняння реакції та дайте назву сполукам, що утворяться в результаті
Бромування бензолсульфокислоти; нітрування п-нітро-толуолу;
Бромування хлорбензолу; нітрування о-дихлор-бензолу;
Бромування толуолу; нітрування о-хлортолуолу;
Бромування нітробензолу; нітрування п-нітротолуолу;
Нітрування фенолу; сульфування 2-нітрофенолу;
Сульфування бензойної кислоти; бромування м-хлортолуолу;
Нітрування бензолсульфокислоти; бромування о-нітро-толуолу;
Нітрування хлорбензолу; бромування м-хлортолуолу;
Сульфування нітробензолу; бромування о-нітро-хлорбензолу;
Сульфування фенолу; бромування м-нітрохлор-бензолу;
Нітрування бензойної кислоти; бромування п-нітро-хлорбензолу;
Сульфування хлористого бензилу; нітрування о-ксило-лу;
Сульфування кумолу; нітрування м-ксилолу;
Сульфування стиролу; нітрування п-ксилолу;
Нітрування хлористого бензилу; хлорування м-бром-хлорбензолу;
Бромування кумолу; сульфування м-нітрофенолу;
Хлорування стиролу; сульфування о-хлортолуолу;
Нітрування хлористого бензилу; сульфування м-нітроаніліну;
Нітрування кумолу; сульфування м-крезолу;
Нітрування стиролу; сульфування м-нітрохлорбензолу.
Галогенохідні вуглеводневих радикалів
Література: [1 с.281-308, 631-642] .
Приклад. Встановлено, що при хлоруванні алканів при температурі 20оС з урахуванням фактору ймовірності відносна швидкість заміщення атома водню змінюється в порядку:
третинний > вторинний> первинний і складає (на один атом водню) 5,0:3,8:1.
Використовуючи ці дані, передбачте вихід первинних, вторинних, третинних хлорпохідних і дайте назву усім ізомерам, що утворяться при монохлоруванні ізобутану.
Розв’язання. В алканів реакції хлорування проходять за радикальним механізмом, причому найлегше вони відбуваються біля найменш гідрогенізованого атому карбону. Це пояснюється тим, що міцність зв’язку С-Н біля такого атому найменша, а стабільність радикала, що утворюється – найбільша.
Для
розрахунку виходу різних галогенпохідних
використовують такі формули:![]()
![]()
![]()
де В1, В2, В3 – вихід моногалогенпохідних з галогеном відповідно біля первинного, вторинного і третинного атомів карбону; а,в,с – кількість атомів гідрогену відповідно біля первинних, вторинних і третинних атомів; С1, С2, С3 – відносна швидкість заміщення водню на галоген відповідно біля первинного, вторинного і третинного атомів.
Таким чином, для того щоб знайти вихід кожної галогенпохідної необхідно визначити кількість атомів гідрогену біля кожного типу атомів карбону.
I III II II I
В молекулі ізогексану: СН3 – СН – СН2 – СН2 – СН3
│I
СН3
три первинних, два вторинних і один третинний атом карбону. Біля кожного первинного атому карбону знаходиться по три атоми гідрогену, тому загальна кількість атомів гідрогену біля первинних атомів карбону: а =3 х 3 = 9 атомів. Біля кожного вторинного – по два атоми гідрогену: в = 2 х 2 = 4. Біля третинного – один атом гідрогену: с = 1 х 1 = 1.
Підставивши ці значення в наведені вище формули отримаємо:
![]()
![]()
![]()
Вихід первинних монохлорпохідних – 30,8 %; вторинних – 52,1%; третинних – 17,1 %.
В процесі монохлорування ізопентану утворюється три ізомери первинних монохлорпохідних (заміщення гідрогену на хлор відбувається біля кожного з трьох первинних атомів карбону):
1) 2) 3)
СН2 – СН – СН2 – СН2 – СН3 СН3 – СН – СН2 – СН2 – СН3 СН2 – СН – СН2 – СН2 – СН2
│ │ │ │ │
Cl СН3 Cl – СН2 СН3 Cl
причому ізомер (1) ідентичний ізомеру (2) – це 2-метил-1-хлорпентан. Ізомер (3) має назву 2-метил-5-хлорпентан. Виходячи з того, що 2-метил-1-хлорпентан утворюється біля двох атомів карбону, вихід його буде в двічі більший, ніж 2-метил-5-хлорпентану. Тому з 30,8% продуктів реакції, що приходяться на первинні галогенпохідні 2/3 – 2-метил-1-хлорпентан і 1/3 – 2-метил-5-хлорпентан.
В молекулі ізогексану 2 вторинних атоми карбону, тому утворюється 2 ізомери вторинних монохлорпохідних:
1) 2)
СН3 – СН – СН – СН2 – СН3 СН3 – СН – СН2 – СН – СН3
│ │ │ │
СН3 Cl СН3 Cl
2-метил-3-хлорпентан 2-метил-4-хлрпентан
ймовірність утворення цих ізомерів однакова, тому з 52,1% продуктів половина – 2-метил-3-хлорпентан; половина – 2-метил-4-хлорпентан.
Біля одного третинного атому карбону утворюється одна третинна монохлорпохідна: Cl
│
СН3 – С – СН – СН2 – СН3
│
СН3
2-метил-2-хлорпентан
і її вихід складає 17,1%.
Таким чином в процесі монохлорування ізогексану утворюється 5 ізомерів:
2-метил-1-хлорпентан; вихід =
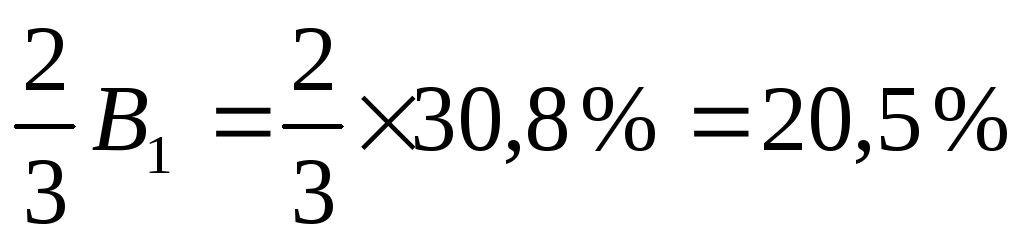
2-метил-5-хлорпентан; вихід =

2-метил-3-хлорпентан; вихід =
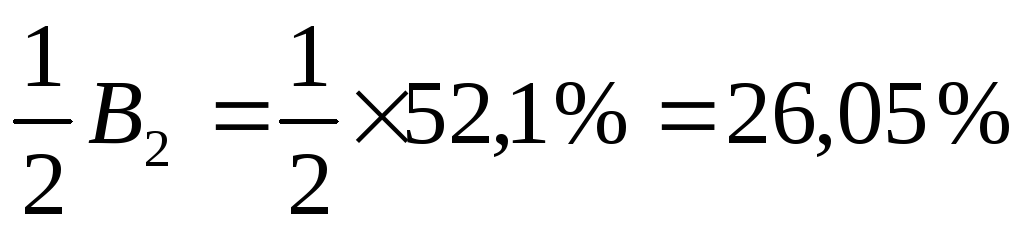
2-метил-4-хлорпентан; вихід =

2-метил-2-хлорпентан; вихід =

