
- •Глава 9. Улавливание химических продуктов коксования
- •9.3. Очистка коксового газа от аммиака
- •9.3.1. Технология производства сульфата аммония
- •9.3.2. Другие способы улавливания и утилизации аммиака
- •9.4. Улавливание пиридиновых оснований
- •9.5. Очистка коксового газа от сероводорода и цианистого водорода
- •9.6. Улавливание бензольных углеводородов
9.5. Очистка коксового газа от сероводорода и цианистого водорода
Этот участок отделения обработки коксового газа обеспечивает получение удовлетворяющего требованиям качества коксового газа, надежную и устойчивую работу всех цехов коксохимического предприятия, решение экологических проблем.
По существующим нормам коксовый газ, используемый в качестве технологического топлива для печей металлургических цехов, должен содержать не более 2 г сероводорода на 1 Нм3 газа; газа для бытовых целей не более 0.02 г/Нм3; газа для нужд синтетических производств не более 0.001 г/Нм3. На заводах Украины, где содержание H2S в газе 18-20 г/Нм3, сероочистные цехи работают с 40-х годов. На заводах России, где в коксующихся углях мало серы, содержание сероводорода в газе невелико и составляет 1 - 3 г/Нм3, сероочисток нет. Построенную на Кемеровском заводе сероочистку сочли целесообразным остановить, так как количество выбрасываемого при сжигании газа этого завода диоксида серы составляет всего 1.0 - 1.5% об. от выбросов этого соединения другими предприятиями промузла.
Содержание HCN в коксовом газе жестко не нормируется. В прямом коксовом газе его содержится около 1 - 3 г/Нм3 в зависимости от содержания азота в коксуемых углях и режима пиролиза химических продуктов коксования в подсводовом пространстве. В обычных условиях цианистый водород выводится из газа по технологическому тракту и содержание его в обратном коксовом газе невелико. Так, на заводах Украины с открытым циклом конечного охлаждения и сероочисткой после бензольного цеха содержание HCN по газовому тракту изменяется следующим образом, г/Нм3: перед первичными холодильниками - 2.4; после первичных холодильников - 2.3; перед сатуратором - 2.2; после сатуратора - 2.05; перед конечными холодильниками - 1.94; после конечных холодильников - 0.9; после сероочистки - 0.15.
Традиционные технические решения конечного охлаждения коксового газа в холодильниках непосредственного действия с охлаждением воды на градирне хотя и позволяли удалять из газа значительную часть цианистого водорода, но одновременно приводили к выбросам в атмосферу значительных количеств этого токсичного вещества (50 - 60 кг/ч для предприятия производительностью 1 млн. т кокса в год). Закрытие цикла конечного холодильника избавляет от этих выбросов, но вызывает накопление тиоцианатов и цианидов в образующемся конденсате и увеличивает концентрацию HCN в газе. К тому же присутствие в газе сероводорода и цианистого водорода приводит к усилению коррозии во всех отделениях коксохимического завода.
Круговые методы очистки коксового газа
Особенностью этих методов является поглощение сероводорода растворами слабых оснований (константа диссоциации 10-6 -"- 10-5) или солями сильных оснований и слабых кислот в аб-сорбционно-десорбционном процессе.
В связи с тем, что в коксовом газе одновременно присутствуют сероводород, цианистый водород и диоксид углерода, содержание которого в несколько раз больше, чем содержание сероводорода, очистка газа происходит в наиболее неблагоприятных условиях. Это, во-первых, возможность одновременного поглощения цианистого водорода и образования в растворе тиоцианатов; во-вторых, возможность необратимого связывания части оснований в соответствующие тио-цианаты, в-третьих, необходимость обеспечения селективного улавливания сероводорода. Присутствие в коксовом газе цианистого водорода - главная причина того, что в качестве поглотителя редко используют растворы органических оснований.
Наиболее распространенным способом круговой сероочистки является вакуум-карбонатная, используемая на большинстве заводов Украины.
Процесс следующий:
H2S + M2CО3 = MHS + МНСОз;

Термодинамически возможен и процесс Н2О+ СО2 + MHS = MHCO3 + H2S.
Абсорбцию осуществляют растворами соды или поташа, или смеси этих солей. Для того, чтобы обеспечить селективное поглощение сероводорода, регенерацию проводят при температуре 65 - 75°С (остаточное давление в верхней части регенератора 14.5 - 15 кПа). При этом из раствора выделяется преимущественно сероводород и регенерированный раствор селективно сорбирует также этот газ.
Концентрация соли подбирается таким образом, чтобы исключить выпадение из растворов кристаллов бикарбонатов. Большая концентрация растворов и, значит, большая сероемкость теоретически могут быть достигнуты при улавливании растворами поташа. Ниже приведены растворимости кислых и средних карбонатов натрия и калия, г/100 см' воды:

Таким образом, при вакуум-поташной сероочистке можно использовать более концентрированные растворы поглотителя, следовательно работать при большей сероемкости раствора и, значит, при меньшем расходе энергии на перекачку и нагревание растворов. Рекомендуемые концентрации растворов должны быть не более 5 % масс. при улавливании растворами соды и не более 15 % масс. при улавливании растворами поташа. Из-за высокой стоимости и дефицитности поташа обычно используют растворы смеси соды и поташа.
В растворе накапливаются и нерегенерируемые соли, образующиеся в результате окисления гидросульфида аммония, образования продуктов взаимодействия компонентов раствора с цианистым водородом, а также при омылении цианистого водорода. Как правило, эти процессы более интенсивно идут в случае использования поташа.
Протекающие при этом процессы следующие:
2HS- + 2О2 = S2О32- + Н2О;
4HS-+О2 = 2Н2О + 4S;
CN-+ S = CNS-;
6CN- + Fe2+ = [Fe(CN)6]4-;
HCN+ 2Н2О = NH3+ HCOOH = HCOONH4;
2HCOONH4 + К2СО3 = 2НСООК + 2NH3 + СО2 + Н2О.
Нерегенерируемые соли накапливаются в растворе, что требует выведения из цикла части раствора (при нормальной эксплуатации около 0.2 м3 /т уловленного сероводорода).
Поэтому приходится, во-первых, расходовать определенные количества соды и поташа для компенсации потерь натрия и калия, связанных в нерегенерируемые соли, во-вторых, поддерживать в рабочем растворе высокую концентрацию нерегенерируемых солей, в-третьих, по этой причине работать с растворами, обладающими высокой вязкостью, что увеличивает расходы на их перекачку и нагревание. Наконец, приходится считаться и с тем, что нерегенерируемые соли могут создать опасность отложения осадков, например, гексацианоферрата калия в трубопроводах, насосах и арматуре и увеличить опасность коррозии оборудования. Возникает необходимость утилизации сточных вод и утилизации нерегенерируемых солей. Этот вопрос рассматривается в последней главе. В табл. 9.8 приводятся сравнительные данные о показателях работы установок вакуум-но-карбонатной сероочистки.
Высокая концентрация балластных солей создает и определенные трудности, связанные с увеличением высаливающего действия, что увеличивает в 4 - 5 раз упругость паров сероводорода над регенерированным раствором и тем самым уменьшает полноту улавливания.Значительный расход поташа, который в несколько раз дороже соды, снижение надежности установок из-за выпадения кристаллов К4Fe(CN)6 при незначительном выигрыше от использования поташа по энергетике привело к применению очистки содопоташным раствором (1:1), показатели использования которого близки к данным табл. 9.8 при использовании поташа.
Расход пара на очистку может быть сокращен на 15 - 20% масс. и более при использовании для подогрева раствора тепла коксового газа, отводимого в первичных газовых холодильниках. В этом случае необходимо на 10 град уменьшить температуру после циркуляционных подогревателей регенераторов (с 80 - 83 до 70 - 73°С).
Таблица 9.8. Показатели вакуум - карбонатной сероочистки (концентрация H2S 18-20 г/Нм3 газа)

На большинстве заводов Украины вакуум-карбонатная сероочистка размещена после улавливания бензольных углеводородов, что позволяет избавиться от очистки газа от нафталина, но создает серьезные трудности при эксплуатации бензольного цеха.
В зарубежной практике применяют двухступенчатую очистку коксового газа от сероводорода в вакуум-карбонатном процессе. В нашей стране накоплен опыт доочистки под давлением. В обоих случаях содержание сероводорода может быть уменьшено до 0.01 - 0.2 г/дм . При этом на 80% увеличиваются капитальные затраты и суммарные энергозатраты. Расход реактивов возрастает на 25 - 35% масс.
В процессе вакуум-карбонатной сероочистки улавливается, в зависимости от плотности орошения и содержания сероводорода в газе от 40 - 60 до 90 % об. цианистого водорода. На отечественных установках поглощение сероводорода проводится преимущественно в аппаратах с деревянной хордовой насадкой. В связи с тем, что скорость абсорбции сероводорода значительно больше, чем для диоксида углерода, оправдано применение аппаратов с малым временем контакта между газом и жидкостью, с провальными или пластинчатыми тарелками. Это позволит получить при регенерации более концентрированный сероводородный газ.
В мировой коксохимической промышленности наиболее распространена из круговых методов аммиачная сероочистка, условиями эффективного использования аммиачной сероочистки, которая, судя по опыту промышленности Германии, в два раза экономичнее вакуум-карбонатной сероочистки, является улавливание сероводорода до улавливания аммиака, применение аммиачной воды с концентрацией, близкой к равновесной между аммиаком в газе и воде (при 25 - 30 °С - около 1,5 % масс.) и, самое главное, применение аппаратов с малым временем контакта между газом и жидкостью. Последнее является решающим условием селективного поглощения сероводорода из газа, так как по условиям равновесия аммиачная вода должна была бы преимущественно улавливать диоксид углерода, что многократно увеличило бы расход тепла на регенерацию и подогрев раствора. Только при малом времени контакта удается использовать то обстоятельство, что скорость поглощения сероводорода в 45 - 85 раз больше скорости поглощения диоксида углерода.
Аммиачная сероочистка используется в ряде вариантов. Применяют абсорберы различных типов: форсуночные, с провальными тарелками и двухступенчатыми пластинчатыми тарелками, включая их вариант, так называемый "скруббер Киттеля". Различной может быть эффективность аммиачной сероочистки в зависимости от того, каким способом осуществляется последующее улавливание аммиака. Эффективное улавливание достигается при соотношении аммиак/сероводород равном 2 в растворе после улавливания. При концентрации, отвечающей равновесной при 25 - 28 °С (около 15 г NH3 на 1 дм3), сероемкость составляет 6 - 7.5 г/дм3. При этом полнота улавливания около 75 - 85 % масс. Увеличение избытка аммиака или концентрации аммиачной воды позволяет повысить полноту извлечения аммиака до 98 % масс. и более. Однако увеличение концентрации аммиака свыше 2 % масс. приводит к десорбции аммиака в газ и, следовательно, для соблюдения баланса по аммиаку, становится необходимым доулавливание аммиака из газа и возвращение его в цикл. Такое решение технически нерационально при улавливании аммиака серной кислотой и получении сульфата аммония (возникает необходимость установки дополнительного абсорбера для поглощения аммиака водой и дополнительной системы отгонки аммиака из этой воды, что значительно увеличивает затраты на сероочистку).
В то же время улавливание сероводорода аммиачной водой повышенных концентраций идеально совмещается с поглощением аммиака в круговом аммонийно-фосфатном процессе. Принципиальная технологическая схема такого совмещенного процесса представлена на рис. 9.11.
В практике промышленных предприятий ФРГ, США, Великобритании и ряда других стран используются различные варианты сероочистки аммиачной водой.
Аммиачная сероочистка имеет особенности, которые серьезно влияют на проектирование и эксплуатацию установок. В зависимости от принятых концентраций аммиачной воды и используемого избытка аммиака полнота улавливания HCN может колебаться от 20 - 30 до 85-95% масс. Образование нерегенерируемых солей происходит в значительно меньшей степени, чем при вакуум-карбонатной очистке. Образующиеся сточные воды, содержащие тиосульфат и тиоцианат аммония, могут быть переработаны по обычной технологии вместе с надсмольной водой с выделением аммиака.
Аммиачная сероочистка (или сероцианоочистка) размещается до улавливания аммиака и бензола, поэтому очистке от сероводорода должна предшествовать очистка от паров и аэрозолей нафталина.
Освоена абсорбционная очистка газа от нафталина. Она осуществляется поглотительным (предпочтительно - соляровым) маслом по обычной абсорбционно-десорбционной схеме. При этом остаточная концентрация нафталина в газе может составлять 0.027 г/Нм3. Аммиачная сероочистка предполагает охлаждение газа перед очисткой до 20 - 25°С. Это означает необходимость более жесткого соблюдения норм ПТЭ и лучшего охлаждения газа. При вакуум-карбонатной сероочистке можно работать и при 40 - 45°С. Наконец, при аммиачной сероочистке возможна аммонийно-цианидная коррозия, что требует использования регенераторов, изготовленных из устойчивых к ней материалов, таких как чугун, сплавы алюминия и титана.

Рис. 9.11. Принципиальная технологическая схема совмещенных аммиачной сероцианоочистки и улавливания аммиака:
1 - сероводородный абсорбер; 2 - аммиачный абсорбер; 3 - теплообменник; 4 - подогреватель; 5 -холодильник; 6, 7, 8, 9, -насосы; 10 - сероводородная колонна; 11 - блок переработки раствора ди-аммонийфосфата с получением безводного аммиака; а -аммиачная вода б - аммиачная вода, насыщенная сероводородом; в - раствор моноаммонийфосфата; г - раствор диаммонийфосфата; д -концентрированная аммиачная вода; е - безводный аммиак; ж - концентрированный сероводородный газ с примесью цианистого водорода на сжигание; з - очищенный газ.
Переработка сероводородного газа
При регенерации насыщенных растворов круговых методов сероочистки выделяется сероводородный газ, содержащий 80 - 90% об. сероводорода. Примесями являются диоксид углерода и цианистый водород (до 3 - 5% об.). В случае аммиачной сероцианоочистки бедных по сероводороду газов в газах регенерации содержится до 40% об. цианистого водорода. Переработка сероводородного газа возможна в двух вариантах: с получением серной кислоты и элементной серы. На коксохимических заводах, имеющих вакуум-карбонатные сероочистки, применяют только переработку в серную кислоту, чтобы использовать ее для удовлетворения нужд коксохимического завода (очистка бензола, производство сульфата аммония).
При использовании этой технологии, принципиально подобной получению серной кислоты контактным методом, приходится решать несколько специфических задач:
1. Окисляют сероводород, содержащий примеси цианистого водорода. Последний может окислиться либо в оксиды азота
4HCN + 7О2 = 2Н2О + 4СО2 + 4NO,
либо в элементный азот
4HCN + 5О2 = 2Н2О + 4СО2 + 2N2.
Для того чтобы не образовывались оксиды азота, окисление (сжигание) сероводорода проводят в две ступени в специальной печи. На первой стадии при недостатке воздуха частично окисляется сероводород, а цианистый водород окисляется до азота, затем происходит введение дополнительного количества воздуха и дожит сероводорода и частично образовавшейся серы до диоксида серы.
2. Другая трудность связана с тем, что обычные катализаторы контактного производства серной кислоты снижают активность в присутствии паров воды. Обычно технологические схемы сернокислотных производств включают узел осушки газа перед контактированием. При сжигании сероводорода неизбежно образование смеси диоксида серы и водяного пара, поэтому возникла необходимость подбора катализатора, устойчивого в присутствии водяных паров. В связи с этим и процесс приготовления серной кислоты из сероводорода получил жаргонное наименование "мокрый катализ".
Катализатором чаще всего служит ванадиевая контактная масса БАВ: V2О5 • 12SiО2 • 0,5А12О3 • 2Н2О • ЗВаО • 2КС1.
3. Наконец, особенностью "мокрого катализа" является получение после контактного аппарата в паровой фазе смеси серного ангидрида и водяного пара. При охлаждении газовой смеси конденсируется серная кислота в виде мелкодисперсного тумана. При охлаждении через стенку или при смешении с холодным воздухом в туман переходит все количество образующейся кислоты. Возможным и реализованным решением оказалось охлаждение газов циркулирующей серной кислотой. Образующаяся при конденсации кислота растворяется в циркулирующем продукте (преимущественно). Правда, и в этих условиях вместе с газом выносится 30-35% масс. кислоты в виде тумана, который улавливается в электрофильтре.
Показатели установок мокрого катализа следующие:

Отличительная особенность кислоты "мокрого катализа" (при соблюдении норм сжигания сероводородного газа, исключающих образование оксидов азота) - высокая чистота, отсутствие примесей посторонних элементов - в отличие от кислоты, получаемой из природной серы и тем более серного колчедана и отбросных газов цветной металлургии.
Высокое качество получаемой серной кислоты делает перспективным использование метода "мокрого катализа" при переходе в химических цехах коксохимических предприятий на методы улавливания и переработки, не связанные с использованием серной кислоты (гидроочистка бензольных углеводородов и нафталина, производство безводного аммиака), так как из-за отсутствия примесей она может быть поставлена самым требовательным потребителям.
Другим направлением в коксохимической промышленности может быть окисление (каталитическое) сероводородного газа до элементной серы. Суть метода в частичном окислении сероводородного газа в условиях, когда примерно 1/3 сероводорода окисляется до оксида серы, а цианистый водород и аммиак - до азота, с последующей обработкой продуктов сгорания на боксите при 270 - 300 °С. При этом непрореагировавший сероводород окисляется диоксидом серы до элементной серы. Сера конденсируется в нижней части аппарата при охлаждении испаряющейся водой. Несконденсированная сера в ряде схем поглощается в скрубберах при промывке газов жидкой серой при 130 - 140 °С. Действующие установки, широко применяемые в отечественной газовой промышленности при окислении сероводорода, извлеченного из природного газа (Оренбургское и Астраханское месторождения), обеспечивают превращение в серу 90 - 98% масс. переданного на переработку сероводорода. В технической литературе способ получения серы из сероводорода на катализаторе называют методом Клауса.
Окислительные методы сероочистки
Общим из этих методов является регенерация насыщенных растворов при продувке кислородом воздуха с восстановлением поглотительной способности раствора и получением элементной серы. Из окислительных методов на коксохимических предприятиях использовалась сероочистка. Принципиальная схема основного блока окислительной сероочистки представлена на рис. 9.12.
Исходными веществами для приготовления поглотительного раствора служат карбонат натрия и оксид мышьяка (III), рН раствора поддерживается в пределах 7.65 - 7.9.
Основные реакции следующие:
поглощение сероводорода:
Na4As2S5О2 + H2S = Na4As2S6О+ H20;
регенерация поглотителя:
2Na4As2S6О + О2 = 2Na4As2S5О2 + 2S.
Абсорбция осуществляется при 40 - 45°С. При этом соотношение As2О3/H2S в растворе поддерживается в пределах 15 - 17, то есть почти в три раза превышает стехиометрическое

Рис. 9.12. Принципиальная технологическая схема окислительной очистки коксового газа от сероводорода:
1 - абсорбер; 2 - регенератор; 3 - вакуум-фильтр; 4 - плавильник; 5 - сборник регенерированного поглотительного раствора; 6, 7 - насосы; 8 - компрессор; а - регенерированный поглотительный раствор; б - насыщенный раствор после улавливания сероводорода; в - серная пена; г - серная паста; д- жидкая чистая сера; е - сжатый воздух.
значение 5.82. В регенераторе раствор и воздух подаются снизу параллельным током. Образующаяся при регенерации мелкодисперсная сера флотируется в восходящем потоке воздуха и отделяется в верхней части регенератора в виде серной пены (10 % масс. твердой фазы). На отдельных предприятиях серная паста репульпируется, промывается чистой водой и поставляется после сушки в виде мелкодисперсной коллоидной серы для сельского хозяйства. На большинстве предприятий серная пена отделяется от большей части оставшегося раствора на вакуум-фильтрах. Далее полученную серную пасту плавят под давлением, отделяя расплавленную серу от раствора и направляя ее поставщикам либо в жидком виде, либо получая чешуированную серу после охлаждения на барабане.
В одноступенчатом процессе сероводород и цианистый водород извлекаются из газа на 90 -95 % масс. В случае применения второго блока улавливания (отношение AS2O3/H2S на второй ступени поддерживается около 30) достигается практически полное удаление обоих веществ из газа (остаточное содержание менее 0.05 г/Нм3).
Характерным для мышьяково-щелочного метода, как и для других окислительных методов сероочистки, является образование больших количеств нерегенерированных балластных солей на стадии регенерации раствора.
Ионы HS- , образование которых является обязательной стадией поглощения сероводорода, окисляются с образованием тиосульфат-иона 2HS- + 2O2 = S2O3 2- + Н2О. При взаимодействии серы с ионами CN-, находящимися в растворе, образуются тиоцианат-ионы. В тиоцианат переходит весь уловленный цианистый водород.
Тиоцианат и тиосульфат натрия связывают значительную долю соды и образующейся при регенерации серы и накапливаются в растворе. Балластные соли накапливаются в растворе (предельно допустимое содержание до 350 г/дм3). Для удаления балластных солей часть раствора выводится из цикла. Переработка отводимых стоков должна, в первую очередь, гарантировать освобождение раствора от мышьяка. С этой целью раствор нейтрализуют серной кислотой, чтобы перевести мышьяк в нерастворимые сульфиды
Na4As2S6О + 2H2SО4 = 2Na2SО4 + As2S5 + H2S + H2О.
Часть сульфида мышьяка (V) превращается по реакции As2S5 = As2S3 + 2S.
Осадок отфильтровывается, растворяется в содовом растворе и вновь возвращается в цикл. В фильтрате содержится до 0.05 г мышьяка на 1 дм3 в виде растворимого Na2HAsО4. Он дополнительно обезвреживается обработкой раствором FeSО4 и соды с тем, чтобы перевести мышьяк в малорастворимые FeAsO3 и FeAsО4. Шлам после фильтрации сбрасывают в отвал, а раствор направляют на переработку. Пути переработки растворов после удаления мышьяка рассматриваются в разделе, посвященном экологическим проблемам коксохимической промышленности.
Мышьяково-щелочная сероцианоочистка требует от персонала повышенного внимания к соблюдению технологического режима и, прежде всего, к поддержанию рН в заданных пределах. Так, рН раствора после регенерации стремятся поддерживать в пределах 7.8 - 7.9 (рН раствора перед регенерацией не менее 7.65). Уменьшение рН ниже заданного предела вызывает выпадение осадков сульфидов мышьяка; увеличение рН значительно увеличивает долю гидросульфид-иона, переходящего в тиосульфат-ион. Выделение некоторого количества сульфидов наблюдается и при повышении температуры раствора выше 60 - 70°С. Регенерация раствора улучшается в присутствии примесей органических веществ, выступающих в качестве катализаторов этого процесса. При этом возникает опасность "перерегенерации"- образования полиоксисульфосолей, неспособных к поглощению сероводорода. Поэтому мышьяково-щелочную сероочистку всегда размещают после улавливания бензольных углеводородов, перед ней обычно устанавливают электрофильтры для удаления аэрозолей поглотительного масла.
Малая стабильность сульфомышьяковых солей приводит к появлению некоторых дополнительных операций. Так, например, при нагревании в плавильнике влажной серной пасты (до 130 -135°С) из раствора выпадает некоторое количество сульфидов мышьяка. Поэтому в автоклав-плавильник добавляют до 2 - 3% от массы серы карбоната натрия. Расходные показатели при одноступенчатой очистке в расчете на 1 т товарной серы при нормальной эксплуатации следующие:
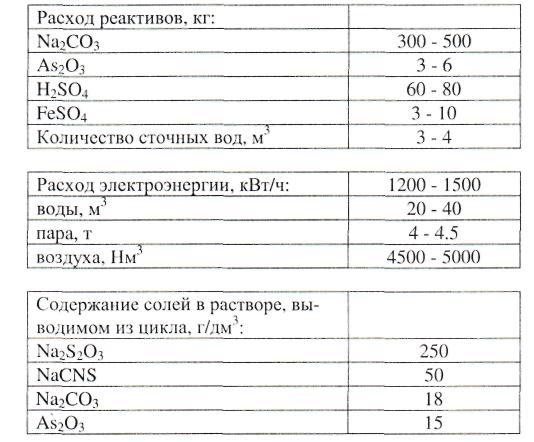
Мышьяковая сероочистка характеризуется невысокой сероемкостью раствора (0.8 - 1.0 г Н2S/дм3) и очень значительным расходом реактивов. Товарным продуктом является сера, содержащая 99.86% масс. основного вещества и не более 0.006% масс. мышьяка.
За рубежом в последние десятилетия вместо мышьяковой сероочистки широко используют различные окислительные методы очистки, получившие в отечественной технической литературе наименование "хинонных".
Общей чертой всех хинонных методов сероочистки (сероцианоочистки) является размещение сероцианоочистки в голове технологического процесса - до улавливания аммиака и использование в качестве абсорбента аммиачной воды (10 - 15 г аммиака на 1 дм"), содержащей 0.2 - 0.3 г катализатора на I дм" раствора. В качестве катализаторов используют различные окислительно-восстановительные системы, используемые как переносчики электронов при окислении S2- в элементную серу. Используемые на предприятиях Великобритании и Японии (преимущественно), а также упоминаемые в литературе хинонные методы очистки носят разнообразные фирменные наименования и отличаются только природой применяемых катализаторов: "Перокс" - гидрохинон; "Стретфорд" - антрахинондисульфокислота и ванадат натрия; "Фумакс-Родакс" - пикриновая кислота; "Такахакс" - 2-сульфокислота 1.4-нафтохинона и др.
Абсорбцию и регенерацию осуществляют при 20 - 22 °С, как правило, работают при очень больших плотностях орошения (до 4 м3 циркулирующего раствора на 1 кг поглощаемого сероводорода) и малых сероемкостях (0.05 - 1.00г сероводорода на 1 дм"). Полнота улавливания сероводорода 99.99 % масс, а цианистого водорода 97 - 100 % масс. Последний полностью обращается в тиоцианат аммония, а сероводород на 75 - 76 % масс. - в элементную серу, на 15 - 20 % масс. в тиоцианат аммония и на 5 - 7 % масс. - в тиосульфат аммония.
Хинонные методы мало чувствительны к примесям органических веществ в газе, хотя и предполагают обязательную предварительную очистку газа от аэрозольного нафталина. Метод не связан с расходованием больших количеств реактивов; удаление сероводорода и цианистого водорода обеспечивается в начале технологического процесса. Общее количество сточных вод составляет 1 - 2 м3/т серы. Полученные сточные воды могут перерабатываться различными путями. Так, возможна выпарка их с последующим термическим разложением и получением при этом смеси аммиака и сероводорода или сжигание при 1100 °С (по схеме Фумакс-Родакс-Компакс) с получением диоксида серы, направляемого на производство серной кислоты.
Технологические приемы улавливания и утилизации цианистого водорода
В основном, это методы улавливания цианистого водорода с получением тиоцианата аммония и тиоцианата натрия. Тиоцианат аммония представляет интерес как сырье для изготовления тиомочевины и ряда ее производных, используемых в качестве пестицидов. Тиоцианат натрия представляет интерес как среда, в расплаве которой изготавливают волокна "нитрон". Заметим, что мощности по производству тиоцианата натрия в настоящее время превышают потребность химической промышленности в тиоцианате натрия.
Общей чертой технологий является предварительное приготовление раствора полисульфидов аммония или натрия и абсорбция цианистого водорода растворами полисульфидов. Получаемый раствор подвергается специальной переработке и очистке. Из подготовленного к дальнейшей переработке раствора путем вакуум-выпарки и кристаллизации получают кристаллические тиоцианаты.
Рассмотрим основные принципы получения тиоцианата натрия. Исходный рабочий раствор полисульфида натрия готовится при насыщении раствора сульфида натрия серой. Затем раствор полисульфидов натрия, обладающий щелочностью (в расчете на карбонат натрия) 15 - 20 г/дм3, направляется на очистку газа от цианистого водорода в специальном скруббере. Часть циркулирующего раствора постоянно отводится из цикла и направляется на перемешивание с серой в специальном реакторе. Раствор после перемешивания и насыщения серой возвращается в цикл.
Естественно, что при поглощении цианистого водорода улавливаются и другие компоненты коксового газа. Оказывается возможным прохождение побочных процессов, характерных для окислительной сероочистки. При 35 - 40°С, удельной плотности орошения 2.5 - 3.0 дм3 раствора полисульфидов на 1 м3 газа и линейной скорости газа около 1 м/с достигается улавливание HCN из газа на 85 - 90% масс. при содержании тиоцианата натрия в растворе 350 - 400 г/дм3. В растворе содержатся также, г/дм3: тиосульфат натрия - 50; карбонат натрия - 20; сульфат натрия - 20; гидросульфид натрия - 4.
На действующих установках с целью упрощения солевого состава раствора последний при кипячении обрабатывается серной кислотой, что позволяет добиться полного разложения тиосульфата натрия. Кислые газы сорбируются раствором соли в абсорбере, а раствор направляется на улавливание HCN.
Полученный раствор нейтрализуется до рН 7 - 8. Далее, при упарке и кристаллизации из раствора выделяют сульфат натрия и серу. Затем гидроксидом бария и сульфидом натрия из раствора осаждают и удаляют примеси сульфат-иона, ионов железа и тяжелых металлов, активированным углем адсорбцией удаляют органические примеси. После удаления осадков фильтрат упаривается, при охлаждении выделяют кристаллы чистого двуводного кристаллогидрата тиоцианата натрия с выходом (с учетом повторной переработки маточных растворов) 70 - 80% масс. от ресурсов в исходном растворе.
Представление о расходах реактивов на производство тиоцианата натрия дают следующие показатели:
Стадия улавливания, т на 1 т извлеченного тиоцината натрия:
100% - ный едкий натр 1.8;
100% - ная сера 1.6.
Стадия очистки, кг/т чистого двуводного тиоцианата:
серная кислота 93;
едкий натр 1.2;
гидроксид бария 4.8;
сульфид натрия 4.0;
активированный уголь 35.0.
