
- •Міністерство освіти і науки України
- •Загальні методичні вказівки
- •Рішення:
- •Рішення:
- •Рішення:
- •Тема для самостійного вивчення:
- •Задачі для самостійного розв’язання студентами
- •Відповіді до задач
- •Приклад розв’язання задач:
- •Рішення
- •Теплова машина. Цикл Карно
- •Рішення:
- •Рішення:
- •Рішення:
- •Рішення:
- •Тема для самостійного вивчення:
- •Друге начало термодинаміки. Ентропія
- •Рішення.
- •Рішення:
- •Рішення:
- •Рішення:
- •Рішення:
- •Тема для самостійного вивчення:
- •Неідеальний газ. Флуктуації.
- •Рішення:
- •Рішення:
- •Тема для самостійного вивчення:
- •Тема для самостійного вивчення:
- •Елементи фізичної кінетики. Нерівноважна тд
Рішення:
Робота, зроблена проти сил взаємодії молекул,

Таким чином,

звідки виразимо
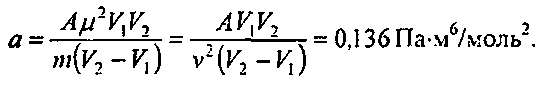
Список літератури, що використовується для підготовки до практичної роботи:
|
1 |
А.М. Федорченко Теоретична фізика: Квантова механіка, термодинаміка і статистична фізика. Т.2.-К.:Вища школа, 1993. - 451 с. |
|
2 |
Л.Д. Ландау, Е.М.Лифшиц Теоретическая физика.Т.5. Статистическая физика .-М.: Наука, 1976. – 584 с. |
|
3 |
І.М.Кучерук Загальний курс фізики. Т.1. механіка. Молекулярна фізика і термодинаміка.-К. : Техніка, 1999. – 536 с. |
|
4 |
Д.В.Сивухин Термодинамика и молекулярная физика.- М.: Наука,1990. – 592 с. |
|
5 |
А.Н. Матвеев Молекулярная физика. – М.: Высшая школа, 1987. – 360 с. |
|
6 |
Г.Ф. Бушок, Є.Ф.Венгер Курс фізики. Т.1. Фізичні основи механіки. Молекулярна фізика і термодинаміка. -К.: Вища школа, 2002. – 375 с. |
Тема для самостійного вивчення:
Неідеальний газ. Критичні параметри.
Основні вимоги до знань та умінь студентів
Знати :
відхилення газів від ідеальності,
інтерполяційне рівняння стану реального газу – рівняння Ван-дер-Ваальса,
параметри критичного стану речовини
Рекомендована література :
|
|
|
|
|
|
|
Питання для самоконтролю :
Хто із перших проаналізував відхилення поведінки реальних газів від законів ідеального газу?
Для чого необхідна інтерполяційна формула?
Наведіть інтерполяційне рівняння стану реального газу.
Параметри критичного стану речовини виражаються через….?
У критичному стані відбувається зменшення структурних одиниць чи ні?
Чим необхідно користуватися при аналізі явищ поблизу критичного стану?
Наведіть формули постійних Ван-дер-Ваальса.
Задача для самостійної роботи:
Обчислити постійні Ван-дер-Ваальса для водню, якщо відомо, що його критична температура Ткр = 33,2 К, критичний тиск Ркр= 1,295 МПа й молярний обсяг у критичному стані Vm кр = 6,5 * 10 -5 м3/моль.
