Лекция 12(поверхностные явления)
.docЛ12 ФИЗИКО-ХИМИЯ ПОВЕРХНОСТНЫХ ЯВЛЕНИЙ.
Живые организмы – системы с очень развитыми поверхностями раздела. К ним относят кожные покровы, поверхность стенок кровеносных сосудов, слизистые оболочки, клеточные мембраны.
Поверхность кожи взрослого человека составляет 3 м2, площадь поверхности всех эритроцитов – 2500 м2, площадь альвеол лёгкого – 1000 м2. Известно, что многие жизненно важные процессы в организме протекают на поверхностях фаз, следовательно, для их понимания надо знать основные закономерности, которым подчиняются поверхностные явления.
Поверхностные явления – совокупность явлений связанных с особенностями поверхностей раздела, т.е. поверхностных слоёв между соприкасающимися фазами (поверхностное натяжение, адсорбция).
Поверхностные явления связаны с тем, что состояние молекул вещества, расположенных на границе раздела двух фаз отличается от состояния молекул в объёме фаз.
газ











 равнодействующая сила
равнодействующая сила
жидкость
Каждая молекула внутри жидкости (А и В) окружена другими молекулами и силы взаимодействия её с ними распределены симметрично: в результате все внутренние молекулы, как бы пребывают в состоянии внутреннего равновесия, равнодействующая сил равна нулю. В ином положении находятся молекулы на границе раздела фаз (С). Силы притяжения, действующие со стороны жидкости, не уравновешиваются силами, действующими со стороны газообразной фазы. Следовательно, действующая молекулярных сил не равна нулю. Эта действующая сила перпендикулярная к поверхности жидкости есть внутреннее давление. Оно втягивает молекулы, расположенные на поверхности жидкости внутрь и тем самым стремится снизить поверхность до минимума (роса, слеза – шар).
Сила, действующая на единицу длины границы раздела и обуславливающая сокращение поверхности жидкости – поверхностное натяжение – σ.
σ = дин/см ; σ = Дж/м2 = Н·м/м2 = Н/м; Н/м = дин/см · 10-3
Поверхностное натяжение воды самое высокое = 72,8 Н/м, C2H5OH σ = 15 Н/м, кровь σ = 45,5 Н/м, ртуть σ = 436 Н/м. Упругость пара выше у спирта по сравнению с водой, т.к. спирт обладает меньшим поверхностным натяжением.
На границе жидкость – газ всегда преобладает поверхностное натяжение.
Из законов Рауля следует, что молекулы стремятся улетать, поэтому они постоянно испаряются и стремятся покинуть жидкость, при этом они совершают работу по преодолению поверхностного натяжения. В результате возникает поверхностный слой молекул с избыточной энергией. Величина поверхностной энергии – F – произведение поверхностного натяжения на величину всей поверхности.
F = σ · S (Дж/м2 · м2 = Дж)
Из термодинамики известно, что всякая система стремится к минимуму энергии, то есть к снижению поверхностной энергии, которая может снизиться за счёт следующих факторов:
-
За счёт снижения площади.
-
За счёт снижения поверхностного натяжения.
Для уменьшения величины поверхностного натяжения необходимо увеличить температуру, так как молекулы двигаются быстрее и поверхностную плёнку разрывают (мыло в тёплой воде лучше мылится, чем в холодной). Понизить поверхностное натяжение можно путём добавления специальных веществ – ПАВ – поверхностно-активные вещества (стиральный порошок при стирке).
Способность растворённых веществ изменять поверхностное натяжение раствора – g – поверхностная активность, которая выражается:
g = -dσ / dc = -∆σ / ∆c = - (σ1- σ2)/(с1-с2)
При растворении веществ поверхностное натяжение снижается, так как молекулы растворенного вещества будут подниматься наверх, и разрушать поверхностную плёнку, а поверхностная активность будет увеличиваться.

 –
Молекула воды.
–
Молекула воды.

















 –
ПАВ
–
ПАВ
К ПАВ относят: мыла, спирты, белки, карбоновые кислоты.
Растворённое вещество может переходить внутрь раствора и взаимодействовать с молекулами растворителя. Эти вещества буду усиливать поверхностный слой, и повышать поверхностное натяжение, а поверхностная активность будет уменьшаться.
Те вещества, которые увеличивают поверхностное натяжение называются поверхностно-инактивные вещества – ПИАВ, к ним относят: соли, щёлочи, кислоты, глицерин, α-аминокислоты.
Растворенное вещество, не изменяющее поверхностное натяжение (при этом молекулы равномерно распределены между поверхностным слоем и объемом раствора) называются поверхностно-нейтральные вещества - ПНВ (сахар, глюкоза, углеводы).
Величина поверхностного натяжения зависит от концентрации этих веществ, а не только от их природы. Существует график зависимости поверхностного натяжения от концентрации – изотерма поверхностного натяжения при постоянной температуре.
σ
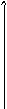
 ПИАВ
ПИАВ

 72,8 ПНВ
72,8 ПНВ
ПАВ

сonst С
Поверхностное натяжение становится постоянным, когда ПАВ занимают всю поверхность.
Дифильность
Молекулы ПАВ состоят из двух частей: полярная часть: – OH, – COOH, – COONa; и неполярной части – R: – C2H5.


R
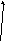
 – COOH =>
– COOH =>

«хвост»
«голова»
Полярная часть - голова гидрофильная («любит» воду), хвост – гидрофобный («боится» воды).
Подобное растворяется в подобном. ПАВ находится на границе раздела и ориентируется в поверхностном слое согласно своему строению («голова» в воде, «хвост» - снаружи). ПАВ снижают взаимодействие молекул в поверхностном слое за счёт расклинивающего действия, и это ведёт к снижению поверхностного натяжения.
На снижение поверхностного натяжения высокую роль играет не только взаимодействие с ПАВ, но и природа ПАВ, а именно длина углеводородного радикала. Закономерность Дюкло-Траубе: поверхностная активность вещества одного гомогенного ряда (спирты) возрастает в 3 раза при удлинении углеводородной цепи на 1 звено (CH2) – метиленовой группы.
Применение ПАВ.
Основное применение ПАВ нашли в синтезе моющих средств.
Возрастание наркотического действия современных препаратов связано с удлинением углеводородной цепи (анальгин, промедол, опиум). В хирургии ПАВ применяют в качестве антисептиков: фенол, четвертичные аммониевые основания.



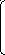

 CH3 +
CH3 +


 OH H3C N
CH3 OH–
OH H3C N
CH3 OH–
CH3
Создание ПАВ с длинной цепью С8 –С14 … привело к выявлению у этих веществ антифаговой активности.
ПАВ находятся в крови человека и к ним относят: белки, фосфолипиды (у них 2 хвоста), спирты. ПАВ ориентируются в крови в виде мицелл – коллоидная частица со сложной структурой.
Смотрим Рис. 12 - 1
Если концентрация фосфолипидов высокая, то начинается построение липосомы.
Смотрим Рис. 12 - 2
Л12 ФИЗИКО-ХИМИЯ ПОВЕРХНОСТНЫХ ЯВЛЕНИЙ.
В водных растворах:



 В растворах желчных
кислот:
В растворах желчных
кислот:











 Мицелла
Мицелла



















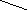









































 H2O
H2O








Рис. Образование мицелл.__________________________________________________