
- •Лекция 15. Основы термодинамики
- •14. 1. Условия термодинамического равновесия системы.
- •14. 2. Квазистатические процессы. Обратимые и необратимые процессы.
- •14. 3. Макроскопическая работа.
- •14. 4. Количество теплоты.
- •14. 5. Первое начало термодинамики.
- •14. 6.Внутренняя энергия идеального газа. Закон Джоуля.
- •14. 7. Теплоемкость.
- •14. 7.1. Уравнение Майера.
- •14. 7. 2. Теплоемкость и степени свободы.
- •14. 7. 3. Теплоемкость идеального газа.
- •14. 7. 4. Зависимость теплоемкости от температуры.
- •14. 8. Адиабатический процесс. Уравнение Пуассона.
- •14. 9. Калорическое уравнение идеального газа.
- •14. 10. Политропические процессы.
14. 3. Макроскопическая работа.
Найдем
работу, совершаемую газом, заключенным
в мягкую эластичную оболочку (рис. 14.1),
при его квазистатическом расширении.
Работа,
совершаемая газом при перемещении
элемента площади
![]() оболочки на расстояние
оболочки на расстояние![]() вдоль нормали
вдоль нормали![]() ,
равна
,
равна
|
|
(14.1) |
|
|
Проинтегрировав
выражение
|
|
Рисунок 14. 1 |
Т.о.,
получаем, что элементарная
работа
![]() газа по квазистатическому расширению
оболочки равна
газа по квазистатическому расширению
оболочки равна
|
|
(14.2) |
Поскольку
для квазистатических процессов
![]() ,
то работа
,
то работа![]() внешних сил над оболочкой с газом равна
внешних сил над оболочкой с газом равна
|
|
(14.3) |
Если мы хотим определить работу, совершаемую в конечном процессе, то надо вычислить интеграл
|
|
(14.4) |
Однако такое вычисление можно провести лишь в том случае, когда давление является определенной функцией объема. Между тем, как следует из уравнения состояния, давление в системе зависит не только от её объема, но и температуры. Поэтому, меняя в ходе процесса температуру, можно квазистатически перевести систему из начального в конечное состояние бесконечным числом способов. При этом каждому способу соответствует своя функция.
Т.о.,
работа
![]() не определяется однозначно заданием
начального и конечного состояний
системы, а зависит также от способа, или
«пути» перехода системы между этими
состояниями.
не определяется однозначно заданием
начального и конечного состояний
системы, а зависит также от способа, или
«пути» перехода системы между этими
состояниями.
Определение. Величины, имеющие вполне определенные значения в каждом состоянии системы, называются функциями состояния.
Понятно,
что работа данному определению не
удовлетворяет и поэтому не может являться
функцией состояния. Более того, можно
сказать, что
работа
![]() характеризует
не состояние системы, а совершаемый
последней процесс.
характеризует
не состояние системы, а совершаемый
последней процесс.
Поскольку
величина работы
![]() зависит от способа пути перехода между
состояниями и не определена однозначно
для конечного состояния, мы пишем для
работы, совершаемой системой на бесконечно
малом перемещении,
зависит от способа пути перехода между
состояниями и не определена однозначно
для конечного состояния, мы пишем для
работы, совершаемой системой на бесконечно
малом перемещении,![]() ,
а не
,
а не![]() .
.
Графически
работа может быть представлена площадью
под кривой, описывающей процесс в
координатах
![]() (или на плоскости
(или на плоскости![]() ).
).
|
|
Пусть
система квазистатически переходит
из состояния
Поэтому
работа
|
|
Рисунок 14. 2. |
Вычислим работу, совершаемую молем идеального газа в трех различных процессах:
|
1.
|
(14.5) |
|
2.
|
(14.6) |
|
3.
|
(14.7) |
Приведенный пример наглядно указывает на зависимость работы, совершаемой системой от пути перехода из начального состояния в конечное
|
|
Если
система в результате произведенных
в ней изменений вернулась в исходное
состояние, то говорят, что она совершила
круговой
процесс,
или цикл.
Если произведенный процесс
квазистатический, то на диаграмме
|
|
Рисунок 14. 3. |


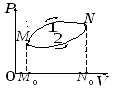
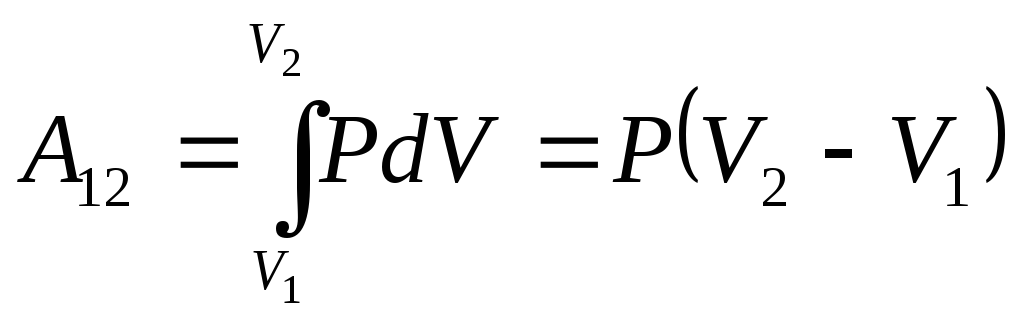 ;
;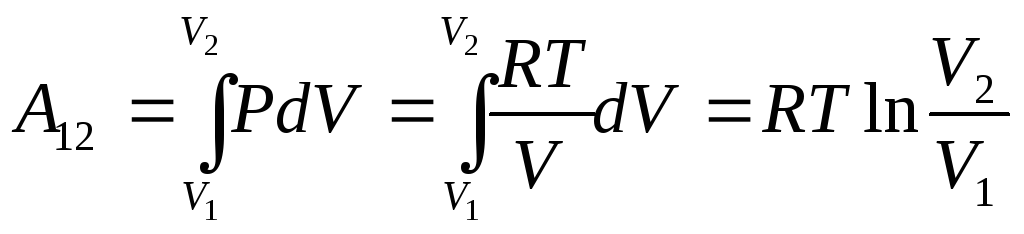 .
.