
-
Классификация катализаторов
Существующее в настоящее время огромное количество катализаторов можно классифицировать по разным критериям: структура, состав, катализируемые процессы, агрегатное состояние и др.
По агрегатному состоянию все катализаторы можно разделить на две большие группы – гомогенные и гетерогенные (Рис. 1.9).
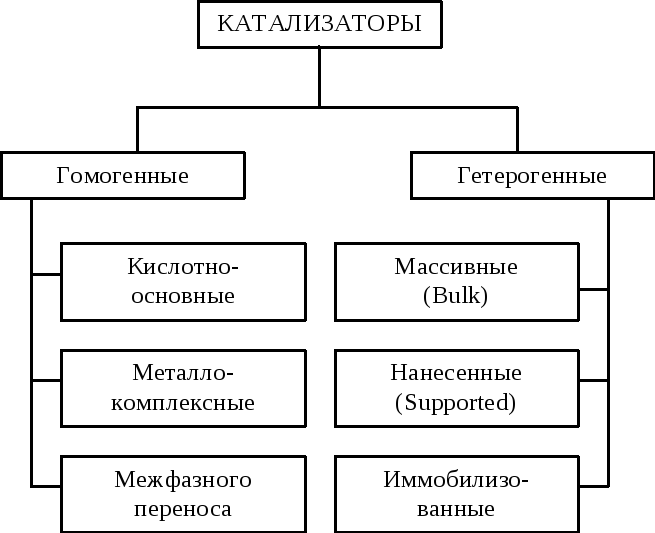
Рис. 1.9. Классификация катализаторов
Гомогенными называются катализаторы, находящиеся в одной фазе с реагентами.
Гетерогенными называются катализаторы, образующие отдельную фазу, не смешивающуюся с реагентами и продуктами. Как правило, это твердые катализаторы.
Каждую из подгрупп катализаторов, представленных на рисунке (1.9) можно, в свою очередь, квалифицировать по различным признакам. Особенно это касается гетерогенных катализаторов, среди которых можно выделить оксидные, кислотные, основные, однокомпонентные, многокомпонентные, металлические и т.д.
|
Массивный катализатор (Fe при синтезе NH3 из N2 и H2) |
Нанесенный катализатор (Pt на силикагеле. Платформинг) |
Иммобилизованный катализатор (Активный компонент химически связан с носителем. Катиониты и аниониты) |
|
|
|
|
Рис. 1.10. Классификация гетерогенных катализаторов по типу активных центров. АК - активный компонент; АЦ - активный центр.
Чаще всего гетерогенные катализаторы классифицируют по типу активных центров (рис. 1.9.) на массивные, нанесенные и иммобилизованные. На рисунке (1.10) схематично изображено строение каждой из этих групп катализаторов.
Массивный катализатор целиком состоит из активного компонента, а активные центры представляют собой доступные для реагентов атомы или группы атомов на поверхности катализатора. Примером служат гранулированный железный катализатор синтеза аммиака, и сетка из сплава платины и родия, являющаяся катализатором окисления аммиака в производстве азотной кислоты.
Нанесенные катализаторы состоят из носителя и нанесенного на его поверхность тем или иным физическим методом активного компонента. При этом носитель может быть как инертным в данном процессе, так и оказывать определенное каталитическое либо промотирующее действие. Примером служит катализатор реформинга, представляющий собой гранулы оксида алюминия с нанесенной на их поверхность металлической платиной.
Иммобилизованные катализаторы это катализаторы, в которых активный компонент химически закреплен на поверхности твердого материала (носителя). Например сульфокатиониты, представляющие собой сульфированный сополимер стирола с дивинилбензолом. Сульфокатиониты содержат -SO3H группы в ароматических фрагментах полимера (носителя) и служат кислотными катализаторами, например, в синтезе метилтретбутилового эфира.
-
Сравнение гомогенного и гетерогенного катализа
Гомогенные катализаторы отличаются значительно большей степенью дисперсности. Каждая молекула гомогенного катализатора является каталитическим центром, в то время как в гетерогенном катализаторе активны только доступные для реагентов центры на поверхности. Следовательно, гомогенный катализатор обладает гораздо большей активностью на единицу массы катализатора. Это позволяет использовать его в гораздо меньших концентрациях, чем гетерогенный.
Гомогенно-каталитические реакции протекают чаще всего под кинетическим контролем, так как скорость диффузии реагентов к каталитическому центру значительно выше скорости собственно химической реакции.
Так как гомогенные катализаторы – это легко идентифицируемые химические соединения, то механизмы гомогенно-каталитических реакций изучены, как правило, хорошо. Для гетерогенных же каталитических процессов представление о механизме реакций часто достаточно туманны и противоречивы.
Основным недостатком гомогенного катализа является сложность отделения катализатора от продуктов реакции и его рециркуляция. Наоборот, для гетерогенного катализа сепарация (выделение) либо не требуется вообще (в случае стационарного слоя катализатора), либо осуществляется такими простыми способами как фильтрация или центрифугирование. Для выделения гомогенных катализаторов требуются значительно более сложные (энергоемкие) процессы, такие как экстракция, ректификация или ионный обмен. Кратко сравнение достоинств и недостатков гомогенных и гетерогенных катализаторов приведено в таблице 1.1.
Идеальным выглядело бы создание катализаторов, обладающих положительными свойствами как гомогенных (высокая удельная активность и селективность), так и гетерогенных (простота сепарации) катализаторов.
В настоящее время очевидно стремление перехода от гомогенно- к гетерогенно-каталитическим процессам. В современной химической промышленности доля гомогенно-каталитических процессов составляет 10-15%.
За свою историю промышленный катализ прошел огромную эволюцию благодаря развитию инструментальных методов исследования катализаторов и механизмов каталитических реакций. Целью этих исследований является создание общей теории катализа - теории, которая бы позволяла предсказывать и создавать катализаторы для всех типов катализа – гомогенного, гетерогенного и ферментативного. Однако до сих пор этого сделать не удалось.
Таблица 1.1.
Сравнение гомогенных и гетерогенных катализаторов.
|
Характеристика |
Гомогенные |
Гетерогенные |
|
Эффективность |
||
|
Активные центры
Концентрация
Селективность
Диффузионные затруднения
Условия реакции
Применимость
Дезактивация |
Каждая молекула
Низкая
Высокая
Отсутствуют
Умеренные (<200оС)
Ограничена (растворимость; фазовое состояние; гидролиз и пр.)
Необратимые реакции с компонентами реакционной массы; разложение |
Только доступные атомы на поверхности
Высокая
Низкая
Присутствуют (часто скорость реакции лимитируется диффузией)
Жесткие (часто >250оС)
Широкая
Разрушение; зашлаковываемость (напр. закоксовывание); отравление |
|
Свойства катализаторов |
||
|
Структура/стехиометрия
Возможность модификации
Термическая стабильность |
Определенные
Высокая
Низкая |
Неопределенные
Низкая
Высокая |
|
Сепарация (Выделение из реакционной массы) |
||
|
Сепарация
Рецикл |
Трудоемкая (химическое связывание; разложение; дистилляция; экстракция; ионный обмен)
Возможен, но сложен |
Не сложная. Для стационарного слоя - не требуется; Для суспендированного катализатора - фильтрация или центрифугирование.
Для стационарного слоя - не требуется; Для суспендированного катализатора - легко осуществим. |



