
- •Неравновесные явления
- •Тема 2: Реакции первого и второго порядка
- •Тема 3: Зависимость скорости реакции от температуры
- •Тема 4: Определение порядков химических реакции
- •Тема 5: Сложные химические реакции
- •Электрохимия
- •Тема 6: Электрическая проводимость и подвижность ионов
- •Тема 7: Теория электролитической диссоциации. Слабые и сильные электролиты
Федеральное государственное автономное образовательное учреждение высшего профессионального образования
«Уральский федеральный университет имени первого
Президента России Б.Н.Ельцина»
Брусницына Людмила Александровна
Неравновесные явления
В СЛОЖНЫХ ХИМИЧЕСИХ ПРОЦЕССАХ
Примеры решения задач
для студентов, обучающихся
по программе бакалавриата по направлению подготовки
240100 – Химическая технология
Екатеринбург
2015
Тема 1: Кинетика химических реакций.
Реакции первого и второго порядка
Основные расчетные формулы:
![]()
![]() ;
;
![]()
Глубина протекания химической реакции
![]()
Плотность глубины реакции
![]()
Реакция I порядка, интегральное уравнение:
![]() ;
;
![]()
Реакция II порядка: А+В=С
![]()
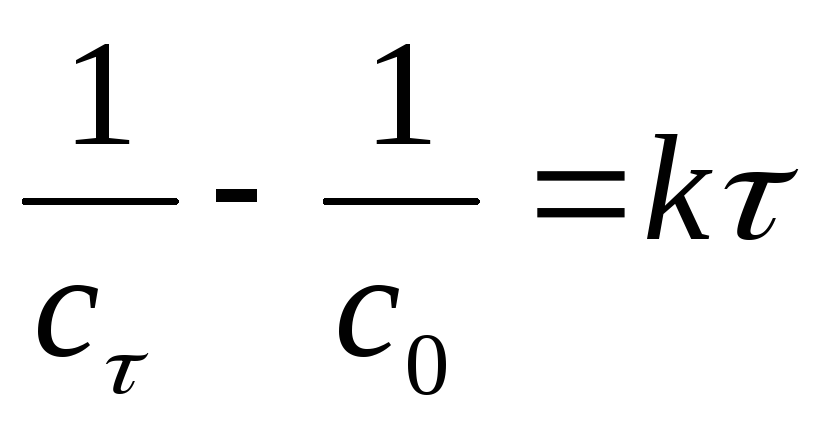 ;
;
![]()
![]()
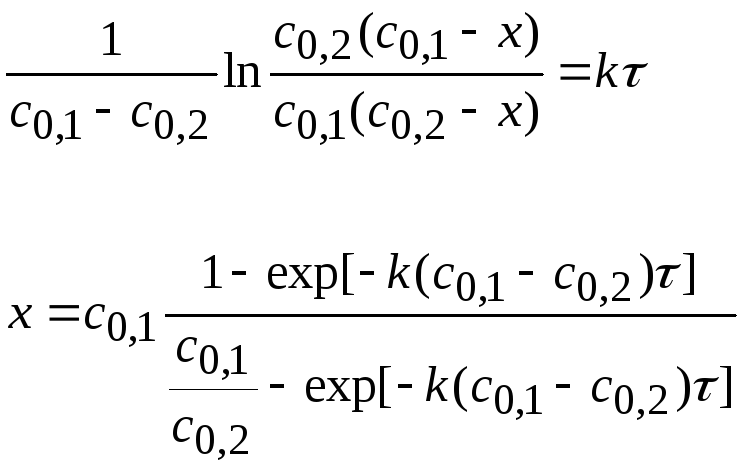
Существует понятие суммарный порядок реакции n = ∑nk и частный порядок реакции по компоненту
![]()
Уравнение Аррениуса:
![]() или
или
![]()
Графическое или аналитическое определение Еа
![]() - система координат
при графическом решении уравнения
Аррениуса.
- система координат
при графическом решении уравнения
Аррениуса.
![]()
![]()
![]()
Аналитический расчет:

Задача № 1
Термическое разложение в газовой фазе (Т = 849 К, V-const)
С2Н5СНО = С2Н6 + СО
происходит как одностадийная реакция. Эта стадия является односторонней, мономолекулярной. Рассчитайте константу скорости прямой реакции по следующим данным:
-
τ, с
0
50
300
450
610
700
∞
р, мм.рт.ст.
(общее давление)
314
345
438
475
510
525
628
Решение:
Для реакции I порядка справедливо интегральное уравнение
![]() ;
;
![]()
k должно быть постоянной.
Рассмотрим реакцию
|
|
С2Н5СНО = С2Н6 + СО | ||
|
τ = 0 |
р0 |
х=0 |
х=0 |
|
τ = τ |
р0 – х |
х |
х |
Р0 – исходное давление С2Н5СНО. В любой момент времени общее давление пара равно
![]() ,
тогда
,
тогда
![]() ;
отсюда
;
отсюда
![]()
3)
![]()
![]()
![]()
Значение k внесем в таблицу:
|
τ, с |
0 |
50 |
300 |
450 |
610 |
700 |
∞ |
|
k∙103, с-1 |
|
2.08 |
1.67 |
1.59 |
1.60 |
1.59 |
|
4) Вычислим значение kср
![]() с-1
с-1
Задача № 2
В реакции
формальдегида с пероксидом водорода
образуется муравьиная кислота (реакция
II
порядка,
![]() )
)
НСНО + Н2О2 = НСООН + Н2О
За время τ
= 2 часа при 333,2 К
![]() .
Вычислите константу скорости реакции;
определите время, за которое прореагирует
90% исходных веществ; рассчитайте время,
за которое реакции дойдет до той же
глубины, если (
.
Вычислите константу скорости реакции;
определите время, за которое прореагирует
90% исходных веществ; рассчитайте время,
за которое реакции дойдет до той же
глубины, если (![]() )
исходную смесь разбавить в 10 раз.
)
исходную смесь разбавить в 10 раз.
Дано:
Реакция II порядка
![]()
Т = 333,2 К
τ1 = 2 часа; сτ1 = 0,215 моль/л
сτ2 = 0,1с0 (90%)
![]()
____________________________________________
К-? τ2-? τ3-?
Решение:
|
|
НСНО + Н2О2 = НСООН + Н2О | |||
|
τ = 0 |
с0 = 1 моль/л |
с0 = 1 моль/л |
0 моль/л |
0 моль/л |
|
τ1 = 2 часа |
сτ1 = 0,215 моль/л |
сτ1 = 0,215 моль/л |
х моль/л |
х моль/л |
|
τ2 = ? |
сτ2 = 0,1 моль/л |
сτ2 = 0,1 моль/л |
0,9 моль/л |
0,9 моль/л |
|
τ3 = ? |
сτ3 = 0,01 моль/л |
сτ3 = 0,01 моль/л |
0,09 моль/л |
0,09 моль/л |
Для реакции II порядка при с1,0=с2,0
1)
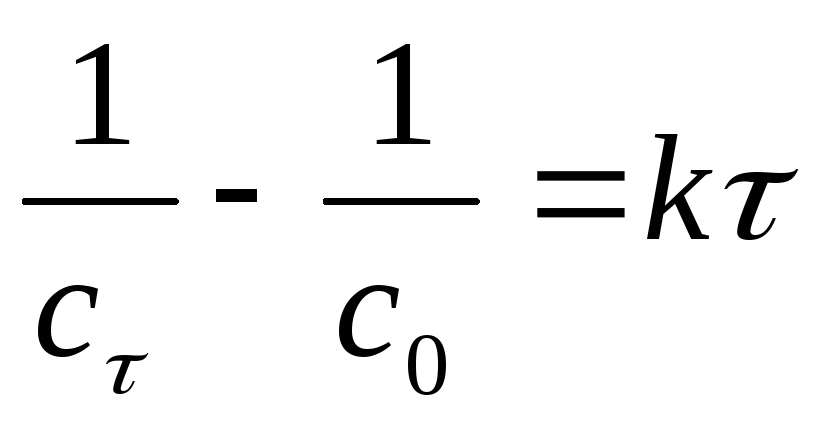 =>
=>
![]()
![]()
2)
![]()
3)
![]()
![]()
Вывод: Если исходные компоненты разбавить в 10 раз, то для достижения той же глубины реакции нужно в 10 раз больше времени.
Задача № 3
Для реакции А→В к = 0,5. Вычислить степень превращения вещества А за время 1 час, если реакция идет по 0, 1 и 2 порядку и с0,1 = 1 моль/л . Определите, как зависит степень превращения вещества от порядка реакции.
Дано:
с0,А = 1 моль/л
к = 0,5
τ = 1 час
________________________
α−?
Решение:
Реакция 0 порядка:
![]()
Реакция 1 порядка:
![]() ;
;
![]()
![]()
Реакция II порядка
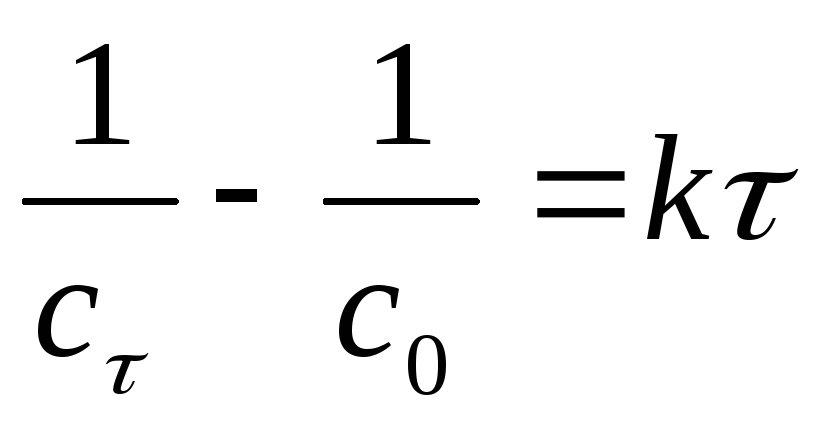 при с0,1
= С2,0
при с0,1
= С2,0
![]()
![]()
Сведем данные расчета в таблицу:
-
Порядок реакции, n
0
1
2
Степень превращения, α
0,5
0,394
0,333
Вывод: При одинаковом значении константы скорости реакции с увеличением порядка реакции уменьшается степень превращения вещества.
Задача № 4
Рассчитать константу скорости реакции кристаллического фиолетового со щелочью по следующим данным
|
τ, с |
0 |
600 |
900 |
1500 |
2340 |
2800 |
|
D |
0,600 |
0,405 |
0,320 |
0,220 |
0,140 |
0,091 |
Щелочь берется в избытке: сщ,0 = 1,8 моль/л, скр,0 = 0,01 моль/л, t = 27 0С.
Решение:
1) Реакция цветная, за концентрацией красителя можно судить по изменению D: D=ε с l
![]()
![]() или
или
![]()
![]()
2) Рассчитать k можно графически или аналитическим расчетным способом. Строим график в координатах lnD = f(τ); k’ = -a = −tgα
|
τ, с |
0 |
600 |
900 |
1500 |
2340 |
2800 |
|
lnD |
-0,511 |
-0,903 |
-1,139 |
-1,514 |
-1,966 |
-2,397 |

2)
![]()
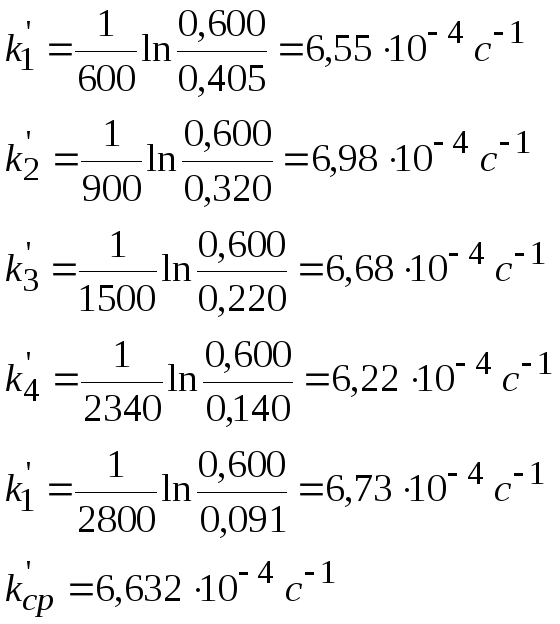
Задача № 5
Дана реакция 2 порядка А+В=С. Исходные концентрации с0,А = с0,В. За время 500 с реакция проходит на 20%. За какое время она пройдет на 60%?
Решение:
Интегральное уравнение реакции II порядка:
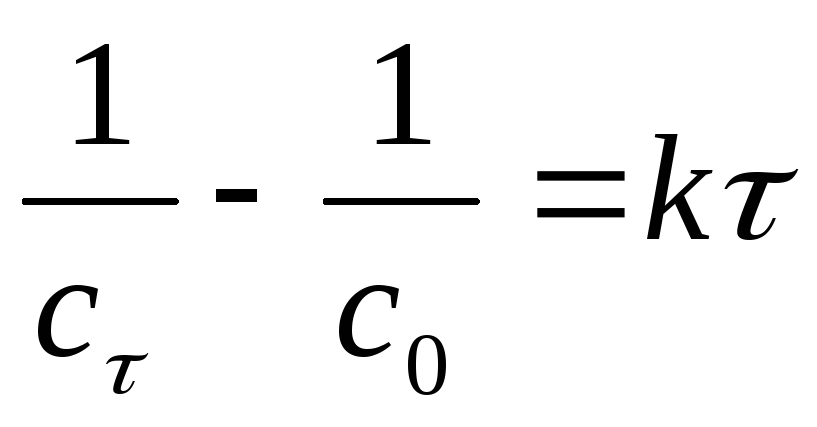 ;
с0
= 100% = 1, сτ
= 100 - 20 = 80% = 0,8
;
с0
= 100% = 1, сτ
= 100 - 20 = 80% = 0,8
![]()
![]()
Ответ: за 3000 с реакция пройдет на 60%.
