
изменениеэнергииГиббсаисоставьтесхемугальваническогоэлемента, T  298 К.
298 К.
[E  1 21 В;
1 21 В;  G
G 
 233 7 кДж/моль]
233 7 кДж/моль]
23. Вычислитеактивностьионовводородаврастворе, вкоторомпотенциалводородногоэлектродаравен 82 мВ, T  298 К. [a
298 К. [a  H
H 

 0 04 моль/л]
0 04 моль/л]
24. Для определения pH желчи (из желчного пузыря) была составлена цепь из водородного и хлорсеребряного электродов, ЭДС которой оказалась равной 0,577 В при T  298 К. Концентрация электролита в электроде сравнения равна 1 моль/л. Определите pH пузырнойжелчи.
298 К. Концентрация электролита в электроде сравнения равна 1 моль/л. Определите pH пузырнойжелчи.
[pH  желчи
желчи
 5 75, что соответствуетнорме]
5 75, что соответствуетнорме]
25. Вычислитепотенциалсеребряногоэлектрода, опущенноговнасыщенный раствор AgI ( Ks  AgI
AgI 
 8 3 10 17 ), T
8 3 10 17 ), T  298 К.
298 К.
[ Ag |
Ag 0 33 В] |
26. |
Для измерения pH слезной жидкости составили гальва- |
ническую цепь из водородного и каломельного электродов, ЭДС которой оказалась равной 0,764 В при T  298 K концентрация электролитавэлектродесравненияравна 0,1 моль/л. Определите pH и концентрацию ионовводородав слезнойжидкости.
298 K концентрация электролитавэлектродесравненияравна 0,1 моль/л. Определите pH и концентрацию ионовводородав слезнойжидкости.
[pH 7 24; a  H
H 

 5 8 10 8 моль/л]
5 8 10 8 моль/л]
27.Гальванический элемент составлен из двух водородных электродов, погруженных в растворы ацетата натрия и хлорида аммония с концентрациями по 1,0 моль/л. Вычислите ЭДС цепи при 298 К.
[E  0 280 В]
0 280 В]
28.Вычислите диффузионный потенциал, возникающий на
границе |
0,01 М и 0,001 М растворов |
KBr при 25 С, если |
u K |
7 62 10 |
|
8 м2 В с , u Br |
|
|
8 12 10 |
|
8 м2 В с . |
|
|
|
|
[ д |
0 0018 В] |
|
|
|
29. |
Определитезначениемембранногопотенциалапри37 С, |
если концентрация ионов K  внутри клетки в 20 раз больше, чем снаружи.
внутри клетки в 20 раз больше, чем снаружи.
[ м 0
м 0 08 В]
08 В]
30. Вычислите теоретическое значение редокс-потенциала для системы, содержащей по 10 мл растворов гексацианоферрата (III) калия и гексацианоферрата (II) калия с концентрациями 0,01 и 0,05 моль/л, T 298 К.
[ r 0 315 В]
31. В растворе концентрация гексацианохромат (III)-ионов в три раза превышает концентрацию гексацианохромат (II)-иона. Чему равен редокс-потенциал этой системы? T 298 К.
[ r 1 25 В]
32. Бромная вода — часто используемый в лабораторной практике реактив. Какие из перечисленных ниже ионов можно окислить бромной водой: а) золото (I); б) олово (II); в) кобальт (II); г) медь (II). Ответ подтвердите расчетом, сделанным для стандартного состояния.
[бромной водой можно окислить ионы олова (II) и кобальта (II)]
33. Будет ли протекать окисление нитрит-иона пермангана-
том калия при T 298 К и pH 6 0, если c NO3 |
c NO3 |
|
c MnO |
|
c Mn2 |
0 1 моль/л? |
|
|
4 |
|
|
|
|
[E 0 456 В, т. е. E 0, реакция протекает самопроизвольно]
34. Концентрации ацетат- и пируват-ионов в системе равны между собой. Чему станет равным редокс-потенциал этой биологической редокс-системы при pH 6 и pH 8? T 298 К.
[при pH 6 r 0 64 В; при pH 8 r 0 76 В]
35. Для системы НАД НАДН H формальный редокспотенциал равен 0 320 В. Вычислите редокс-потенциал при восстановлении 15% НАД , T 298 К.
[ r 0 324 В]
36. В ходе биологического окисления протекает следующая реакция
Редокс-потенциал пары НАД НАДН H равен 0 32 В при pH 7 0, а пары ФП ФПH2 равен 0 060 В, T 298 К. Найдите
величину Gр-ции реакции и укажите, на что расходуется выделяемая энергия.
[ G 50 2 кДж, выделяемая энергия в митохондриях расходуется на синтез АТФ]
37.Рассчитайте количество вещества цитохрома c1 в окисленной форме, которое может образоваться из соответствующей восстановленной формы за счет энергии, освобождаемой при окислении глюкозы в количестве 1 моль при с. у.
[ 0 14 моль]
38.ЭДС элемента Pt, H2 NH4OH, NH4Cl KCl, AgCl Ag равна 0,746 В при 25 ÆС. Определите pH и соотношение концентраций компонентов, входящих в состав аммиачной буферной си-
стемы. xc 0 201 В, pK NH4OH 4 76.
[pH буфера 9 24; соотношение концентраций компонентов буферной системы равно 1]
39.Рассчитайте потенциал водородного электрода при 25 ÆС
вбуферном растворе, приготовленном из 500 мл 0,1 М раствора
Na2HPO4 и 350 мл 0,05 М раствора NaH2РO4; pK H2PO4 [ 2H H2 0 452 В]
40.Сравните окислительную способность озона и кислорода по отношению к нейтральному водному раствору иодида калия. Ответ подтвердите расчетами.
[ионы I окисляются озоном, но не окисляются кислородом]
41.Содержащиеся в растениях нитраты могут восстанавливаться в нитриты и реагировать в желудке с входящими в со-
став пищевых продуктов вторичными аминами с образованием сильных канцерогенов — нитрозаминов. Определите, могут ли in vivo нитрат-анионы восстанавливаться аскорбиновой кислотой
с образованием нитрит-анионов.
[аскорбиновая кислота восстанавливает нитрат-ионы с образованием нитрит-анионов]
42. Редокс-потенциал системы НАДФ НАДФН при 298 К и pH 7 равен 0 3 В. Как надо изменить pH, чтобы редокс-по- тенциал стал численно равным формальному редокс-потенциалу этой системы Æ 0 324 В?
[pH 7 41]

43.Обоснуйте возможность протекания следующих реакций
вс. у., используя табличные данные. Подберите коэффициенты ионно-электроннымметодом:
1)HI  HNO 2
HNO 2 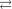 I2
I2  NO
NO  H2O
H2O
2)KMnO 4  H2O2
H2O2  H2SO 4
H2SO 4  O2
O2  MnSO 4
MnSO 4  K2SO 4
K2SO 4  H2O
H2O
3)KMnO 4  Na2SO 3
Na2SO 3  H2SO 4
H2SO 4 
4)KMnO 4  Na2SO 3
Na2SO 3  H2O
H2O 
5)KMnO 4  Na2SO 3
Na2SO 3  KOH
KOH 
6)KI  FeCl 3
FeCl 3  I2
I2  KCl
KCl  FeCl 2
FeCl 2
7)FeSO 4  I2
I2  H2SO 4
H2SO 4  Fe2
Fe2  SO 4
SO 4  3
3 



8)Fe 2
 Cr2O27
Cr2O27 
 H
H 
 Cr3
Cr3
 Fe 3
Fe 3




9)KMnO 4  KNO 2
KNO 2  KOH
KOH 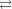 KNO 3
KNO 3  K2MnO 4
K2MnO 4 



10)Pb 2
 Cl2
Cl2  H2O2
H2O2  PbO 2
PbO 2  2Cl
2Cl
44. Определите, можнолиокислитьмедьконцентрированным иразбавленнымрастворамиазотнойкислоты, если 

 Cu 2
Cu 2
 Cu
Cu 

 0 34 В;
0 34 В; 
 NO 3 NO 2 0 8 В;
NO 3 NO 2 0 8 В; 
 NO 3 NO
NO 3 NO 
 0 96 В?
0 96 В?
Ответ поясните, напишите уравнения реакций, укажите протекающиена электродахпроцессы, рассчитайте значение ЭДС. [окислить можно и концентрированным и разбавленным растворамиазотной кислоты]
45. Можно ли совмещать в ротовой полости протезы, приготовленныеизнержавеющейсталиизолота? Составьтесхемугальванического элемента и покажите его работу в нейтральной слю-
не, обогащенной кислородом. Рассчитайте ЭДС ( 

 Fe2
Fe2
 Fe
Fe 
 0 44 В;
0 44 В; 

 Au3
Au3
 Au
Au
 1 498 В).
1 498 В).
[E  0,841 В]
0,841 В]
46. Рассмотритекоррозионныесвойс твазубныхпротезов, изготовленныхизсплаваPd сAg, вслюнесpH  6, содержащейрастворенныйкислород. РассчитайтеЭДС(
6, содержащейрастворенныйкислород. РассчитайтеЭДС( 

 Pd 2
Pd 2
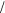 Pd
Pd 

 0 99 В;
0 99 В; 

 Ag
Ag
 Ag
Ag

 0 8 В).
0 8 В).
[E  0,075 B]
0,075 B]
47. Определите, вкакомнаправлениимогутсамопроизвольно протекать реакции. Ответ поясните. Рассчитайте значение ЭДС:
1) FeCl 3 |
KI |
FeCl 2 KCl |
I2, |
|
|
если Fe3 |
Fe2 |
0 77 В; |
I2 2I |
|
0 54 В; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2) NaCl |
|
|
|
|
Fe2 |
SO 4 |
3 |
FeSO 4 |
Cl2 |
|
|
|
Na2SO 4, |
если |
Fe 3 |
|
Fe2 |
|
|
|
|
|
0 77 В; |
Cl2 |
|
2Cl |
|
|
|
|
|
|
1 36 В; |
|
|
|
|
|
|
3) SnCl 2 |
|
|
|
|
FeCl 3 |
|
SnCl 4 |
FeCl 2 |
, |
|
|
Fe2 |
|
|
если |
Sn 4 |
|
|
Sn 2 |
|
|
|
|
|
0 15 В; |
Fe |
3 |
|
|
|
0 77 В; |
4) 2Mn 2 |
|
|
|
|
|
5Br2 |
8H2O |
2MnO |
|
|
|
|
10Br |
|
|
16H , |
4 |
|
|
|
|
|
если |
MnO |
|
|
|
|
|
Mn2 |
|
|
1 51 В; |
|
Br2 |
2Br |
|
|
|
1 06 В; |
|
4 |
|
|
|
|
|
|
5) Mn 2 |
|
|
|
|
|
|
|
NO |
|
|
|
MnO |
|
|
NO |
|
, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
4 |
2 |
|
|
|
Mn2 |
|
|
если |
NO |
|
|
|
|
NO |
|
|
|
|
0 83 В; |
MnO |
|
|
|
1 51 В; |
3 |
|
2 |
|
|
|
4 |
|
|
6) PbO 2 |
|
|
KI |
|
|
|
H2SO 4 |
|
|
I2 |
K2SO |
4 |
|
|
|
PbSO 4 H2O, |
если |
I2 |
2I |
|
|
|
|
|
|
|
|
|
0 54 В; |
|
|
PbO 2 |
|
Pb 2 |
|
|
|
|
|
|
1 68 В; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
7) KF |
|
|
FeCl 3 |
|
|
|
|
F2 |
FeCl 2 |
KCl, |
|
|
|
|
|
|
|
|
|
|
если |
F2 |
2F |
|
|
|
|
|
|
2 87 В; |
Fe3 |
|
Fe2 |
|
|
|
|
|
|
0 77 В; |
|
|
|
|
|
|
|
|
|
|
|
|
8) NaNO 2 KMnO 4 H2SO 4 |
NaNO 3 MnSO |
4 K2SO 4 H2O, |
если |
NO |
|
|
|
NO |
|
|
|
|
0 83 В; |
MnO |
|
|
Mn2 |
|
1 51 В. |
3 |
|
|
2 |
|
|
4 |
|
|
48. |
Мембранныйпотенциалнервнойклеткисоставил 80 мВ |
при 310 К. Концентрация ионов калия внутри клетки составила 150 ммоль/л. Чему равна концентрация ионов калия во внеклкточнойжидкости?
[7,5 ммоль/л]
49. Можно ли ионы NO 2 восстановить ионами Br ? Ответ подтвердитерасчетами.
[нельзя]
50. Определите, какая из реакций пойдет в первую очередь в кислой среде при добавлении KMnO4 к смеси Na2SO3 и NaNO2. Ответ подтвердите расчетами.
[c Na2SO3]

М о д у л ь 5
ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ. ДИСПЕРСНЫЕ СИСТЕМЫ.
ВМС И ИХ РАСТВОРЫ
ОСНОВНЫЕ ВЕЛИЧИНЫ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ХАРАКТЕРИСТИКИ ПОВЕРХНОСТНЫХ ЯВЛЕНИЙ, КОЛЛОИДНЫХ И РАСТВОРОВ ВМС
Параметр |
Обозначение, |
Смысловое значение |
|
единица |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Свободная |
|
Gs, Дж |
|
|
|
Термодинамическая |
функция, |
поверхност- |
Gs S Gs min |
характеризующая энергию меж- |
ная энергия |
|
|
|
|
|
|
|
молекулярноговзаимодействия |
|
|
|
|
|
|
|
|
частиц на поверхности раздела |
|
|
|
|
|
|
|
|
фаз с частицами каждой из кон- |
|
|
|
|
|
|
|
|
тактирующих фаз |
|
|
|
|
|
|
|
|
|
|
|
Удельная |
|
, Дж м2 |
|
|
|
Удельная свободная |
поверх- |
свободная |
|
|
|
|
|
|
|
ностная энергия, характеризую- |
поверхност- |
|
|
|
|
|
|
|
щая энергию межфазного взаи- |
ная энергия |
|
|
|
|
|
|
|
модействия единицы площади |
или поверх- |
|
|
|
|
|
|
|
поверхности раздела фаз |
ностное |
|
|
|
|
|
|
|
|
|
натяжение |
|
|
|
|
|
|
|
|
|
Поверх- |
|
n0 |
|
mжn0 |
Поверхностное натяжение жид- |
|
ж 0 |
|
, ж 0 |
|
, |
|
ностное |
nж |
m0nж |
кости —другоеназваниеудель- |
натяжение |
ж 0 |
жn0 |
, |
|
ной свободной поверхностной |
0nж |
|
жидкости |
где 0 — поверхностное |
энергии. Приведенные форму- |
|
натяжение воды; n0 — |
лы используются для расчета |
|
числокапельводы; nж — |
поверхностногонатяженияста- |
|
число капель жидкости; |
лагмометрическим методом |
|
m0 —масса воды; mж — |
|
|
|
масса жидкости; |
|
0 — |
|
|
|
плотность воды; |
ж — |
|
|
|
плотность жидкости |
|
|










 298 К.
298 К. 1 21 В;
1 21 В; 

 233 7 кДж/моль]
233 7 кДж/моль] 298 К. [
298 К. [ H
H 

 0 04 моль/л]
0 04 моль/л] 298 К. Концентрация электролита в электроде сравнения равна 1 моль/л. Определите pH пузырнойжелчи.
298 К. Концентрация электролита в электроде сравнения равна 1 моль/л. Определите pH пузырнойжелчи. желчи
желчи
 5 75, что соответствуетнорме]
5 75, что соответствуетнорме] AgI
AgI 
 8 3 10
8 3 10  298 К.
298 К. 298 K концентрация электролитавэлектродесравненияравна 0,1 моль/л. Определите pH и концентрацию ионовводородав слезнойжидкости.
298 K концентрация электролитавэлектродесравненияравна 0,1 моль/л. Определите pH и концентрацию ионовводородав слезнойжидкости. H
H 

 5 8 10
5 8 10  0 280 В]
0 280 В] внутри клетки в 20 раз больше, чем снаружи.
внутри клетки в 20 раз больше, чем снаружи.
 08 В]
08 В] HNO
HNO 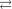 I
I NO
NO  H
H H
H H
H O
O MnSO
MnSO  K
K H
H Na
Na H
H
 Na
Na H
H
 Na
Na KOH
KOH 
 FeCl
FeCl  I
I KCl
KCl  FeCl
FeCl  I
I H
H Fe
Fe SO
SO 





 Cr
Cr
 H
H 
 Cr
Cr
 Fe
Fe 




 KNO
KNO  KOH
KOH  KNO
KNO  K
K




 Cl
Cl H
H PbO
PbO  2Cl
2Cl

 Cu
Cu 
 Cu
Cu 

 0 34 В;
0 34 В; 
 NO
NO 
 NO
NO 
 0 96 В?
0 96 В?

 Fe
Fe
 Fe
Fe 
 0 44 В;
0 44 В; 

 Au
Au
 Au
Au
 1 498 В).
1 498 В). 0,841 В]
0,841 В] 6, содержащейрастворенныйкислород. РассчитайтеЭДС(
6, содержащейрастворенныйкислород. РассчитайтеЭДС( 

 Pd
Pd 
 Pd
Pd 

 0 99 В;
0 99 В; 

 Ag
Ag
 Ag
Ag

 0 8 В).
0 8 В). 0,075 B]
0,075 B]