
- •I. Основные понятия и законы химии
- •II. Строение атома
- •1. Ядерная модель атома. Строение атома. Состав атомных ядер. Массовое число. Атомный номер. Нуклид. Изотопы. Явление радиоактивности. Воздействие радиоактивного излучения на живую материю.
- •III. Периодический закон и периодическая система элементов д.И.Менделеева
- •IV. Химическая связь и строение вещества
- •Поскольку в этой молекуле оба атома кислорода равноценны (и, следовательно, равноценны обе связи s-o), свойства молекулы лучше передает графическая формула с делокализацией π-связью:
- •5. Ионная и металлическая связь. Механизм образования ионной связи. Степень ионности связи. Ионные кристаллические решетки. Координационное число иона.
- •9. Молекулярное и немолекулярное строение веществ. Молекулярные, атомные и ионные соединения. Графические и структурные формулы веществ. Газообразное и конденсированное состояния веществ.
- •V. Химическая кинетика и термодинамика
- •VI. Растворы
- •VII. Окислительно-восстановительные реакции (овр)
- •Электродвижущая сила (эдс) гальванического элемента
- •1. Оценить окислительно-восстановительные свойства веществ.
- •2. Предсказать принципиальную возможность осуществления реакции в
- •4. Выбрать наиболее вероятную реакцию из нескольких возможных.
- •4.Коррозия металлов. Основные виды коррозии металлов. Методы защиты металлов от коррозии.
- •VIII. Комплексные соединения
- •IX. Водород и элементы группы viia
- •Простые вещества
- •Водород
- •Галогены и их соединения
- •Бинарные соединения галогенов
II. Строение атома
1. Ядерная модель атома. Строение атома. Состав атомных ядер. Массовое число. Атомный номер. Нуклид. Изотопы. Явление радиоактивности. Воздействие радиоактивного излучения на живую материю.
1 с. 32-34; 2 с. 55-64; 3 с. 46-53; 4 с. 10-12; 5 с. 32-37; 6 с. 32-37; 8 с. 84-86.
Атом – электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов.
Ядра атомов состоят из протонов и нейтронов, имеющих общее название нуклоны.
Массовое число (А) равно сумме числа протонов и числа нейтронов, содержащихся в ядре данного атома.
Главной характеристикой атома является заряд ядра, определяемый числом протонов, содержащихся в ядре.
Химический элемент – это вид атомных частиц с одинаковым положительным зарядом ядра.
Нуклид
– атомная
частица с определенным значением
атомного номера (протонного числа) и
массового числа.
Например,
![]() - нуклид натрия-23.
- нуклид натрия-23.
Изотопы
– нуклиды
одного и того же химического элемента.
Например,
![]() (протий - Н), .
(протий - Н), .![]() (дейтерий - D),
(дейтерий - D),![]() (тритий - T) - изотопы водорода.
(тритий - T) - изотопы водорода.
Радиоактивность – самопроизвольное превращение неустойчивых атомных ядер в другие ядра, сопровождающееся испусканием различных частиц (α-частиц, β––частиц, β+–позитронов, –нейтрино, ̃–антинейтрино и др.).
Основными типами радиоактивных превращений являются:
α-распад, при котором образуется α-частица, представляющая собой ядро атома гелия -
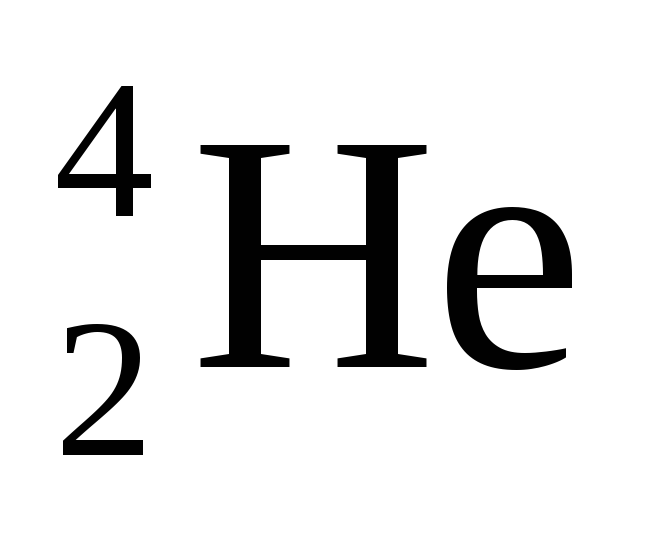 :
: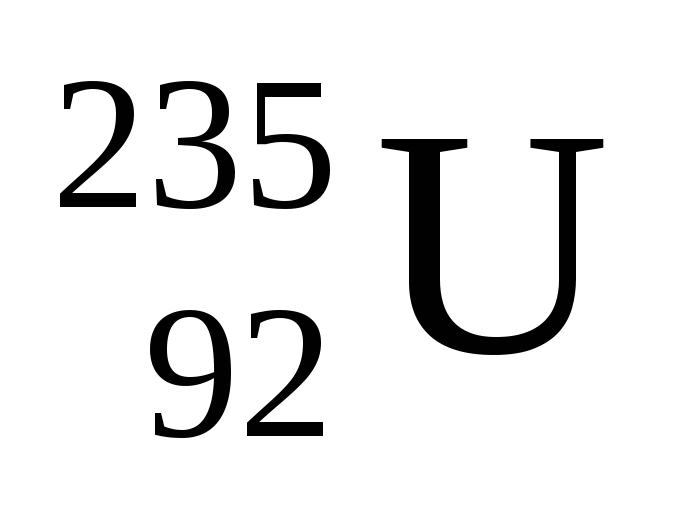 ---->
---->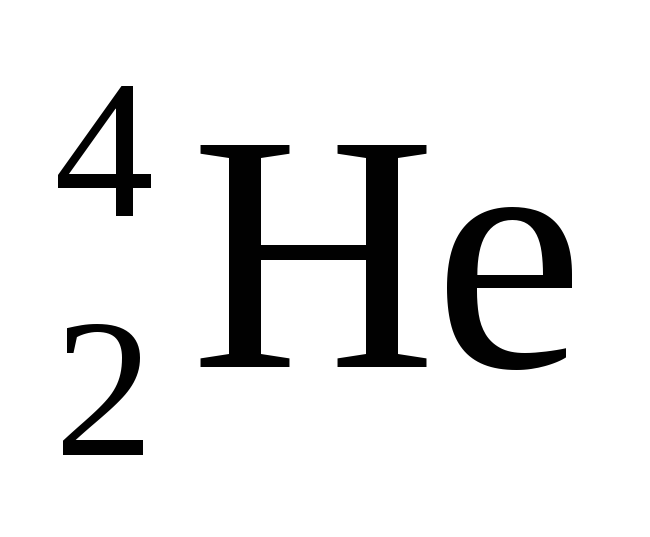 +
+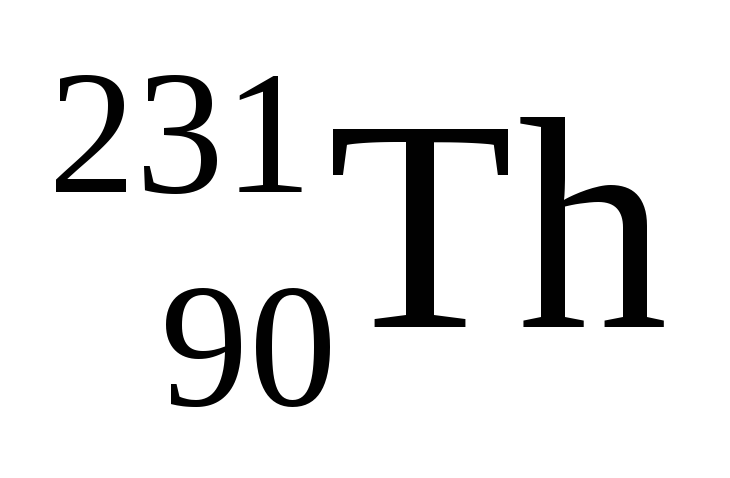 ;
;β-распад (известны три вида такого распада): а) электронный, за счет ядерного процесса превращения нейтрона (
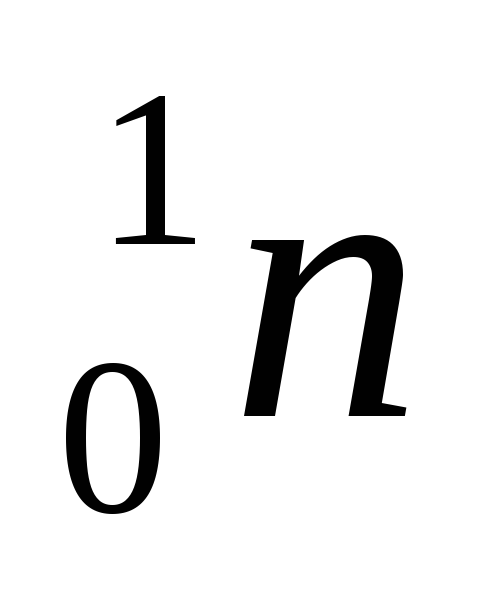 )
в протон (
)
в протон (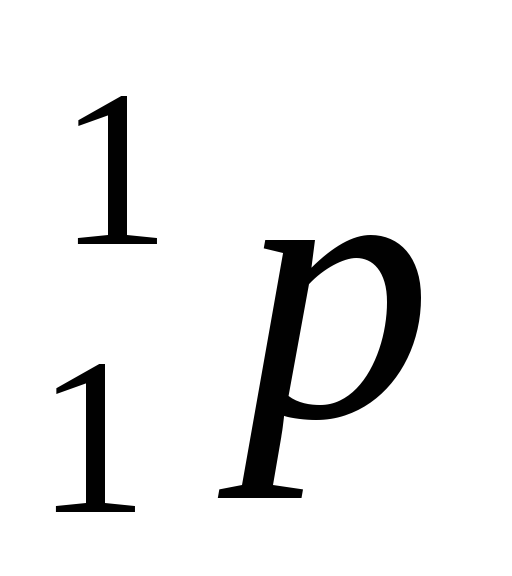 ),
электрон и антинейтрино (̃):
),
электрон и антинейтрино (̃):
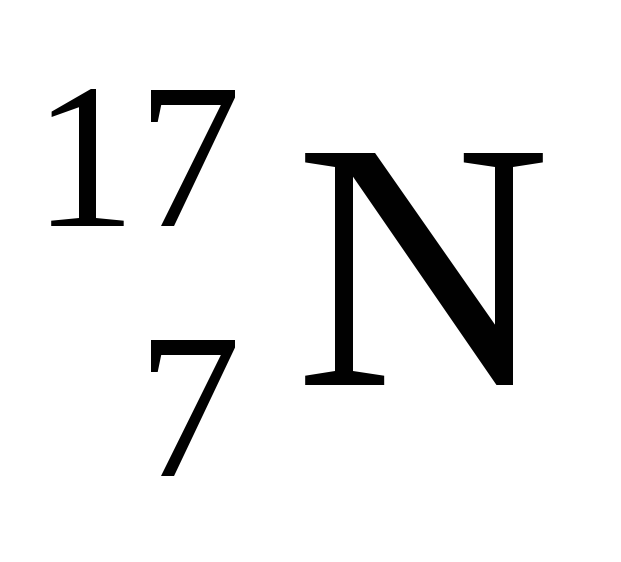 --->
--->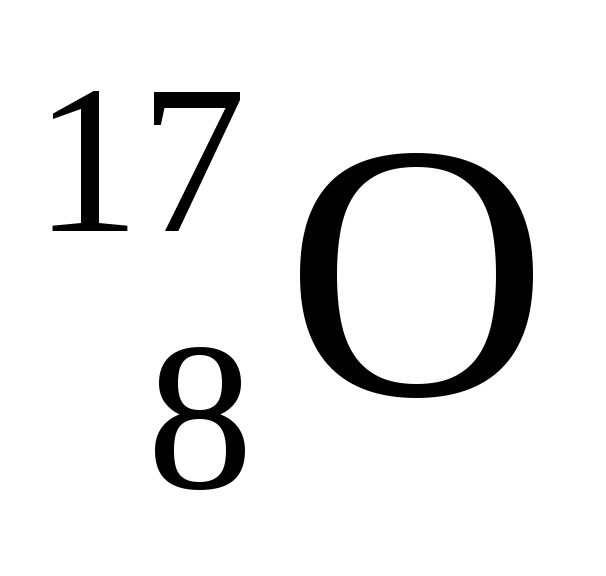 + β–
+ ̃;
б)
позитронный, за счет ядерного процесса
превращения протона (
+ β–
+ ̃;
б)
позитронный, за счет ядерного процесса
превращения протона (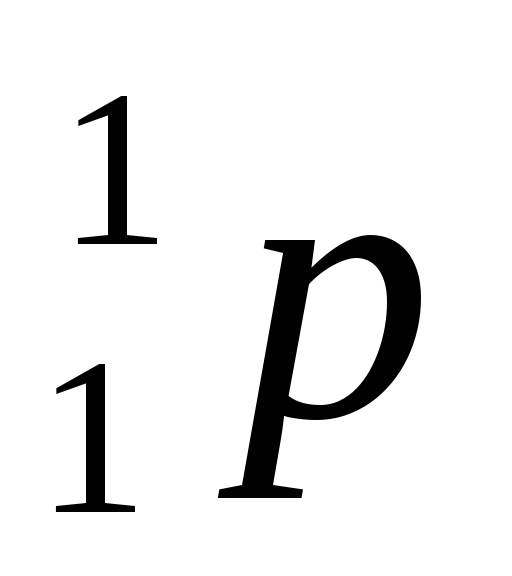 )
в нейтрон (
)
в нейтрон (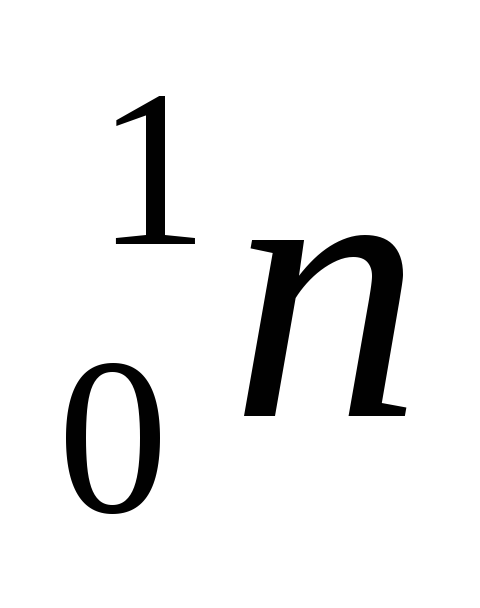 ),
позитрон (β+)
и нейтрино ():
),
позитрон (β+)
и нейтрино ():
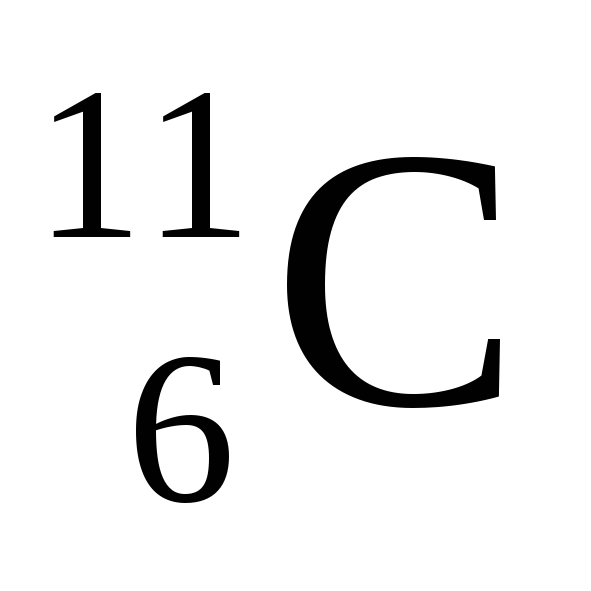 --->
--->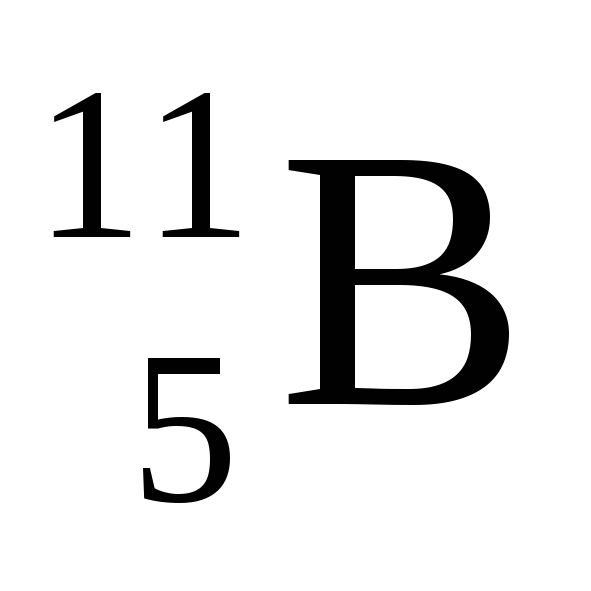 + β+
+ ;
в)
электронный захват, за счет ядерного
процесса захвата протоном (
+ β+
+ ;
в)
электронный захват, за счет ядерного
процесса захвата протоном (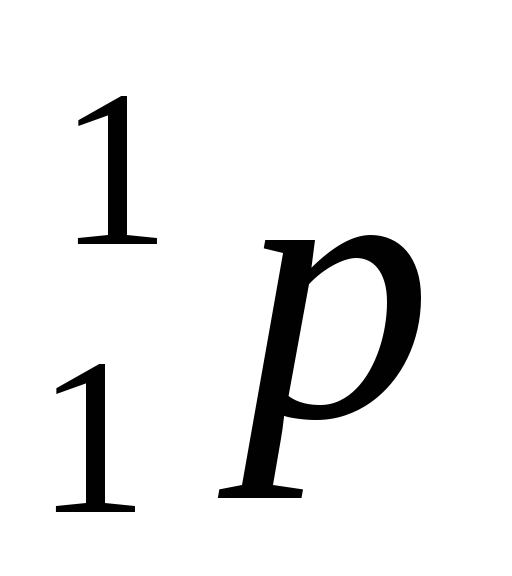 )
ядра электрона (e–)
с электронной оболочки атома с
образованием нейтрона (
)
ядра электрона (e–)
с электронной оболочки атома с
образованием нейтрона (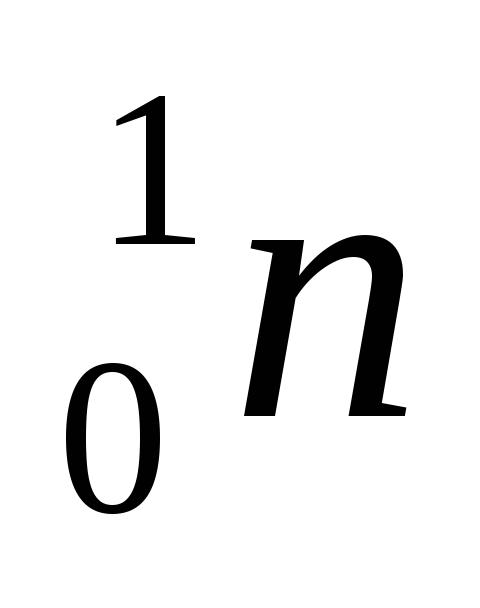 )
и нейтрино ():
)
и нейтрино ():
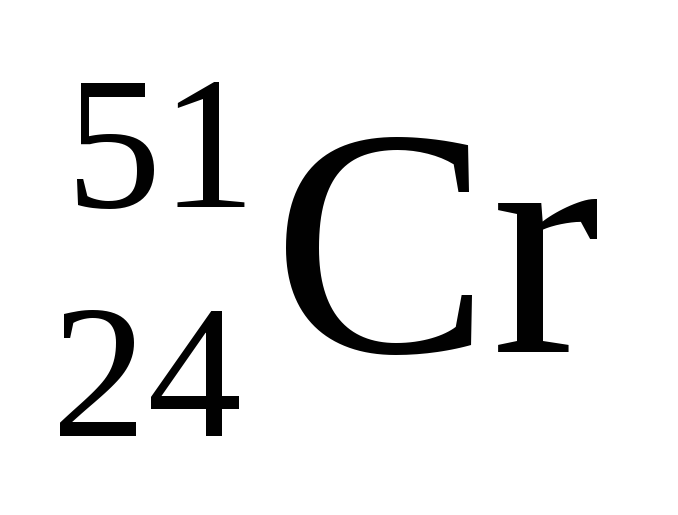 + e–
--->
+ e–
--->
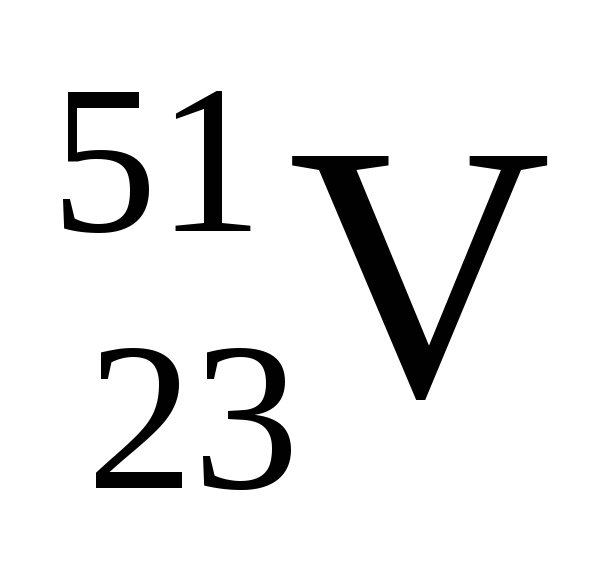 +
+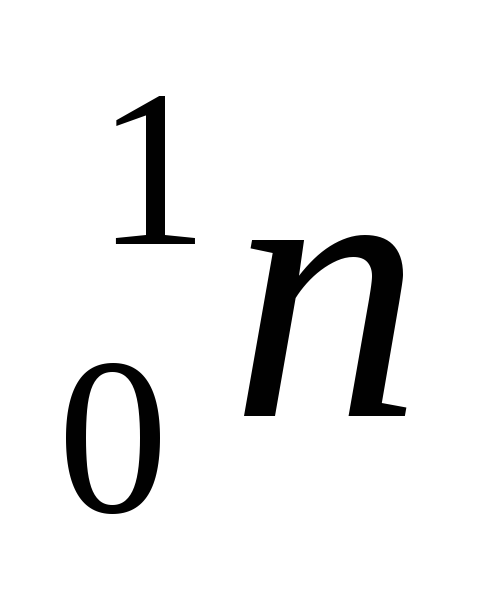 +.
+.
2. Строение электронных оболочек атомов. Волновые свойства материальных частиц. Понятие об электронном облаке. Атомная орбиталь. Электронная плотность. Радиальное распределение электронной плотности около ядра атома водорода.
Квантовые числа как характеристики состояния электрона в атоме. Энергия и форма электронного облака. Ориентация облака. Спин электрона.
1 с. 34-38; 2 с. 64-81; 3 с. 50-59; 4 с. 21-30; 5 с. 37-45; 6 с. 37-45; 8 с. 86-97;
Согласно квантово-механическим представлениям любому материальному объекту присуща двойственность (дуализм) – частица-волна, т.е. объект обладает как корпускулярными свойствами (т.е. свойствами частицы), так волновыми свойствами (т.е. свойствами волнового процесса). Эта двойственность тем сильнее проявляется, чем меньше размеры частиц.
Электрон в атоме можно рассматривать и как частицу, и как волновой процесс.
Принцип неопределенности Гейзенберга – для микрочастиц невозможно сколь угодно точно одновременно определить координаты и импульс. Поэтому для описания движения электрона в атоме используют вероятностный подход (т.е. задают не положение и скорость электрона в каждой точке пространства, а вероятность его обнаружения в этой точке или элементе объема).
Под электронным облаком обычно понимают область околоядерного пространства, в котором вероятность обнаружить электрон составляет 90%. Эту область пространства часто называют орбиталью.
Волновая функция, описывающая поведение электрона в атоме, зависит от ряда параметров, называемых квантовыми числами и принимающих вполне определенные дискретные значения.
Главное квантовое число (n) – определяет основной запас энергии электрона, т.е. степень его удаления от ядра, или размер электронного облака (орбитали). Орбитальное (или побочное, азимутальное) квантовое число (l) – определяет пространственную форму электронного облака. Магнитное квантовое число (ml) – характеризует ориентацию электронного облака в пространстве. Спиновое квантовое число (ms) – характеризует собственный момент количества движения электрона.
3. Понятия: энергетический уровень (слой), электронная оболочка, подуровень (подслой), электронная орбиталь. Взаимное расположение уровней и подуровней (графическое изображение). Понятие об эффективном заряде ядра.
1 с. 36-37; 2 с. 89-93; 3 с. 82; 4 с. 30-38; 8 с. 97-101.
Энергетический уровень (слой, оболочка) – совокупность электронных состояний, имеющих одинаковое значение главного квантового числа n. При n=1 имеем первый энергетический уровень, при n=2 - второй и т.д. Энергетические уровни принято обозначать заглавными буквами K (n=1), L (n=2), M (n=3), N (n=4) и т.д.
Энергетический подуровень (подслой) - совокупность энергетических состояний с заданными значениями главного (n) и орбитального (l) квантовых чисел. Например, 2p подуровень (n = 2, l = 1), 4s подуровень (n = 4, l = 0), 5d подуровень (n = 5, l = 2).
Заполнение электронами начинается с подуровня, имеющего минимальную энергию (1s-подуровень), а затем по мере возрастания энергии подуровня.
Правило Клечковского - электроны размещаются последовательно на орбиталях, характеризуемых возрастанием суммы главного и орбитального квантового чисел (n+l); при одинаковых значениях этой суммы раньше заполняется орбиталь с меньшим значением главного квантового числа (n).
|
Орбиталь |
1s |
2s |
2p |
3s |
3p |
3d |
4s |
4p |
4d |
4f |
5s |
5p |
5d |
5f |
|
Сумма (n+l) |
1 |
2 |
3 |
3 |
4 |
5 |
4 |
5 |
6 |
7 |
5 |
6 |
7 |
8 |
В порядке увеличения энергии подуровни располагаются в следующий ряд: 1s<2s<2p<3s<3p<4s<3d<4p<5s<4d<5p<6s<4f<5d<6p<7s<5f<6d<7p и т.д. Заполнение подуровней электронами осуществляется с самого низшего по энергии, а затем заполняются подуровни в указанной последовательности.
Состояние электрона, характеризующееся набором определенных значений трех квантовых чисел - главного (n), орбитального (l) и магнитного (ml) - называется атомной электронной орбиталью. Орбиталь характеризуется определенной энергией или размерами (определяемой главным квантовым числом), формой или симметрией (определяемой орбитальным квантовым числом) и ориентацией в пространстве (определяемой магнитным квантовым числом). Например, для орбитали 3рх n = 3, l = 1 и ml =–1, для орбитали 4dxy n = 4, l = 2 и ml = –2.
4. Принцип Паули. Правило Хунда. Порядок заполнения электронами орбиталей в атомах периодической системы. Понятие «электронная конфигурация», «структура электронной оболочки», «квантовая ячейка».
1 с. 38-40; 2 с. 83-94; 3 с. 82-96; 4 с. 30-38; 5 с. 45-53; 6 с. 45-53; 8 с. 97-102.
Принцип Паули - в атоме не может быть двух электронов, у которых набор всех четырех квантовых чисел был бы одинаков. Следовательно на одной орбитали может разместиться только два электрона у которых три квантовых числа одинаковы, а четвертое – спиновое – различается.
Максимальное число электронов, которое может разместиться на энергетическом уровне (т.е. максимальная емкость энергетического уровня), имеющем значение главного квантового числа n, равно 2n2. Например, на третьем энергетическом уровне (n = 3) максимально может находиться 2n2= 2·32= 18 электронов, на пятом энергетическом уровне (n=5) максимально может находиться 2n2= 2·52= 50 электронов.
Правило Хунда - в пределах энергетического подуровня электроны заполняют орбитали так, чтобы их суммарный спин был максимальным.
Распределение электронов в атоме, находящемся в основном, т.е. в невозбужденном состоянии, (его электронная конфигурация) определяется зарядом ядра и соответствует принципу минимальной энергии: наиболее устойчивое состояние электрона в атоме соответствует минимально возможному значению его энергии. Это означает, что в пределах одного подуровня электроны сначала заполняют все свободные орбитали, а затем на орбиталь добавляется по второму электрону.
Электронная конфигурация атома записывается в виде формулы, в которой для каждого энергетического подуровня указывается число электронов. Например, электронную конфигурацию атома натрия можно представить следующим образом: 1s22s22p63s1. Из формулы следует, что в атоме натрия на подуровне 1s находится 2 электрона (1s2), на подуровне 2s также два электрона (2s2), на подуровне 2р - 6 электронов (2p6), а на подуровне 3s - 1 электрон (3s1). Всего в атоме натрия содержится (2+2+6+1)=11 электронов.
