
Комплексные соединения 1
.pdf
1
ЛЕКЦИЯ № 7
План лекции:
1.Комплексные (координационные) соединения и их свойства. Типы комплексных соединений.
2.Равновесия в растворах комплексных соединений. Константы устойчивости и нестойкости комплексных соединений, их взаимосвязь.
3.Факторы, влияющие на устойчивость комплексных соединений. Влияние избытка лиганда на процесс комплексообразования.
Комплексные (координационные) соединения и их свойства.
Комплексные (координационные) соединения – это сложные частицы, которые могут самостоятельно существовать как в кристаллическом состоянии, так и в растворе.
Особенностью комплексных соединений является наличие центрального атома и связанных с ним ковалентной связью лигандов.
Центральный атом (комплексообразователь) – положительно заряженный ион ме-
талла (Мz+), имеющий свободные s-, p-, d- или f-орбитали.
Лиганд (L) – нейтральная молекула или отрицательно заряженный анион (ацидолиганд), имеющие неподеленную электронную пару.
При взаимодействии иона-комплексообразователя с лигандом возникает химическая связь, для образования которой лиганд отдает свою неподеленную электронную пару (донор электронов), а металл принимает электроны, предоставляя пустую орбиталь (акцептор электронов):
M 
 + :L ↔ M : L
+ :L ↔ M : L
Такой механизм образования химической связи называют донорно-акцепторным, а химическую связь – донорно-акцепторной или координационной (здесь и далее для краткости и простоты восприятия заряды частиц не указаны). Координационная связь является разновидностью ковалентной связи.
Координационную связь «металл-нейтральный лиганд» принято обозначать стрелкой, направленной от лиганда к металлу (M L, например, Ag NH3), а связь «металлацидолиганд» одинарной чертой (M – L, например, Ag – CN).
Центральный атом может образовывать координационные связи с несколькими лигандами, последовательно присоединяя их (ступенчатое комплексообразование):
M + L ↔ ML
ML + L ↔ ML2
. . . . . . . . . . . . . . .
MLn-1 + L ↔ MLn
При этом число связей, образуемых комплексообразователем с лигандами, называется координационным числом центрального атома. Координационное число (КЧ) может иметь
любые целые значения от 2 до 12, однако, наиболее часто встречающиеся координацион-
ные числа – 2, 4 и 6. Например, [Ag(NH3)2]+ (КЧ = 2), [Cu(NH3)4]2+ (КЧ = 4), [Ni(NH3)6]2+
(КЧ = 6).
Координационное число, как правило, выше степени окисления центрального атома и часто равно удвоенному заряду иона-комплексообразователя, но не всегда (смотри выше приведенные примеры аммиакатов серебра, меди и никеля).
2
Координационное число главным образом определяется электронным строением центрального атома (числом свободных орбиталей, участвующих в комплексообразовании), но иногда зависит и от природы лиганда.
Свободные (вакантные) орбитали центрального атома, участвующие в образовании координационных связей, гибридизированы и гибридные орбитали имеют вполне определенное направление в пространстве, то есть тип гибридизации вакантных орбиталей центрального атома определяет как число координированных лигандов, так и пространственную конфигурацию комплекса.
Заряд ЦА |
Тип гибридизации |
КЧ |
Тип и пространственная |
Примеры |
|||||
(z+) |
(число орбиталей) |
конфигурация комплекса |
|||||||
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
1+ |
sp |
|
(2) |
2 |
ML2 |
[Ag(CN)2]- |
|||
|
(линейная) |
|
|||||||
|
|
|
|
|
|
|
[Cu(NH3)2]+ |
||
|
|
|
|
|
|
|
|
||
|
sp3 |
|
|
(4) |
|
ML4 |
[Cd(NH3)4]2+ |
||
2+ |
|
|
|
|
|
4 |
(тетраэдр) |
[Zn(OH)4]2- |
|
|
|
|
|
|
|
|
|||
|
dsp2 |
|
(4) |
|
ML4 |
[PtCl4]2- |
|||
|
|
|
|
|
|
|
(плоский квадрат) |
[PdBr4]2- |
|
|
|
|
|
|
|
|
|
|
|
2+ |
|
|
|
|
|
|
|
[Fe(CN)6]4- |
|
|
2 |
|
3 |
|
|
ML6 |
|
||
|
|
|
|
|
|||||
3+ |
d |
sp |
|
|
(6) |
6 |
(октаэдр) |
[Fe(CN)6]3- |
|
|
|
|
|
|
|
|
|
|
|
4+ |
|
|
|
|
|
|
|
[PtCl6]2- |
|
|
|
|
|
|
|
|
|
|
|
Из таблицы видно, что для однозарядных ионов металлов в соответствии с sp- гибридизацией характерно координационное число равное двум и линейная конфигурация комплекса; для двузаряженных ионов, в зависимости от типа гибридизации, возможны координационные числа 4 или 6, а сама комплексная частица может иметь форму тетраэдра, октаэдра или плоского квадрата. Комплексы с центральными атомами в более высокой степени окисления (+3 и +4, КЧ = 6), как правило, имеют октаэдрическое строение.
На значение координационного числа центрального атома может оказывать влияние природа лиганда, образующего комплекс. Например, алюминий в большинстве соединений находится в sp3d2-гибридизации, как во фторидном комплексе [AlF6]3-, и проявляет координационное число 6. Однако, с более объѐмными галогенидными ионами (хлоридом, бромидом и иодидом) образует комплексы состава [AlHal4]- с координационным числом центрального атома равным 4, так как в этом случае из-за возникающих стерических (пространственных) затруднений более энергетически стабильной является sp3-гибридное состояние центрального атома.
Вто же время для иона Cr3+, имеющего бόльший размер, чем ион алюминия, стерических затруднеий при комплексообразовании с различными лигандами не возникает и
трехвалентный хром во всех комплексах проявляет координационное число равное 6, соответствующее d2sp3-гибридизации центрального атома.
Всостав лигандов, участвующих в комплексообразовании, входят атомы, обладающие одной или несколькими неподеленными парами электронов. Такие атомы способны образовывать координационную связь и их называют донорными атомами. Типичными донорными атомами являются галогены, азот, сера, кислород, фосфор, мышьяк.

3
Если в состав лиганда входит один донорный атом, то такой лиганд называют монодентатным, если больше – полидентатным (би-, три-, тетра-, пентадентатными и т.д.).
Кмонодентатным лигандам относят анионы одноосновных кислот (ацидолиганды)
–F-, Cl-, Br-, I-, CN-, SCN-, NO2- и др., гидроксильный ион ОН-, нейтральные молекулы, имеющие только один донорный атом – аммиак NH3 и органические амины (алифатические – RNH2, R2NH, R3N, гетероциклические – пиридин С5Н5N и т.п.), Н2О, Н2S и органические сульфиды, РН3, P(C6H5)3 и др. Эти лиганды образуют обычно только одну координационную связь (за исключением случаев образования мостиковых связей между двумя атомами металла).
Бидентатные лиганды имеют в своѐм составе два донорных атома, способных к образованию координационной связи. Примерами бидентатных лигандов являются:
NH2 – CH2 – CH2 – NH2 - этилендиамин En (два донорных атомов азота)
NH2 – CH2 – COOH - аминоуксусная кислота (глицин) GlyH (один донорный атом азота аминогруппы и один донорный атом кислорода карбоксильной группы)
Для тридентатных лигандов характерно наличие в их составе трех донорных ато-
мов:
NH2 – CH2 – CH2 – NH – CH2 – CH2 – NH2 - диэтилентриамин dien (три атома азота)
Среди множества полидентатных лигандов большое значение для аналитической химии имеет гексадентатный лиганд – этилендиаминтетрауксусная кислота (ЭДТУК, ЭДТА, EDTA), который способен координироваться через два атома азота и четыре атома кислорода каждой из карбоксильных групп:
HOOC – CH2 |
CH2 |
– COOH |
|
N – CH2 – CH2 – N |
|
HOOC – CH2 |
CH2 |
– COOH |
Этот лиганд, дигидрат динатриевой соли которого известен под названием торговой марки «Трилон Б», образует очень прочные комплексы с катионами многих металлов, что позволяет его использовать для количественного определения металлов методом комплексонометрического титрования.
Таким образом, каждый лиганд характеризуется дентатностью, то есть наличием донорных атомов, способных к образованию координационных связей (максимальная дентатность). Однако, полидентатные лиганды не всегда реализуют свою максимальную дентатность при образовании комплексного соединения и при этом образуют меньшее число связей, чем это возможно. Например, потенциально бидентатная аминоуксусная кислота (глицин, GlyH) в комплексе [CoEn2(GlyH)Cl]Cl2 образует только одну координационную связь с кобальтом через атом азота аминогруппы, проявляя себя как монодентатный лиганд. Нагревание комплекса приводит к отщеплению HCl и образованию нового комплексного соединения [CoEn2(Gly)]Cl2, в котором глицин бидентатно связан с кобальтом через атом азота аминогруппы и атом кислорода депротонированной карбоксильной группы.
В то же время казалось бы сугубо монодентатный хлорид-ион может быть бидентатным, осуществляя одновременно связь с двумя атомами комплексообразователя находясь между ними в виде мостика ( M – Cl – M ).
4
Поэтому реально для каждого лиганда под термином «дентатность» понимают число координационных связей, которые этот лиганд образует с центральным атомом в данном комплексе.
Типы комплексных соединений.
Ион металла-комплексообразователя и окружающие его лиганды образуют внутреннюю сферу комплекса. Эта внутренняя сфера обычно при написании формулы комплексного соединения заключается в квадратные скобки – [MLn]z. Если внутренняя сфера комплекса заряжена, то для компенсации этого заряда необходимы ионы, образующие внешнюю сферу. Внешнесферные ионы записываются за квадратными скобками; они связаны с комплексной частицей ионной связью и в водном растворе диссоциируют по типу сильного электролита, то есть нацело (α = 1).
Например, в комплексных соединениях K2[PtCl4] и [Pt(NH3)4]Cl2 внутреннюю сферу составляют комплексные частицы [PtCl4]2- и [Pt(NH3)4]2+, а внешнюю сферу ионы K+ и Cl- соответственно.
В зависимости от заряда внутренней сферы комплексы могут быть неэлектролит-
ными, катионными и анионными.
Для неэлектролитных комплексов заряд внутренней сферы равен нулю (z = 0) и у них отсутствует внешняя сфера, например:
[Pt(NH3)2Cl2]0, [Co(NH3)3Br3]0
Заряд внутренней сферы катионных комплексов положительный (z+) и в их внешней сфере находятся анионы, например:
[Cu(NH3)4]Cl2 → [Cu(NH3)4]2+ + 2Cl-
[Pt(NH3)3Cl]Cl → [Pt(NH3)3Cl]+ + Cl-
Внутренняя сфера комплексов анионного типа несет отрицательный заряд (z-), а их внешняя сфера содержит катионы, например:
Na3[Co(NO2)6] → 3Na+ + [Co(NO2)6]3-
K[PtNH3Cl3] → K+ + [PtNH3Cl3]-
Если во внутренней сфере комплекса содержатся лиганды одного типа, то такие комплексы называются однолигандными, если лиганды разного типа – смешаннолиганд-
ными.
Примерами однолигандных комплексов служат аммиакаты – [Cu(NH3)4]Сl2, [Ag(NH3)2]Br, аквокомплексы – [Co(H2O)6]Сl3, [Cr(H2O)6]Br3, гидроксокомплексы – K3[Cr(OН)6], Na[Al(OH)4], ацидокомплексы – (NH4)3[FeF6], K2[HgCl4]
Смешаннолигандными являются – [Pt(NH3)2Cl2], Na2[Fe(CN)5NO].
Взависимости от числа центральных атомов, входящих в состав комплексной частицы, различают моноядерные и полиядерные комплексы.
Всостав моноядерного комплекса входит один центральный атом, вокруг которого могут располагаться как монодентатные, так и полидентатные лиганды. Примерами моноядерных комплексов являются все выше упомянутые соединения.
Для полиядерных комплексов характерно наличие двух и более центральных атомов, связанных между собой мостиковыми полидентатными лигандами (биядерные, триядерные, тетраядерные и т.д.).
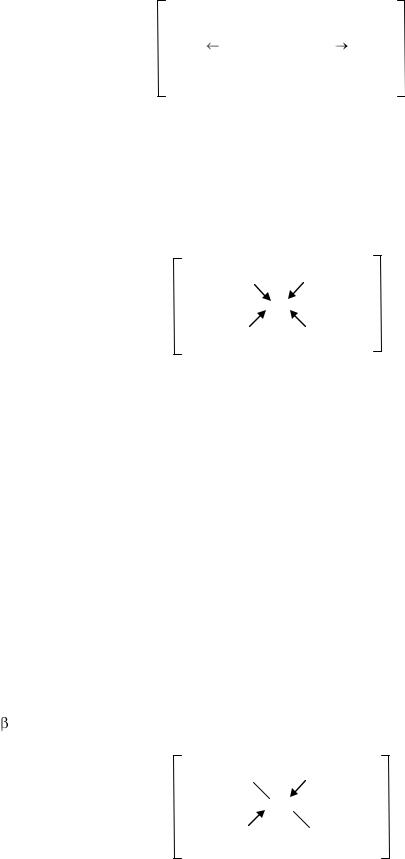
5
Например: |
2- |
Cl |
Cl |
| |
| |
Cl – Pt NH2 – (CH2)2 – NH2 |
Pt – Cl |
| |
| |
Cl |
Cl |
В этом биядерном комплексе два центральных атома платины связаны между собой мостиковым бидентатным этилендиамином.
Особое место среди комплексных соединений занимают хелаты. Это комплексы, в которых полидентатные лиганды образуют с центральным атомом хелатные (клешневидные) циклы (от англ. chelate – клешня). Хелатные комплексы образует, например, бидентатный этилендиамин (En):
2+
CH2 |
– NH2 |
NH2 |
– CH2 |
||
|
|
|
Pt |
|
|
|
|
|
|
|
|
CH2 |
– NH2 |
NH2 |
– CH2 |
||
В этом комплексе молекулы этилендиамина образуют два пятичленных хелатных цикла, каждый из которых включает атом платины и по два атома азота и углерода лиганда.
Поскольку в состав хелатных циклов входит атом металла, то их также называют
металлоциклами.
Образование хелатных циклов приводит к повышению устойчивости комплексных соединений, по сравнению с комплексами тех же металлов с монодентатными лигандами, образующими аналогичные координационные связи, например, указанный хелатный комплекс платины с этилендиамином [PtEn2]2+ значительно более устойчив, чем [Pt(NH3)4]2+.
Наибольшей устойчивостью обладают пяти- и шестичленные металлоциклы (правило циклов Чугаева). Соединения с трех-, четырехчленными циклами и с числом звеньев больше семи образуются редко из-за их малой устойчивости. Стабильность хелатных комплексов возрастает с увеличением числа металлоциклов в комплексе.
Особое значение в аналитической химии имеют неэлектролитные хелатные комплексы с полидентатными органическими лигандами, которые называют внутрикомплексными соединениями (ВКС). Образующие внутрикомплексные соединения полидентатные лиганды обладают как нейтральными, так и отрицательно заряженными (анионными) электронодонорными группами.
Примером внутрикомплексного соединения может служить хелатный комплекс меди(II) с -аминопропионовой кислотой:
0
CH2 |
– СОО |
NH2 – CH2 |
||
|
|
|
Cu |
|
|
|
|
|
|
CH2 |
– NH2 |
ООС – CH2 |
||
Наличие во внутренней сфере внутрикомплексных соединений хелатных циклов определяет высокую устойчивость ВКС, что предопределяет их широкое использование в химическом анализе для прочного связывания мешающих ионов (маскировка) и при комплексонометрическом титровании.
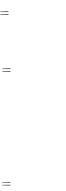
6
Поскольку внутрикомплексные соединения являются неэлектролитами, то они часто плохо растворимы в воде, что используется для выделения ионов металлов из раствора с целью их отделения или гравиметрического (весового) определения. В то же время внутрикомплексные соединения хорошо растворимы в органических растворителях, в том числе не смешивающихся с водой, что позволяет на их основе разрабатывать экстракционные процессы для разделения, очистки и концентрирования отдельных элементов.
Яркая окраска многих внутрикомплексных соединений позволяет использовать реакции их образования для обнаружения катионов металлов в анализируемом растворе. Примеры таких реакций будут приведены далее в разделе, посвященном применению комплексных соединений в качественном химическом анализе.
Равновесия в растворах комплексных соединений. Константы устойчивости и нестойкости комплексных соединений, их взаимосвязь.
При смешивании растворов, содержащих ион металла М и лиганд L (заряды для простоты опущены), происходит процесс последовательного присоединения лиганда к металлу, то есть происходит ступенчатое комплексообразование:
M + L ↔ ML
ML + L ↔ ML2
. . . . . . . . . . . . . . .
MLn-1 + L ↔ MLn
K1 |
|
[ML] |
||
|
|
|
||
[M][L] |
||||
|
||||
K2 |
|
[ML2 ] |
||
[ML][L] |
||||
|
||||
. . . . . . . . . . . . . .
Kn |
[MLn ] |
||
[MLn-1 |
][L] |
||
|
|||
При этом для каждой ступени устанавливается химическое равновесие, которое характеризуется соответствующей константой равновесия. Константы K1, K2 . . . Kn называ-
ют ступенчатыми константами устойчивости (образования) комплексов. Индекс кон-
станты указывает на ступень комплексообразования и соответствует порядковому номеру присоединяемого лиганда, например, K1 и K2 это первая и вторая константы устойчивости, которые характеризуют присоединение первого и второго лиганда. Как правило, каждая последующая ступенчатая константа устойчивости меньше предыдущей: K1 > K2 > . . .
> Kn (хотя встречаются и исключения, когда Ki+1 > Ki).
Приведенные здесь и далее выражения представляют собой концентрационные константы устойчивости, то есть константы, выраженные через равновесные концентрации частиц. Значения концентрационных констант зависят от природы реагентов, растворителя, температуры и ионной силы раствора. В справочниках, чаще всего, приведены значения термодинамических констант устойчивости, выраженных через активности и не зависящих от ионной силы раствора. Однако, в разбавленных растворах, где коэффициенты активности стремятся к единице, концентрационная и термодинамическая константы совпадают.
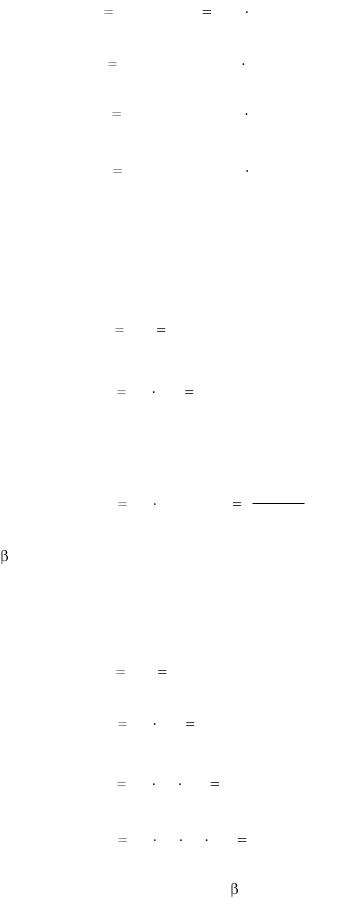
7
Например, при смешивании растворов, содержащих ионы Hg2+ и I-, происходит ступенчатое комплексообразование:
Hg2+ + I- |
↔ [HgI]+ |
|
|
K |
|
|
|
|
[HgI+ ] |
|
7,4 1012 |
|||||||||
|
|
|
|
|
|
|
|
|
|
[Hg2+ ][I- ] |
||||||||||
|
|
|
|
|
|
|
|
|
1 |
|
|
|||||||||
|
+ |
|
|
- |
|
0 |
|
|
|
|
|
[HgI2 ] |
10 |
|||||||
[HgI] |
|
|
+ I |
↔ [HgI2] |
|
|
K2 |
|
|
|
|
|
|
|
|
|
|
= 8,9 10 |
||
|
|
|
|
|
|
[HgI+ ][I- ] |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
0 |
|
- |
|
|
- |
|
|
|
|
|
[HgI3- ] |
3 |
||||||
[HgI2] |
|
|
+ I |
↔ [HgI3] |
|
K |
3 |
|
|
|
|
|
|
|
|
|
= 6,0 10 |
|||
|
|
|
|
|
[HgI |
2 |
][I- ] |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
[HgI3]- + I- |
↔ [HgI4]2- |
K |
|
|
|
|
[HgI42- ] |
|
= 1,7 102 |
|||||||||||
4 |
|
|
|
[HgI- |
][I- ] |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
Процесс комплексообразования можно представить в виде суммарных равновесий, объединяющих несколько ступеней и характеризующихся суммарными ( кумулятивными) константами устойчивости, которые являются произведением соответствующих ступенчатых констант:
M + L ↔ ML
M + 2L ↔ ML2
. . . . . . . . . . . .
M + nL ↔ MLn
β |
K |
[ML] |
||
|
|
|
||
|
|
|
||
1 |
1 |
[M][L] |
||
|
|
|||
β2 |
K1 K2 |
|
[ML2 ] |
|
[M][L]2 |
||||
. . . . . . . . . . . . . . . . . . . . . .
βn K1 K2 . . . Kn [MLn ]n
[M][L]
Суммарную константу
вости (образования).
Суммарные равновесия комплексообразования при взаимодействии ионов Hg2+ и I- и соответствующие им суммарные константы устойчивости выглядят следующим образом:
2+ |
- |
|
+ |
|
|
|
|
[HgI+ ] |
|
|
|
|
|
|
||
Hg |
+ I ↔ [HgI] |
|
|
β |
K |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
1 |
|
[Hg2+ ][I- ] |
|
|
|
|
|
|
||
2+ |
- |
|
|
0 |
|
|
|
|
[HgI2 ] |
|||||||
Hg |
+ 2I |
↔ [HgI2] |
|
β2 |
K1 |
K2 |
|
|
|
|
|
|
|
|
|
|
|
[Hg |
2+ |
|
- 2 |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
][I ] |
|||||||
Hg2+ |
+ 3I- |
↔ [HgI3]- |
β3 |
K1 |
K2 K3 |
|
|
[HgI3- ] |
|
|||||||
|
|
|
|
|
[Hg2+ ][I- ]3 |
|||||||||||
Hg2+ + 4I- |
↔ [HgI4]2- |
β4 |
K1 K2 K3 K4 |
|
|
|
[HgI42- ] |
|
||||||||
|
|
|
|
|
|
|
[Hg2+ ][I- ]4 |
|||||||||
Для комплексного иона [HgI4]2- константа устойчивости |
4 |
является общей. |
||||||||||||||

8
Константа устойчивости служит количественной характеристикой прочности ком-
плексного соединения в растворе – чем больше константа устойчивости, тем прочнее комплекс и тем полнее связаны (закомплексованы) ионы металла.
Константы устойчивости комплексов часто имеют очень высокие числовые значения, поэтому обычно в справочниках приводят не сами значения констант, а их десятичные логарифмы lg n .
Например, в справочнике по аналитической химии для процесса комплексообразования ионов Hg2+ и I- приведены следующие значения логарифмов суммарных констант устойчивости:
Ион металла |
|
Лиганд |
|
lg 1 |
|
lg |
2 |
|
|
lg 3 |
|
lg 4 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Hg2+ |
|
|
|
I- |
|
|
12,87 |
|
23,82 |
|
|
27,60 |
|
29,83 |
||
|
|
|
|
|
|
|||||||||||
По этим данным можно рассчитать значения суммарных и ступенчатых констант ус- |
||||||||||||||||
тойчивости для комплексного иона [HgI4]2-: |
|
|
|
|
|
|
|
|||||||||
lg |
1 |
= 12,87 |
K1 |
= 1 = 1012,87 = 7,4 1012 |
|
|
|
|
|
|
||||||
lg |
2 |
= 23,82 |
2 |
= 1023,82 = 6,6 1023 |
|
|
|
|
|
|
|
|||||
lgK2 = lg |
2 – lg |
1 |
|
= 23,82 – 12,87 = |
10,95 |
K2 |
= 1010,95 = 8,9 1010 |
|
||||||||
lg |
3 |
= 27,60 |
3 |
= 1027,60 = 4,0 1027 |
|
|
|
|
|
|
|
|||||
lgK3 = lg |
3 – lg |
2 |
|
= 27,60 – 23,82 = |
3,78 |
K3 |
= 103,78 |
= 6,0 103 |
|
|
||||||
lg |
4 |
= 29,83 |
4 |
= 1029,83 = 6,8 1029 |
|
|
|
|
|
|
|
|||||
lgK4 = lg |
4 – lg |
3 |
|
= 29,83 – 27,60 = |
2,23 |
K4 |
= 102,23 |
= 1,7 102 |
|
|
||||||
Прочность комплексных соединений можно характеризовать также с помощью констант нестойкости, которые соответствуют процессу диссоциации комплексной частицы в растворе.
Диссоциация комплекса является процессом обратным его образованию и также протекает ступенчато:
MLn ↔ MLn-1 + L
MLn-1 ↔ MLn-2 + L
. . . . . . . . . . . .
ML ↔ M + L
Kн1 |
[MLn 1 ][L] |
1 |
|
|||||||||
|
|
|
[MLn ] |
|
|
|
|
Kn |
|
|||
|
|
|
|
|
|
|
|
|||||
Kн2 |
|
[MLn 2 ][L] |
1 |
|||||||||
|
|
|
[MLn 1 |
] |
|
|
|
|
Kn 1 |
|||
|
|
|
|
|
|
|
|
|||||
|
. . . . . . . . . . . . |
|
|
|
||||||||
Kнn |
|
|
[M][L] |
|
|
1 |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
[ML] |
|
|
|
K1 |
|||||
|
|
|
|
|
|
|
||||||

9
При этом для каждой ступени устанавливается химическое равновесие, которое характеризуется соответствующей константой равновесия. Константы Kн1, Kн2 . . . Kнn назы-
вают ступенчатыми константами нестойкости (неустойчивости) комплексов. Индекс константы указывает на ступень диссоциации и соответствует порядковому номеру отщепляемого лиганда, например, Kн1 и Kн2 это первая и вторая константы нестойкости, которые характеризуют отщепление первого и второго лиганда.
Очевидно, что каждая ступенчатая константа нестойкости является величиной, обратной соответствующей ступенчатой константе устойчивости, поэтому каждая последующая ступенчатая константа нестойкости меньше предыдущей: Kн1 > Kн2 > . . . > Kнn.
Например, ступенчатая диссоциация комплекса [HgI4]2- в водном растворе происходит следующим образом:
[HgI4]2- |
↔ [HgI3]- |
+ |
I- |
K |
|
[HgI3- ][I- ] |
|
|
|
1 |
|
|
5,9 10-3 |
||||||||||
н1 |
|
|
[HgI2- ] |
K |
4 |
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
||||
[HgI3]- |
|
↔ [HgI2]0 |
+ |
I- |
K |
|
|
[HgI2 ][I- ] |
|
|
|
1 |
|
1,7 10-4 |
|||||||||
|
н2 |
|
|
[HgI- ] |
|
K |
3 |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|||
[HgI2]0 |
|
↔ [HgI]+ |
+ |
I- |
K |
|
[HgI+ ][I- ] |
1 |
|
|
1,1 10-11 |
||||||||||||
|
н3 |
|
|
[HgI2 ] |
|
|
K2 |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
[HgI] |
+ |
|
2+ |
- |
|
|
|
|
[Hg2+ ][I- ] |
1 |
|
|
|
|
-13 |
||||||||
|
↔ Hg + I |
|
Kн4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1,4 10 |
|||||
|
|
|
|
|
|
|
|
[HgI+ ] |
|
|
K |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
Процесс диссоциации комплекса можно представить в виде суммарных равновесий, объединяющих несколько ступеней и характеризующихся суммарными ( кумулятивными) константами нестойкости, которые являются произведением соответствующих ступенчатых констант:
MLn ↔ MLn-1 + L
MLn ↔ MLn-2 + 2L
. . . . . . . . . . . .
MLn ↔ M + nL
βн1 = Kн1 |
= |
[MLn 1 ][L] |
||
|
[MLn |
] |
||
|
|
|
||
βн2 |
Kн1 |
Kн2 |
[MLn 2 ][L]2 |
1 |
||
[MLn |
] |
|
Kn Kn 1 |
|||
|
|
|
|
|||
. . . . . . . . . . . . . . . . .
βнn |
Kн1 |
Kн2 |
. . . Kнn |
[M][L]n |
1 |
||
[MLn |
] |
|
Kn Kn 1 . . . K1 |
||||
|
|
|
|
|
|||
Суммарную константу нn для комплекса MLn называют общей константой нестойкости ( неустойчивости). Очевидно, что общая константа нестойкости есть величина, обратная общей константе устойчивости:
1
βнn βn
Суммарные равновесия при диссоциации комплексного иона [HgI4]2- и соответствующие им суммарные константы нестойкости выглядят следующим образом:

|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
10 |
|
2- |
|
|
- |
- |
|
|
|
|
|
|
[HgI3- ][I- ] |
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
[HgI4] |
|
↔ [HgI3] |
|
+ I |
βн1 |
Kн1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
[HgI42- ] |
|
|
K4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
2- |
|
|
0 |
- |
βн2 |
Kн1 |
Kн2 |
|
[HgI2 ][I- ]2 |
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
[HgI4] |
|
↔ [HgI2] |
|
+ 2I |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
[HgI |
2- |
] |
|
|
|
|
|
|
|
K |
|
K |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
4 |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
[HgI4]2- |
↔ [HgI]+ |
|
+ 3I- |
βн3 |
Kн1 |
Kн2 |
Kн3 |
|
|
[HgI+ ][I- ]3 |
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
[HgI |
2- |
] |
|
|
|
|
K |
|
K |
|
|
K |
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
4 |
3 |
|
2 |
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
[HgI4]2- |
↔ Hg2+ |
+ 4I- |
β |
|
K |
|
K |
|
K |
|
|
K |
|
|
|
|
|
[Hg2+ ][I- ]4 |
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|||||||||||
н4 |
н1 |
н2 |
н3 |
н4 |
|
|
|
|
|
[HgI2- ] |
|
|
|
|
|
|
K |
4 |
K |
3 |
K |
2 |
K |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|||||
Для комплексного иона [HgI4]2- константа н4 |
является общей константой нестойко- |
|||||||||||||||||||||||||||||||||||||||||||
сти.
Константа нестойкости, как и константа устойчивости, служит количественной характеристикой устойчивости комплексного соединения в растворе – чем меньше кон-
станта устойчивости, тем прочнее комплекс и тем полнее связаны (закомплексованы)
ионы металла.
Константы нестойкости комплексов часто имеют очень низкие числовые значения, поэтому обычно приводят не сами значения констант, а их показатели p нn = -lg нn .
Так как константы устойчивости и нестойкости являются величинами обратными друг другу, то численные значения показателя константы нестойкости и логарифма константы устойчивости для данной комплексной частицы совпадают.
Знание констант устойчивости (или нестойкости) позволяет рассчитывать равновесные концентрации частиц в растворах комплексных соединений. Особое значение при этом имеет определение концентрации свободных ( незакомплексованных) ионов металла, для чего используют уравнение суммарного равновесия комплексной частицы MLn в растворе:
MLn ↔ M + nL
Это равновесие характеризуется общей константой устойчивости:
β |
|
[MLn ] |
|
n |
[M][L]n |
||
|
Если исходная концентрация комплекса в растворе Ск, а равновесную концентрацию ионов металла [M] обозначим через х, то [L] = nx и [MLn] = Ск - x ≈ Ск (x << Ск). Тогда:
β |
|
[MLn ] |
|
(Cк x) |
|
Cк |
n |
[M][L]n |
|
x (nx)n |
|
nn xn 1 |
|
|
|
|
Откуда:
x [M] |
n 1 |
|
Cк |
|
|
nn β |
n |
|
|||
|
|
|
|
||
|
|
|
|
|
