
Комплексные соединения
.pdfМинистерство здравоохранения Российской Федерации
Государственное бюджетное образовательное учреждение высшего профессионального образования
МОСКОВСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИКОСТОМАТОЛОГИЧЕСКИЙ УНИВЕРСИТЕТ
им. А.И.Евдокимова
КАФЕДРА ОБЩЕЙ И БИООРГАНИЧЕСКОЙ ХИМИИ
Лекция № 12
КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ.
Продолжительность – 1 академический час
Составитель:
профессор А.А.Прокопов
МОСКВА
2013
2
Комплексные (координационные) соединения составляют
обширную группу веществ высшего порядка неорганического и органического происхождения. Они обеспечивают жизнь: гемоглобин
– комплексное соединение железа – переносит кислород из лёгких в
ткани, хлорофилл – комплексное соединение магния – отвечает за фотосинтез в растениях, витамин В12 – комплексное соединение кобальта и т.д.
Свойства и строение комплексных соединений объясняет
координационная теория Вернера (1893 г., Швейцария).
Комплексное соединение – это вещество, в узлах
кристаллической решётки которого находятся сложные частицы
(комплексные ионы или молекулы), построенные за счёт координации
одним атомом обычных молекул и ионов; эти частицы способны существовать и при переходе вещества в растворённое или
расплавленное состояние.
Комплексное соединение, как правило, состоит из двух сфер –
внутренней и внешней.
Комплексный ион (или внутренняя сфера комплексного
соединения) – частица, |
состоящая из |
комплексообразователя |
– обычно иона d- или |
f- металла в определённой степени |
|
3
окисления, и окружающих его лигандов - противоположно
заряженных ионов или нейтральных молекул.
II
К4[PtCl6] гексахлороплатинат (II) калия
I
[Ag(NH3)2]Cl хлорид диамминсеребра (I)
Комплексный ион сохраняет в значительной степени
стабильность при растворении, его границы показывают квадратными
скобками.
Заряд внутренней сферы равен алгебраической сумме зарядов
комплексообразователя и лигандов:
III |
|
|
[Fe(CN)6]x |
+3 + 6(-1) = x |
x = -3 |
Если известен заряд |
внутренней сферы и |
лигандов, легко |
определить заряд комплексообразователя:
x |
|
|
[Pt(NH3)4Cl2]+2 |
x + 4·0 + 2(-1) = +2 |
x = +4 |
Ионы, не разместившиеся во внутренней сфере, более удалены от центрального атома, они составляют внешнюю сферу.
Связь внутренней сферы с внешней ионогенная, она легко расщепляется в водном растворе, – т.е. это диссоциация сильного электролита:

|
4 |
[Cu(NH3)4 SO4 |
[Cu(NH3)4]2+ + SO42- |
Ковалентная связь между комплексообразователем и лигандами
значительно прочнее, она имеет донорно-акцепторное происхождение.
Донор электронной пары – лиганд.
|
|
|
|
|
|
7N - 1s22s22p3 |
|
|
|
s |
|
|
|
|
|
|
|
|
|
|
|
|
|
I |
|
↑↓ |
|
|
p |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
||
II |
↑↓ |
|
↑ |
↑ |
↑ |
|
|
|
|
|
|
|
|
|
Валентность азота 3, |
|
Молекула аммиака: |
|
|||||
|
|
|
|||||
|
|
|
|
|
|
|
Н |
|
:NH3 |
|
|
или |
|
N:H |
|
|
|
|
|
|
|
|
Н |
Aтом азота в состоянии sp3-гибридизации.
Акцептор электронной пары – комплексообразователь Cu2+:
|
|
29Cu - 1s22s22p63s23p64s13d10 |
|
|
|
Cu |
- 2e Cu2+ |
|
|
29Cu2+ - 1s22s22p63s23p64s03d9 |
|
s |
p |
d |
f |
IV
с в о б о д н ы е |
о р б и т а л и |
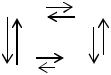
5
|
|
|
|
|
|
NH3 |
|
Четыре |
равноценные |
||
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
||
H3N |
|
Cu2+ |
|
NH3 |
двухэлектронные -связи |
||||||
|
|
||||||||||
|
|
|
|
NH3 |
|
Cu2+ ----- N |
|
||||
|
|
|
|
|
|||||||
Общее |
число |
связей, |
существующих |
между |
|||||||
комплексообразователем и лигандами, называется координационным
числом комплексообразователя (кч).
Координационное число зависит:
1. От заряда (степени окисления) комплексообразователя
Степень окисления |
Координационное число |
Пример |
комплексообразователя |
комплексообразователя |
|
+1 |
2 |
[Ag(NH3)2]Cl |
|
|
|
+2 |
4, 6 |
[Zn(NH)3)4]SO4, K4[Fe(CN)6] |
|
|
|
+3 |
4, 6 |
[Co(H2О)6]Cl3 |
|
|
|
2. От размеров комплексообразователя и лигандов:
- чем больше радиус комплексообразователя, тем больше его
координационное число
[BF4]¯ к.ч. = 4 |
[AlF6]3- к.ч. = 6. |
- чем меньше размер лиганда, тем больше к.ч. комплексообразователя:
[AlF6]3- к.ч.= 6 |
[AlCl4]¯ |
к.ч. = 4 |

6
3.От концентрации растворов, в которых идёт комплексообразование.
4.От температуры: повышение температуры, как правило,
приводит к понижению координационного числа.
Типы лигандов.
Лиганды, которые образуют только одну связь с комплексообразователем, - это монодентатные лиганды (однозубые):
NH3, Н2О, CN-, NO2-, Cl-, СО и т.д.
Бидентатные |
лиганды |
способны |
образовывать |
с |
комплексообразователем две связи:
оксалат-ион ¯СОО-СОО¯, СО32– , SO42– ,
1,2-диаминоэтан Н2N-CH2-CH2-NH2.
Полидентатные лиганды (многозубые) могут образовывать более
двух связей с комплексообразователем:
ЭДТА (этилендиаминтетраацетат)
¯ООСН2С |
СН2СОО¯ |
N – CH2 – CH2 – N |
|
¯ООСН2С |
СН2СОО¯ |
Координационные числа разных комплексообразователей имеют |
|
значения от 2 до 10, причём, К.Ч. |
4 и 6 наблюдаются у 95% |

7
известных комплексов.
Классификация комплексных соединений по типу лигандов.
I. Комплексы, содержащие молекулярные монодентатные лиганды:
а) Аквакомплексы (лиганды – молекулы воды) |
|
|||||
|
[Co(H2О)6]Cl2 |
хлорид гексааквакобальта (II), |
к.ч. = 6 |
|||
[Ca(H2O)4](NO3)2 |
нитрат тетрааквакальция, |
к.ч. = 4 |
||||
б) Аммиакаты (Аммины. Лиганды – молекулы аммиака): |
||||||
[Cu(NH3)4]SO4 |
сульфат тетрамминмеди (II), |
к.ч.= 4 |
||||
[Pt(NH3)6]Cl4 |
хлорид гексамминплатины (IV), |
к.ч. = 6 |
||||
в) Карбонилы |
металлов (лиганды – |
молекулы СО, |
||||
|
|
|
|
|
|
|
комплексообразователь – атом металла в нулевой степени окисления).
[Fe(CO)5] |
пентакарбонилжелезо, |
к.ч. = 5 |
|
|
неэлектролиты |
[Co(CO)6] |
гексакарбонилкобальт, |
к.ч. = 6. |
г) Полигалогениды (типа Me[Hal(Hal2)x], комплексообразователь –
галогенид-ион, лиганды – молекулы галогенов):
K[I(I2)] йодойодат(I) калия.
II.Комплексные соединения, содержащие ионные лиганды.
а) Ацидокомплексы (лиганды – кислотные остатки
кислородсодержащих или бескислородных кислот):
K4[Fe(CN)6] гексацианоферрат (II) калия, к.ч.= 6.
8
Na3[Co(NO2)6] гексанитрокoбальтат(III) натрия, к.ч. = 6
б) Гидроксосоли (лиганды – гидроксильные группы)
Na3[Al(OH)6] гексагидроксоалюминат (III) натрия, к.ч. = 6.
Ш. Циклические комплексные соединения, содержащие полидентатные лиганды.
а) собственно циклические комплексные соединения – во
внутренней |
сфере |
они |
имеют |
циклы, |
образованные |
комплексообразователем и полидентатным лигандом:
(CH2)2 –NH2 |
H2N – (CH2)2 |
|
|
|
NH2 |
NH2 |
||
|
Co |
Cl3 |
|
|
к.ч. = 6 |
|
Н2N |
NH2 |
|
(CH2)2 |
|
Образовались три пятичленных цикла, каждый из которых, как
клешня, захватил комплексообразователь. Соединения такого типа
называются клешневидные или хелатные (chele – клешня).
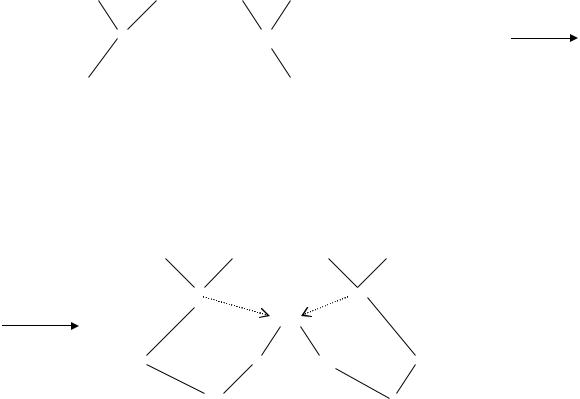
9
б) внутрикомплексные соединения: полидентатный лиганд
связан с комплексообразователем и |
обычными ковалентными и |
|
донорно-акцепторными |
связями |
(такие лиганды называются |
комплексонами). Комплексоны – производные аминополикарбоновых
кислот.
NaООСН2С |
СН2 – СН2 |
СН2СООNa |
N |
N |
+ Mg2+ |
HOOCH2C |
|
CH2COOH |
Комплексон III ( Трилон Б )
NaOOCH2C |
CH2 |
|
CH2 |
CH2COONa |
||||
|
||||||||
N |
|
|
N |
|
|
|
||
|
|
|
|
Mg |
|
|
|
|
CH2 |
O |
O |
|
|
CH2 + 2H+ |
|||
C |
|
|
|
C |
||||
|
|
|
|
|
|
|
|
|
O |
|
|
|
O |
||||
Это внутрикомплексное соединение, к.ч.(Mg2+) = 4.
Такие комплексы обладают повышенной прочностью. В организме
10
комплексоны могут связывать в комплексы этого типа токсические металлы, переводить в растворимое состояние камни в почках, печени и т.д. Комплексоны используются как антидоты, при радиационном поражении, для выведения 90Sr.
(См. Машковский М.Д. «Лекарственные средства» Глава
«Комплексообразующие соединения»).
Гемоглобин, хлорофилл, витамин В12 по своей природе –
внутрикомплексные соединения.
Комплексные соединения классифицируются также по заряду
комплекса: |
|
|
1. |
Анионные |
К2[HgI4] тетрайодомеркурат (II) калия. |
2. |
Катионные |
[Ag(NH3)2]Cl хлорид диамминсеребра (I). |
3.Катионо-анионные [Cr(NH3)6][Co(CN)6]
гексацианокобальтат(III) гексамминхрома (III).
4. Нейтральные комплексы (неэлектролиты).
[PtCl2(NH3)2] диамминдихлороплатина (II).
