
- •10. Понятие об идеальном растворе. Константа растворимости. Условия растворения и образования осадков.
- •Второй закон Рауля
- •Растворы электролитов
- •14.Автопротолиз воды. Константа автопротолиза воды. Водородный показатель.
- •15. Типы протолитических реакций. Понятие о гидролизе. Роль гидролиза в биохимических процессах. Ацидиметрия и алкалиметрия.
- •16 Вопрос. Буферные системы:их классификация и механизм действия. Буферные системы крови бионеорганические и биоорганические. Буферная ёмкость. Кислотно-основный баланс организма
- •17. Лигандообразовательные реакции. Основные положения координационной теории Вернера. Комплексообразователь, лиганды, координационные числа, дентантность.
- •18. Пространственное строение комплексных соединений. Классы комплексных соединений: внутрикомплексные, анионные, катионные нейтральные.
- •Вопрос №21. Химия элементов s-блока. Электронные структуры атомов и катионов. Сравнение свойств ионов элементов 1а- и 2а-групп. Биологическая роль натрия, калия, магния, кальция.
- •Биологическая роль элементов. Химическое сходство и биологический антагонизм.
- •Вопрос №22.
- •Вопрос 23. Химия элементов p-блока
- •24 Вопрос. Адсорбционные равновесия и …
- •Адсорбция на подвижной границе раздела фаз(на поверхности жидкости)
- •Вопрос 30.
- •Вопрос 30 (следующий)
- •Вопрос 32. Потенциометрия.
- •Вопрос 33 Электродные потенциалы и механизмы их возникновения.
- •Вопрос 35. Жидкости и ткани организма как проводники второго рода. Удельная электропроводимость. Закон Кольрауша о независимой подвижности ионов. Гидратация ионов.
Вопрос 32. Потенциометрия.
Потенциометрия – один из электрохимических методов анализа. Гальванические элементы, используемые в потенциометрии, составляют из измерительного электрода и электрода сравнения. Измерительный электрод отражает свойства раствора (активность ионов, концентрации веществ). По механизму возникновения различают ионно-металлические, редокс-электроды, мембранные.
Ионно-металлический электрод – металл, опущенный в раствор соли металла, функционирует как электрод Iрода, если его потенциал зависит от активности катиона в растворе. Полуреакция: Mz++ze-=M
В газовых электродах потенциал-определяющий материал не является проводником, поэтому используют инертные металлы, насыщенные соответствующим газом. Электроды II рода представляют собой малоактивный металл, покрытый слоем собственного труднорастворимого электролита, опущенный в раствор хорошо растворимого электролита с одноименными анионами.Полуреакции Mz++ze-=M дополнительно идет реакция: MA= Mz++Az-. Суммарная реакция: MA++ze-=M+Az-.
Электроды II рода – электроды, обратимые по отношения к катионам и анионам.
Мембранные электроды подразделяют на электроды с твердой мембраной, стеклянные электроды, электроды с жидкой мембраной. Потенциал мембранного электрода зависит от активности ограниченного числа ионов. Электроды, зависящие только от одного рода ионов – ионоселективные.
В стеклянной мембране переносчик электричества – ионы. В настоящее время использую H+ -селективные электроды.
Водородный электрод при давлении водорода рН2 равном 1 атм (1,01 х 105 Па), термодинамич. активности ионов водорода в р-ре аН+, равной 1, наз. стандартным водородным электродом, а его потенциал условно принимают равным нулю. Потенциалы других электродов, отнесенные к стандартному водородному электроду, составляют шкалу стандартных электродных потенциалов .Для водородного электрода сравнения Нернста уравнение записывается в виде:
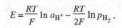
где Т - абс. т-ра; F - постоянная Фарадея; R - газовая постоянная. При рН2 = 1 атм электродный потенциал
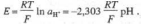
Используется в широком диапазоне рН - от значений, соответствующим конц. к-там, до значений, соответствующим конц. щелочам. Однако в нейтральных р-рах водородный электрод сравнения может нормально функционировать лишь при условии, что р-р обладает достаточно хорошими буферными св-вами. Это связано с тем, что при установлении равновесного потенциала на платинированной платине, а также при пропускании тока через водородный электрод сравнения появляется (или исчезает) нек-рое кол-во ионов Н+, т. е. изменяется рН р-ра, что особенно заметно в нейтральных средах. Водородный электрод применяют в широком интервале т-р, отвечающем существованию водных р-ров. Следует, однако, учитывать, что при повышении т-ры парциальное давление водорода падает вследствие роста давления паров р-рителя и обусловленное этим изменение потенциала электрода сравнения соответствует ур-нию
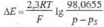 ,
где р - барометрич. давление (в кПа), a ps
- суммарное давление насыщ. паров над
р-ром (кПа). Возможность использования
водородного электрода в орг. средах
требует спец. проверки, т. к. Pt может
катализировать процессы с участием
орг. соед., вследствие чего нарушается
равновесие электродной р-ции и электрод
приобретает стационарный потенциал,
отличный от равновесного.
Каломельный
электрод сравнения изготавливают,
используя ртуть и р-ры каломели в хлориде
калия. Электродная р-ция на этом электроде
отвечает ур-нию: 2Hg + 2Сl-
,
где р - барометрич. давление (в кПа), a ps
- суммарное давление насыщ. паров над
р-ром (кПа). Возможность использования
водородного электрода в орг. средах
требует спец. проверки, т. к. Pt может
катализировать процессы с участием
орг. соед., вследствие чего нарушается
равновесие электродной р-ции и электрод
приобретает стационарный потенциал,
отличный от равновесного.
Каломельный
электрод сравнения изготавливают,
используя ртуть и р-ры каломели в хлориде
калия. Электродная р-ция на этом электроде
отвечает ур-нию: 2Hg + 2Сl- Hg2Cl2,
а соответствующее ур-ние Нернста имеет
вид:
Hg2Cl2,
а соответствующее ур-ние Нернста имеет
вид:
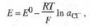
где
E0
- стандартный потенциал. В зависимости
от концентрацииКС1 различают насыщенный, нормальный и
децинормальныйкаломельные
электродысравнения. Этиэлектродысравнения хорошо воспроизводимы,
устойчивы и пригодны для работы при
т-рах до 80 °С. При более высоких т-рах
начинается разложениехлорида
ртути. Частокаломельный
электродсравнения подсоединяют
через солевой мостик, состоящий из
концентриров. р-ра КС1 для снижениядиффузионного
потенциала. Потенциал Екаломельного
электродасравнения зависит от т-ры,
причем температурный коэф. минимален
для децинормальногоэлектрода,
для к-рого Е =0,3365 - 6 х 10-5(t-25),
где t - т-ра (°С).
Галогеносеребряные
электродысравнения представляют собой серебряную
проволоку, покрытую галогенидомсеребра,
к-рый наносится путем термич. или
электрохим. разложениясолисеребра.
Электродная р-ция отвечает ур-нию: Ag +
Hal- AgHal
+ е (Hal - галоген),
а ур-ние Нернста имеет вид: .
AgHal
+ е (Hal - галоген),
а ур-ние Нернста имеет вид: .

Удобны
при работе с электрохим. ячейками без
жидкостного мостика, применимы как в
водных, так и во мн. неводных средах,
устойчивы при повышенных т-рах. В области
т-р 0-95 °С потенциал хлорсеребряного
электродасравнения описывается
ур-нием: E=0,23655-- 4,8564 x 10-4t
- 3,4205 x 10-6t2
+ 5,869 x 10-9t3.
Оксидно-ртутный электродсравнения приготавливают изртутии насыщенных р-ровоксида
ртутив водном р-рещелочи.
Электродная р-ция: Hg2O
+ 2e + H2O 2Hg + 2OH ;
2Hg + 2OH ;
ур-ние
Нернста:
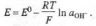
Удобен при работе в щелочных р-рах, т. к. при этом легко реализовать цепи без жидкостного соединения.
Потенциометрический метод титрования основан на измерении потенциала электрода, погруженного в раствор. Величина этого потенциала пропорциональна концентрации соответствующих ионов в растворе. Электрод, по потенциалу которого судят о концентрации определяемых ионов в растворе, называют индикаторным электродом. Потенциал индикаторного электрода определяют, сравнивая его с постоянной величиной потенциала электрода сравнения. Обычно в качестве электрода сравнения применяют нормальный водородный электрод или каломельный электрод.
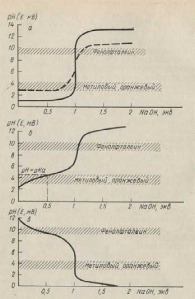
Рис. 17. Кривые потенциометрического титрования.
а - кривая нейтрализации хлористоводородной кислоты едким натром (10-1 и 10-3 н. растворы); б - кривая нейтрализации уксусной кислоты едким натром; в - кривая нейтрализации аммиака хлористоводородной кислотой.
Зависимость величины потенциала индикаторного электрода от концентрации раствора позволяет установить точку эквивалентности при титровании, так как в этой точке концентрация определяемого иона становится ничтожно малой, что в свою очередь приводит к резкому изменению (скачку) потенциала (рис. 17).
Титрование, при котором точка эквивалентности определяется по скачку потенциала электрода, погруженного в раствор, называют потенциометрическим титрованием, Потенциометричеокое титрование может успешно использоваться для титрования окрашенных и мутных растворов, слабых кислот и оснований, смесей кислот или оснований, смесей окислителей или восстановителей в неводных средах, для определения рН исследуемых растворов и т. д. Таким образом, метод потенциометрического титрования имеет ряд существенных преимуществ по сравнению с индикаторным методом.
