
- •10. Понятие об идеальном растворе. Константа растворимости. Условия растворения и образования осадков.
- •Второй закон Рауля
- •Растворы электролитов
- •14.Автопротолиз воды. Константа автопротолиза воды. Водородный показатель.
- •15. Типы протолитических реакций. Понятие о гидролизе. Роль гидролиза в биохимических процессах. Ацидиметрия и алкалиметрия.
- •16 Вопрос. Буферные системы:их классификация и механизм действия. Буферные системы крови бионеорганические и биоорганические. Буферная ёмкость. Кислотно-основный баланс организма
- •17. Лигандообразовательные реакции. Основные положения координационной теории Вернера. Комплексообразователь, лиганды, координационные числа, дентантность.
- •18. Пространственное строение комплексных соединений. Классы комплексных соединений: внутрикомплексные, анионные, катионные нейтральные.
- •Вопрос №21. Химия элементов s-блока. Электронные структуры атомов и катионов. Сравнение свойств ионов элементов 1а- и 2а-групп. Биологическая роль натрия, калия, магния, кальция.
- •Биологическая роль элементов. Химическое сходство и биологический антагонизм.
- •Вопрос №22.
- •Вопрос 23. Химия элементов p-блока
- •24 Вопрос. Адсорбционные равновесия и …
- •Адсорбция на подвижной границе раздела фаз(на поверхности жидкости)
- •Вопрос 30.
- •Вопрос 30 (следующий)
- •Вопрос 32. Потенциометрия.
- •Вопрос 33 Электродные потенциалы и механизмы их возникновения.
- •Вопрос 35. Жидкости и ткани организма как проводники второго рода. Удельная электропроводимость. Закон Кольрауша о независимой подвижности ионов. Гидратация ионов.
Вопрос 33 Электродные потенциалы и механизмы их возникновения.
Для определения направления и полноты протекания окислительно-восстановительных реакций между окислительно-восстановительными системами в водных растворах используются значения электродных потенциалов этих систем.Механизм возникновения электродных потенциалов, их количественное определение, процессы, которые сопровождаются возникновением электрического тока или вызваны электрическим током, изучаются особым разделом химии – электрохимией. Сочетая электрод, представляющий исследуемую окислительно-восстановительную систему, со стандартным водородным электродом, определяют электродный потенциал Е данной системы. Для того, чтобы можно было сравнивать окислительно-восстановительные свойства различных систем по их электродным потенциалам, необходимо, чтобы последние также были измерены при стандартных условиях. Таковыми обычно являются концентрация ионов, равная 1 моль/л, давление газообразных веществ 101,325 кПа и температура 298,15 К. Потенциалы, измеренные в таких условиях, носят название стандартных электродных потенциалов и обозначаются Ео. Они часто называются также окислительно-восстановительными или редокс-потенциалами, представляя собой разность между редокс-потенциалом системы при стандартных условиях и потенциалом стандартного водородного электрода.. Стандартный электродный потенциал – это потенциал данного электродного процесса при концентрациях всех участвующих в нем веществ, равных единице.Стандартные электродные потенциалы окислительно-восстановительных систем приводятся в справочной литературе. Эти системы записаны в форме уравнений полуреакций восстановления, в левой части которых находятся атомы, ионы или молекулы, принимающие электроны (окисленная форма) Электрохимический ряд напряжений характеризует свойства металлов в водных растворах:чем меньше электродный потенциал металла, тем легче он окисляется и труднее восстанавливается из своих ионов;металлы, имеющие отрицательные электродные потенциалы, т.е. стоящие в ряду напряжений левее водорода, способны вытеснять его из разбавленных растворов кислот;каждый металл способен вытеснять (восстанавливать) из растворов солей те металлы, которые имеют более высокий электродный потенциал.При условиях, отличающихся от стандартных, численное значение равновесного электродного потенциала для окислительно-восстановительной системы, записанной в форме , определяется по уравнению Нернста:
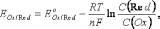
Где
 и
и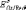 - соответственно электродный и стандартный
потенциалы системы; R – универсальная
газовая постоянная; Т – абсолютная
температура; F – постоянная Фарадея; n
– число электронов, участвующих в
окислительно-восстановительном
процессе.С(Red) и C(Ox) – молярные концентрации
соответственно восстановленной и
окисленной форм соединения. Например,
для окислительно-восстановительной
системы
- соответственно электродный и стандартный
потенциалы системы; R – универсальная
газовая постоянная; Т – абсолютная
температура; F – постоянная Фарадея; n
– число электронов, участвующих в
окислительно-восстановительном
процессе.С(Red) и C(Ox) – молярные концентрации
соответственно восстановленной и
окисленной форм соединения. Например,
для окислительно-восстановительной
системы
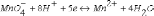 уравнение
Нернста имеет вид
уравнение
Нернста имеет вид
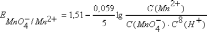
Вопрос 35. Жидкости и ткани организма как проводники второго рода. Удельная электропроводимость. Закон Кольрауша о независимой подвижности ионов. Гидратация ионов.
Ткани организма человека относятся к проводникам второго рода, поэтому прохождение через них электрического тока связано с перемещением положительно заряженных частиц (катионов) к отрицательному полюсу - катоду, а отрицательно заряженных частиц (анионов) - к положительному полюсу - аноду.
В биологических тканях возникает ток проводимости. Подойдя к тому или иному полюсу, ионы восстанавливают свою наружную электронную оболочку и превращаются в атомы, обладающие высокой химической активностью. Этот процесс носит название терапевтического электролиза.
Электропроводность растворов электролитов обусловлена перемещением ионов в электрическом поле (в отличие от электронной проводимости проводников первого рода). Электропроводность - математическая оценка способности раствора проводить электрический ток, зависит в основном от степени минерализации исследуемого раствора и его температуры.
В качестве количественной меры способности раствора электролита проводить электрический ток используют обычно удельную электропроводность κ (каппа) - величину, обратную удельному сопротивлению (т.е. величину, обратную сопротивлению столба раствора между электродами площадью 1 см2, находящимися на расстоянии 1 см):
χ=1/ρ, Ом-1см-1
Удельная электропроводимость - численно равна проводимости вещества заключенного в объеме между двумя электродами, стоящими друг от друга на расстоянии l=1, и с S=1 м2
χ=1/R*l/S
Зависит от концентрации вещ-ва в растворе.
Закон Кольрауша (или закон аддитивности электропроводности при бесконечном разбавлении электролитов) гласит, что в бесконечно разбавленном растворе перенос электричества осуществляется всеми ионами независимо друг от друга; при этом общая молярная электропроводность раствора равна сумме молярных электропроводностей отдельных ионов.
Гидратация (от греч. hydro — вода) — присоединение молекул воды к молекулам или ионам. Гидратация является частным случаем сольватации — присоединения к молекулам или ионам веществ молекул органического растворителя. В отличие от гидролиза гидратация не сопровождается образованием водородных или гидроксильных ионов. Гидратация в водных растворах приводит к образованию стойких и нестойких соединений воды с растворенным веществом (гидратов); в органических растворителях образуются аналогичные гидратам сольваты. Гидратация обусловливает устойчивость ионов в растворах и затрудняет их ассоциацию.
Гидратация является движущей силой электролитической диссоциации — источником энергии, необходимой для разделения противоположно заряженных ионов.
