
- •«Поджелудочная железа. Инсулин, глюкагон, соматостатин. Диабет 1-го типа (инсулиндефицитный) и диабет 2-го типа (инсулинрезистентный). Причины возникновения, сравнительная характеристика»
- •Содержание
- •1.Введение
- •2. Экзокринная функция поджелудочной железы
- •3. Эндокринная функция поджелудочной железы
- •3.1. Инсулин: химическая природа, регуляция секреции, механизм действия, роль в обмене.
- •Реакции, связанные с активностью фосфатидилинозитол-3-киназы
- •Реакции, связанные с активацией map-киназного пути
- •Очень быстрые эффекты (секунды)
- •Быстрые эффекты (минуты)
- •Медленные эффекты (минуты-часы)
- •Очень медленные эффекты (часы-сутки)
- •3.2. Глюкагон: химическая природа, регуляция секреции, механизм действия, роль в обмене.
- •3.3. Соматостатин: химическая природа, регуляция секреции, механизм действия, роль в обмене.
- •4. Гипо- и гиперинсулинизм
- •5. Са́харный диабе́т 1-го типа
- •6.Сахарный диабет 2-го типа
- •Заключение
- •Лист для заметок литература
Реакции, связанные с активностью фосфатидилинозитол-3-киназы
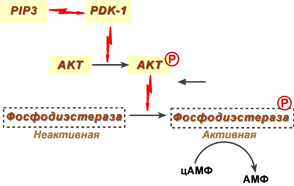
После активации IRS-белок и целый ряд вспомогательных белков способствуют закреплению на мембране гетеродимерного фермента фосфоинозитол-3-киназы, содержащего регуляторную p85 (название произошло от ММ белка 85 кДа) и каталитическую p110 субъединицы. Эта киназа фосфорилирует мембранные фосфатидилинозитолфосфаты по 3-му положению до фосфатидилинозитол-3,4-дифосфата (PIP2) и до фосфатидилинозитол-3,4,5-трифосфата (PIP3). Считается, что PIP3 может выступать в качестве мембранного якоря для других элементов при действии инсулина.

После образования указанных фосфолипидов происходит активация протеинкиназы PDK1 (3-phosphoinositide dependent protein kinase-1), которая вместе с ДНК-протеинкиназой (DNA-PK, англ. DNA-dependent protein kinase, DNA-PK) дважды фосфорилирует протеинкиназу B (также часто называемую AKT1, англ. RAC-alpha serine/threonine-protein kinase), которая прикрепляется к мембране благодаря PIP3.
Фосфорилирование активирует протеинкиназу В (АКТ1), она покидает мембрану и перемещается в цитоплазму и ядро клетки, где фосфорилирует многочисленные белки-мишени (более 100 штук), которые обеспечивают дальнейший клеточный ответ:

в частности, именно действие протеинкиназы В (АКТ1) приводит к перемещению глюкозных транспортеров ГлюТ-4 на клеточную мембрану и к поглощению глюкозы миоцитами и адипоцитами.
также, например, активная протеинкиназа В (АКТ1) фосфорилирует и активирует фосфодиэстеразу (ФДЭ), гидролизующую цАМФ до АМФ, в результате чего концентрация цАМФ в клетках-мишенях снижается. Поскольку при участии цАМФ активируется протеинкиназа А, стимулирующая ТАГ-липазу и фосфорилазу гликогена, то в результате действия инсулина в адипоцитах происходит подавление липолиза, а в печени – остановка гликогенолиза.
еще одним примером является действие протеинкиназы В (AKT) на киназу гликогенсинтазы. Фосфорилирование этой киназы инактивирует ее. В результате она не в состоянии действовать на гликогенсинтазу, фосфорилировать и инактивировать ее. Таким образом, влияние инсулина приводит к удержанию гликогенсинтазы в активной форме и к синтезу гликогена.
Реакции, связанные с активацией map-киназного пути
В самом начале развертывания этого пути в действие вступает еще один субстрат инсулинового рецептора – белок Shc (англ. Src (homology 2 domain containing) transforming protein 1), связывающийся с активированным (аутофосфорилированным) инсулиновым рецептором. Далее Shc-белок взаимодействует с Grb-белком (англ. growth factor receptor bound protein) и вынуждает его присоединиться к рецептору.
Также в мембране постоянно присутствует белок Ras, который в спокойном состоянии связан с ГДФ. Поблизости из Ras-белка находятся «вспомогательные» белки – GEF (англ. GTF exchange factor) и SOS (англ. son of sevenless) и белок GAP (англ. GTPase activating factor).
Формирование комплекса белков Shc-Grb активирует группу GEF-SOS-GAP и приводит к замене ГДФ на ГТФ в составе Ras-белка, что вызывает его активацию (комплекс Ras-ГТФ) и передачу сигнала на протеинкиназу Raf-1.
При активации протеинкиназы Raf-1 происходит ее присоединение к плазматической мембране, фосфорилирование дополнительными киназами по остаткам тирозина, серина и треонина, а также одновременное взаимодействие с рецептором инсулина.
Далее активированная Raf-1 фосфорилирует (активирует) MAPK-K – киназу белка MAPK(англ. mitogen-activated protein kinase, также она называется MEK, англ. MAPK/ERK kinase), которая в свою очередь фосфорилирует фермент МАPК (MAP-киназа, или иначе ERK, англ. extracellular signal-regulated kinase).
1. После активации МАP-киназа напрямую или через дополнительные киназы фосфорилирует белки цитоплазмы, изменяя их активность, например:
активация фосфолипазы А2 приводит отщеплению от фосфолипидов арахидоновой кислоты, которая далее превращается в эйкозаноиды,
активация рибосомальной киназы запускает процесс трансляции белков,
активация протеинфосфатаз приводит к дефосфорилированию многих ферментов.

2. Весьма масштабной по последствиям является передача инсулинового сигнала в ядро. МАP-киназа самостоятельно фосфорилирует и этим активирует ряд факторов транскрипции, обеспечивая считывание определенных генов, важных для деления, дифференцировки и других клеточных ответов.
Одним из белков, связанных с этим механизмом, является транскрипционный фактор CREB (англ. cAMP response element-binding protein). В неактивном состоянии фактор дефосфорилирован и не влияет на транскрипцию. При действии активирующих сигналов фактор связывается с определенными CRE-последовательностями ДНК (англ. cAMP-response elements), усиливая или ослабляя считывание информации с ДНК и ее реализацию. Кроме MAP-киназного пути фактор чувствителен к сигнальным путям, связанным с протеинкиназой А и кальций-кальмодулином.
Скорость эффектов действия инсулина
Биологические эффекты инсулина подразделяются по скорости развития:
