
-1-
УДК ББК
ISВN 5-89004-097-9
Чебышев Н. В., Гринева Г. Г. , Козарь М. В. , Гуленков С. И.
Биология (Учебник). - М.: ВУНМЦ, 2000. - 592 с.
Учебник для студентов медицинских ВУЗов "Биология", авторы Н. В. Чебышев,
Г. Г. Гринева, М. В. Козарь, С. И. Гуленков, предназначен для факультетов высшего сестринского образования и для изучения курса биологии на фармацевтических факультетах. Он написан в соответствии с программами для этих факультетов.
Учебник может быть использован при изучении курса биологии в медицинских училищах и колледжах.
Учебник содержит введение и шесть разделов в соответствии с программой:
• молекулярно-генетический уровень организации живого
• клеточный уровень организации живого
• организменный уровень организации живого
• популяционно-видовой уровень организации живого
• биоценотический уровень организации живого
• биосферный уровень организации живого Учебник адаптирован к программам этих факультетов, хорошо иллюстрирован, что позволит студентам лучше освоить изучаемый материал.
http://www.bestmedbook.com/

-2-
Глава 1
ОРГАНИЗАЦИЯ ЖИЗНИ НА ЗЕМЛЕ
1.1. Введение в науку биологию
Биология — наука о жизни (от греч. биос — жизнь, логос — наука) — изучает закономерности жизни и развития живых существ. Термин «биология» был
предложен немецким ботаником Г.Р. Тревиранусом и французским естествоиспытателем Ж.-Б. Ламарком в 1802 году независимо друг от друга. Биология относится к естественным наукам. Разделы науки биологии можно классифицировать по-разному. Например, в биологии выделяют науки по объектам исследования: о животных — зоологию; о растениях — ботанику; анатомию и физиологию человека как основу медицинской науки. В пределах каждой из этих наук имеются более узкие дисциплины. Например, в зоологии выделяют протозоологию, энтомологию, гельминтологию и другие.
Биологию классифицируют по дисциплинам, изучающим морфологию (строение) и физиологию (функции) организмов. К морфологическим наукам относят, например, цитологию, гистологию, анатомию. Физиологические науки — это
физиология растений, животных и человека.
Для современной биологии характерно комплексное взаимодействие с другими науками (химией, физикой, математикой) и появление новых сложных дисциплин.
Значение биологии для медицины велико. Биология — теоретическая основа медицины. Врач древней Греции Гиппократ (460-274 г. до н.э.) считал, что
«необходимо, чтобы каждый врач понимал природу». Во всех теоретических и практических медицинских науках используются общебиологические обобщения. Теоретические исследования, проводимые в различных областях биологии, позволяют использовать полученные данные в практической деятельности медицинских работников. Например, открытие структуры вирусов, возбудителей инфекционных заболеваний (оспы, кори, гриппа и других), и способов их передачи, позволило ученым создать вакцину, предотвращающую распространение этих заболеваний или снижающую риск гибели людей от этих тяжелых инфекций.
1.2. ОПРЕДЕЛЕНИЕ ЖИЗНИ
Согласно определению, данному ученым-биологом М.В. Волькенштейном (1965 г.), «живые организмы представляют собой открытые, саморегулирующиеся, самовоспроизводящиеся системы, построенные из биополимеров — белков и
нуклеиновых кислот». Через живые открытые системы проходят потоки энергии,

-3-
информации, вещества.
Живые организмы отличаются от неживых признаками, совокупность которых определяет их жизненные проявления.
1.3. ОСНОВНЫЕ СВОЙСТВА ЖИВОГО
К основным свойствам живого можно отнести:
1. Химический состав. Живые существа состоят из тех же химических элементов, что и неживые, но в организмах есть молекулы веществ, характерных только для живого (нуклеиновые кислоты, белки, липиды).
2. Дискретность и целостность. Любая биологическая система (клетка,
организм, вид и т.д.) состоит из отдельных частей, т.е. дискретна. Взаимодействие этих частей образует целостную систему (например, в состав организма входят отдельные органы, связанные структурно и функционально в единое целое).
3. Структурная организация. Живые системы способны создавать порядок из хаотичного движения молекул, образуя определенные структуры. Для живого характерна упорядоченность в пространстве и времени. Это комплекс сложных саморегулирующихся процессов обмена веществ, протекающих в строго определенном порядке, направленном на поддержание постоянства внутренней среды — гомеостаза.
4. Обмен веществ и энергии. Живые организмы — открытые системы, совершающие постоянный обмен веществом и энергией с окружающей средой. При изменении условий среды происходит саморегуляция жизненных процессов по принципу обратной связи, направленная на восстановление постоянства внутренней среды — гомеостаза. Например, продукты жизнедеятельности могут оказывать сильное и строго специфическое тормозящее воздействие на те ферменты, которые составили начальное звено в длинной цепи реакций.
5. Самовоспроизведение. Самообновление. Время существования любой биологической системы ограничено. Для поддержания жизни происходит процесс самовоспроизведения, связанный с образованием новых молекул и структур, несущих генетическую информацию, находящуюся в молекулах ДНК.
6. Наследственность. Молекула ДНК способна хранить, передавать наследственную информацию, благодаря матричному принципу репликации, обеспечивая материальную преемственность между поколениями.
7. Изменчивость. При передаче наследственной информации иногда возникают различные отклонения, приводящие к изменению признаков и свойств у потомков. Если эти изменения благоприятствуют жизни, они могут закрепиться отбором.
8. Рост и развитие. Организмы наследуют определенную генетическую информацию о возможности развития тех или иных признаков. Реализация информации происходит во время индивидуального развития — онтогенеза. На

-4-
определенном этапе онтогенеза осуществляется рост организма, связанный с репродукцией молекул, клеток и других биологических структур. Рост сопровождается развитием.
9. Раздражимость и движение. Все живое избирательно реагирует на внешние воздействия специфическими реакциями благодаря свойству раздражимости. Организмы отвечают на воздействие движением. Проявление формы движения зависит от структуры организма.

-5-
2.1.1. НЕОРГАНИЧЕСКИЕ ВЕЩЕСТВА
Вода необходима для осуществления жизненных процессов в клетке. Ее основные функции следующие:
1. Универсальный растворитель.
2. Среда, в которой протекают биохимические реакции.
3. Определяет физиологические свойства клетки (ее упругость, объем).
4. Участвует в химических реакциях.
5. Поддерживает тепловое равновесие клетки и организма в целом благодаря высокой теплоемкости и теплопроводности.
6. Основное средство для транспорта веществ. Минеральные вещества клетки находятся в виде ионов. Наиболее важные из них катионы - это K+ , Na+, Ca++, Mg++, анионы - это Сl-, НСО3-, Н2РО4-.
Концентрация ионов в клетке и окружающей ее среде неодинаковая. Например, содержание калия в клетках в десятки раз выше, чем в межклеточном пространстве. Катионов натрия, наоборот, в 10 раз меньше в клетке, чем вне ее. Снижение концентрации К+ в клетке приводит к уменьшению в ней воды, количество которой возрастает в межклеточном пространстве тем больше, чем выше в межклеточной жидкости концентрация Na+. Уменьшение катионов натрия в межклеточном пространстве приводит к уменьшению в нем содержания воды.
Неравномерное распределение ионов калия и натрия с наружной и внутренней стороны мембран нервных и мышечных клеток обеспечивает возможность возникновения и распространения электрических импульсов.
Анионы слабых кислот внутри клетки способствуют сохранению определенной концентрации водородных ионов (рН). В клетке поддерживается слабощелочная реакция (рН=7,2).
2.1.2. 0РГАНИЧЕСКИЕ ВЕЩЕСТВА
Органические соединения состоят из многих повторяющихся элементов (мономеров) и представляют собой крупные молекулы, называемые полимерами. К органическим полимерным молекулам относят белки, жиры, углеводы, нуклеиновые кислоты.
2.1.2.1. Белки
Белки - высокомолекулярные полимерные органические вещества, определя- ющие структуру и жизнедеятельность клетки и организма в целом. Структурной единицей, мономером их биополимерной молекулы является аминокислота. В образовании белков принимают участие 20 аминокислот. В состав молекулы
каждого белка входят определенные аминокислоты в свойственном этому белку количественном соотношении и порядке расположения в полипептидной цепи.

-6-
Аминокислота имеет следующую формулу:
В состав аминокислот входят: NH2 - аминокислотная группа, сдающая
основными свойствами; СООН - карбоксильная группа, имеет кислотные свойства. Аминокислоты отличаются друг от друга своими радикалами - R. Аминокислоты - амфотерные соединения, соединяющиеся друг с другом в молекуле белка с помощью пептидных связей.
Схема конденсации аминокислот (образование первичной структуры белка)
Есть первичная, вторичная, третичная и четвертичная структуры белка (рис. 2).
Рис. 2. Различные структуры молекул белка: / — первичная, 2 - вторичная, 3 — третичная,
4 — четвертичная (на примере гемоглобина крови).
Порядок, количество и качество аминокислот, входящих в состав молекулы белка, определяют его первичную структуру (например, инсулин). Белки первичной структуры могут с помощью водородных связей соединяться в спираль и образовывать вторичную структуру (например, кератин). Полипептидные цепи,
скручиваясь определенным образом в компактную структуру, образуют глобулу (шар), представляющую собой третичную структуру белка. Большинство белков имеют третичную структуру. Аминокислоты активны только на поверхности глобулы.

-7-
Белки, имеющие глобулярную структуру, объединяются вместе и формируют четвертичную структуру (например, гемоглобин). Замена одной аминокислоты
приводит к изменению свойств белка.
При воздействии высокой температуры, кислот и других факторов сложные белковые молекулы разрушаются. Это явление называется денатурацией. При улучшении условий денатурированный белок способен восстановить свою структуру вновь, если не разрушается его первичная структура. Этот процесс называется ренатурацией (рис. 3).
Рис. 3. Денатурация белка.
Белки отличаются видовой специфичностью. Каждый вид животных имеет свои белки.
В одном и том же организме каждая ткань имеет свои белки — это тканевая специфичность.
Организмы характеризуются также индивидуальной специфичностью белков. Белки бывают простые и сложные. Простые состоят из аминокислот, например, альбумины, глобулины, фибриноген, миозин и др. В состав сложных белков, кроме аминокислот, входят и другие органические соединения, например, жиры, углеводы, образуя липопротеиды, гликопротеиды и другие. Белки выполняют следующие функции:
• ферментативную (например, амилаза, расщепляет углеводы);
• структурную (например, входят в состав мембран клетки);
• рецепторную (например, родопсин, способствует лучшему зрению);
• транспортную (например, гемоглобин, переносит кислород или диоксид
углерода);
• защитную (например, иммуноглобулины, участвуют в образовании
иммунитета);
• двигательную (например, актин, миозин, участвуют в сокращении мышечных волокон);
• гормональную (например, инсулин, превращает глюкозу в гликоген);
• энергетическую (при расщеплении 1 г белка выделяется 4,2 ккал энергии).
2.1.2.2. Жиры
Жиры - органические соединения, которые наряду с белками и углеводами,

-8-
обязательно присутствуют в клетках. Их относят к большой группе органических жироподобных соединений, классу липидов.
Жиры представляют собой соединения глицерина (трехатомный спирт) и высокомолекулярных жирных кислот (насыщенных, например, стеариновой,
пальмитиновой, и ненасыщенных, таких, как олеиновая, линолевая и другие). Соотношением насыщенных и ненасыщенных жирных кислот определяются физические и химические свойства жиров.
Жиры нерастворимы в воде, но хорошо растворяются в органических растворителях, например в эфире.
Функции липидов в клетке разнообразны:
• структурная (принимают участие в построении мембраны);
• энергетическая (при распаде в организме 1 г жира выделяется 9,2 ккал энергии - в 2,5 раза больше, чем при распаде того же количества углеводов);
• защитная (от потери тепла, механических повреждений);
• жир - источник эндогенной воды (при окислении Юг жира выделяется 11 г воды);
• регуляция обмена веществ (например, стероидные гормоны —
кортикостерон и др.).
2.1.2.3. Углеводы
Углеводы - большая группа органических соединений, входящих в состав живых клеток. Термин "углеводы" введен впервые отечественным ученым
К. Шмидтом в середине прошлого столетия (1844 г.). В нем отражены представления о группе веществ, молекула которых отвечает общей формуле: Сn(Н2O)n — углерод и вода.
Углеводы принято делить на 3 группы: моносахариды (например, глюкоза, фруктоза, манноза), олигосахариды (включают от 2 до 10 остатков моносахаридов: сахароза, лактоза), полисахариды (высокомолекулярные соединения, например,
гликоген, крахмал).
Функции углеводов:
1) моносахариды, первичные продукты фотосинтеза, служат исходными для построения разнообразных органических веществ;
2) углеводы — основной источник энергии для организма, т.к. при их
разложении с использованием кислорода выделяется больше энергии, чем при окислении жира в том же объеме кислорода;
3) защитная функция. Слизь, выделяемая различными железами, содержит много углеводов и их производных. Она предохраняет стенки полых органов (бронхи, желудок, кишечник) от механических повреждений. Обладая антисептическими свойствами, слизь защищает организм от проникновения болезнетворных бактерий;
4) структурная и опорная функции. Сложные полисахариды и их производные
-9-
входят в состав плазматической мембраны, оболочки растительных и бактериальных клеток, наружного скелета членистоногих.
2.1.2.4. Нуклеиновые кислоты
Нуклеиновые кислоты - это ДНК (дезоксирибонуклеиновая кислота) и РНК (рибонуклеиновая кислота).
2.1.2.4.1. Дезоксирибонуклеиновая кислота
Молекулы ДНК (дезоксирибонуклеиновой кислоты) - это самые крупные
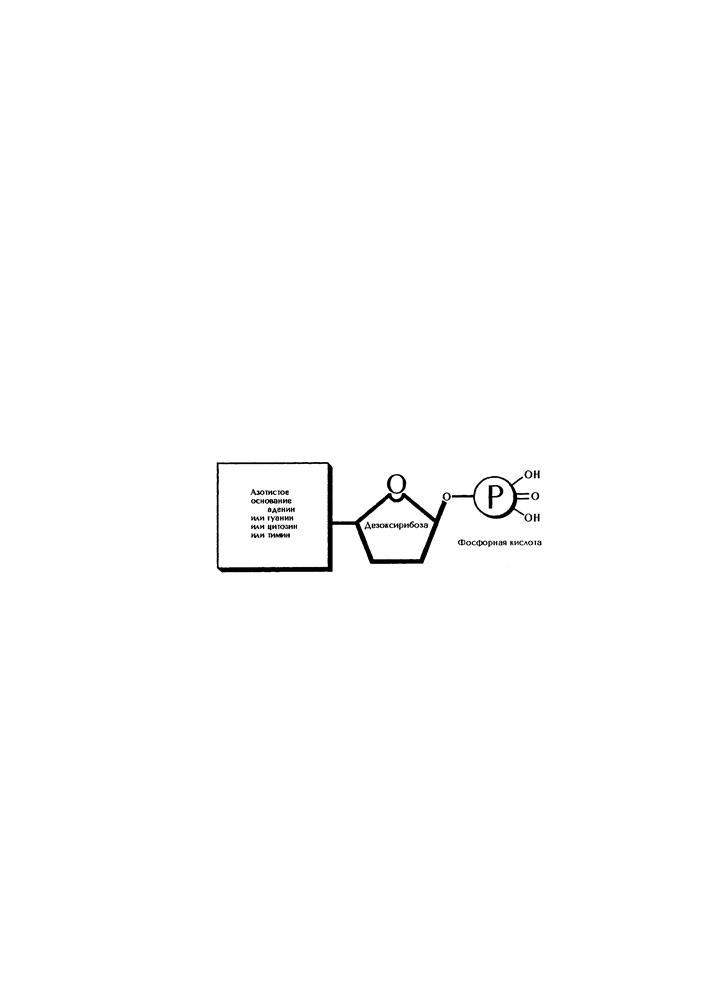
биополимеры, их мономером является нуклеотид (рис. 4). Он состоит из остатков трех веществ: азотистого основания, углевода дезоксирибозы и фосфорной кислоты. Известны четыре нуклеотида, участвующие в образовании молекулы ДНК. Они отличаются друг от друга азотистыми основаниями.
Два азотистых основания цитозин и тимин - производные пиримидина. Аденин и гуанин - относят к производным пурина. В названии каждого нуклеотида отражено название азотистого основания. Различают нуклеотиды: цитидиловый (Ц),
тимидиловый (Т), адениловый (А), гуаниловый (Г).
Рис. 4. Схема строения нуклеотида.
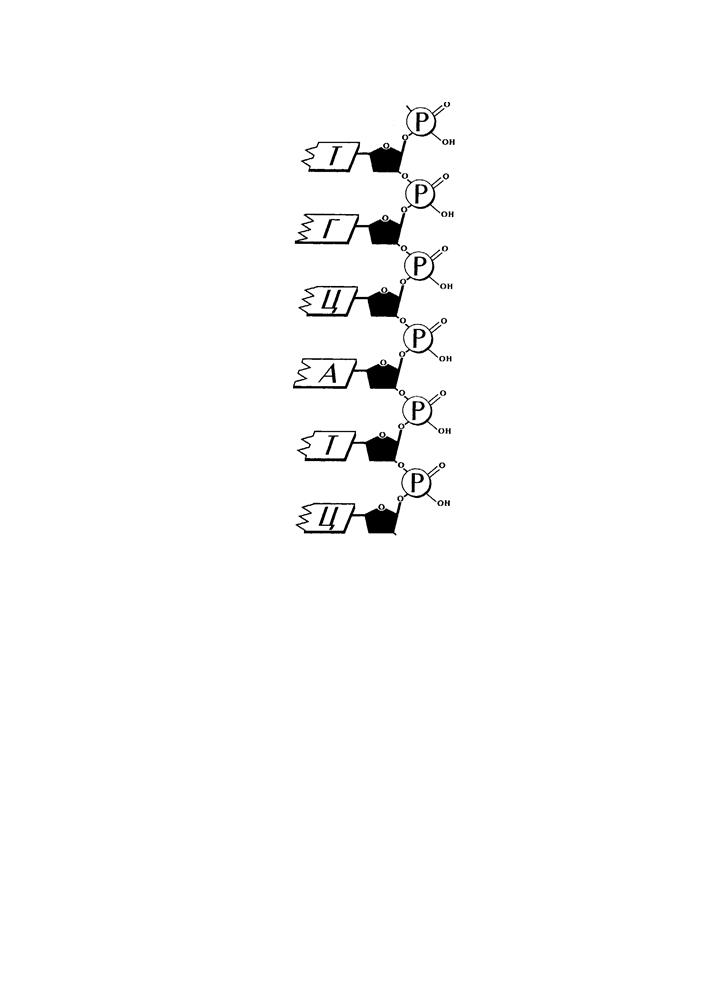
Соединение нуклеотидов в нити ДНК происходит через углевод одного нуклеотида и остаток фосфорной кислоты соседнего (рис. 5).
-10-
Рис. 5. Соединение нуклеотидов в полинуклеотидную цепь.
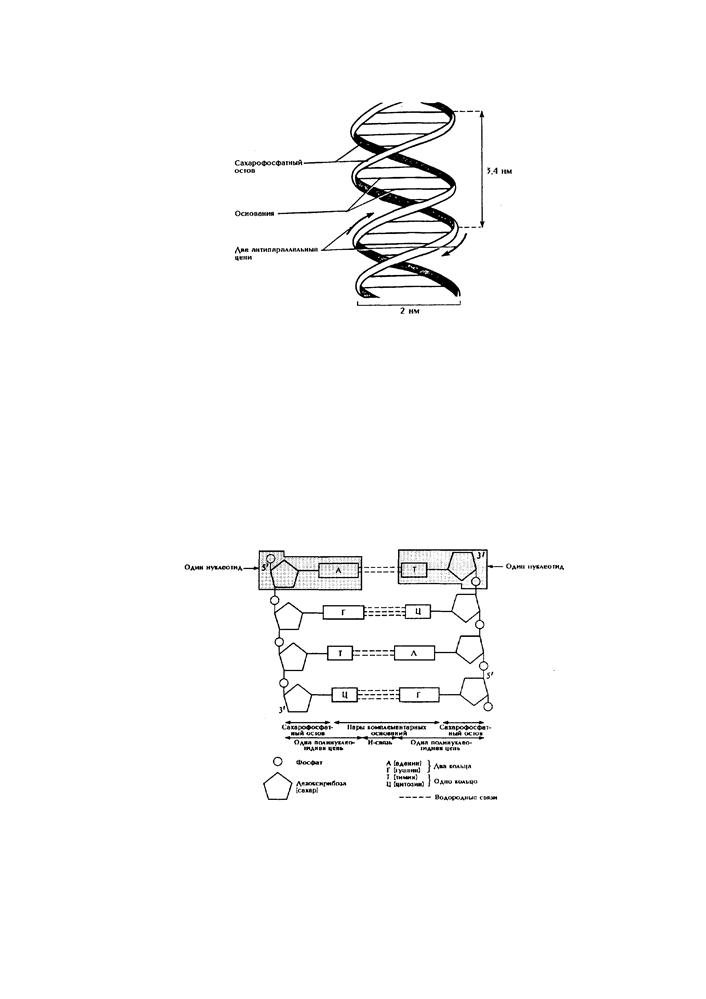
Согласно модели ДНК, предложенной Дж. Уотсоном и Ф. Криком (1953 г.), молекула ДНК представляет собой две спирально обвивающие друг друга нити (рис.
6). Обе нити вместе закручены вокруг общей оси. Две нити молекулы удерживаются рядом водородными связями, которые возникают между их комплементарными азотистыми основаниями. Аденин комплементарен тимину, а гуанин - цитозину. Между аденином и тимином возникают две водородные связи, между гуанином и цитозином - три (рис. 7).
ДНК находится в ядре, где она вместе с белками образует линейные структуры - хромосомы. Хромосомы хорошо видны при микроскопировании в период деления ядра; в интерфазе они деспирализованы.
-11-
Рис. 6. Схематическое изображение структуры ДНК. На один полный оборот спирали приходится 10 пар оснований (расстояние между соседними парами оснований равно 0,34 нм).
ДНК имеется в митохондриях и пластидах (хлоропластах и лейкопластах), где их молекулы образуют кольцевые структуры. В клетках доядерных организмов также присутствует кольцевая ДНК.
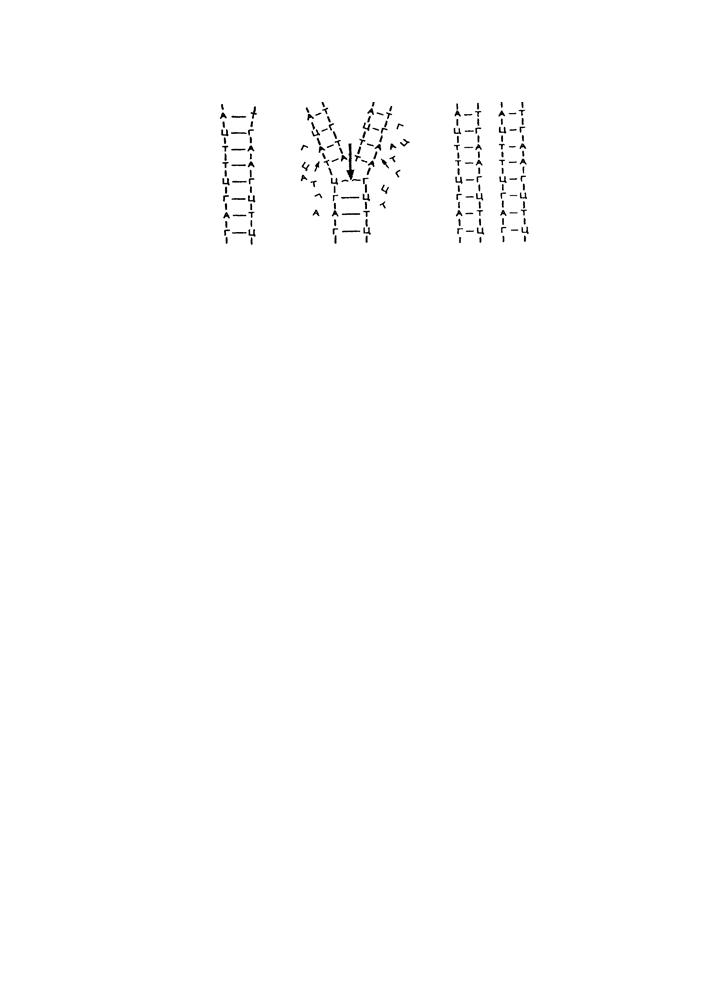
ДНК способна к самоудвоению (редупликации) (рис. 8). Это имеет место в определенном периоде жизненного цикла клетки, называемом синтетическим. Редупликация позволяет сохранить постоянство структуры ДНК. Если под воздействием различных факторов в процессе репликации в молекуле ДНК происходят изменения в числе, порядке следования нуклеотидов, то возникают мутации.
Рис. 7. ДНК (схематическое изображение развернутых цепей).
-12-
Рис. 8. Схема удвоения ДНК.
Основная функция ДНК - хранение наследственной информации, заключенной в последовательности нуклеотидов, образующих ее молекулу, и передача этой информации дочерним клеткам. Возможность передачи наследственной информации от клетки к клетке обеспечивается способностью хромосом к разделению на хроматиды с последующей редупликацией молекулы ДНК.
В ДНК заключена вся информация о структуре и деятельности клеток, о признаках каждой клетки и организма в целом. Эта информация называется генетической.
В молекуле ДНК закодирована генетическая информация о последовательности аминокислот в молекуле белка. Участок ДНК, несущий информацию об одной полипептидной цепи, называется геном. Передача и реализация информации осуществляется в клетке при участии рибонуклеиновых кислот.
2.1.2.4.2. РИБОНУКЛЕИНОВАЯ КИСЛОТА
Рибонуклеиновые кислоты бывают нескольких видов. Есть рибосомальная, транспортная и информационная РНК. Нуклеотид РНК состоит из одного из азотистых оснований (аденина, гуанина, цитозина и урацила), углевода - рибозы и остатка фосфорной кислоты. Молекулы РНК - одноцепочковые.
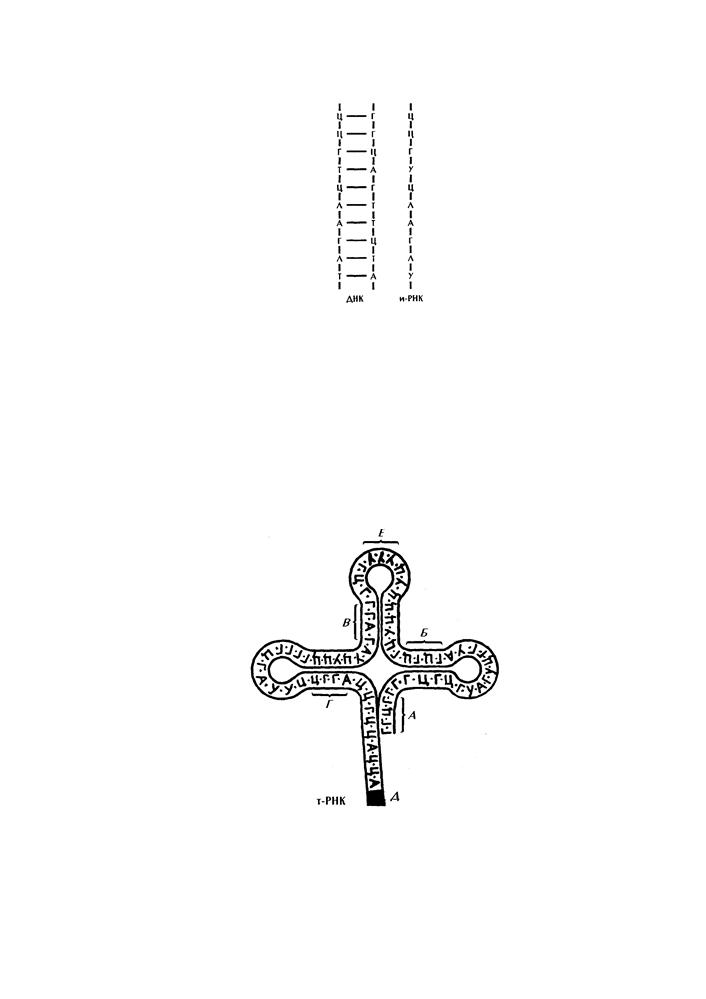
Рибосомальная РНК (р-РНК) в соединении с белком входит в состав рибосом. Р-РНК составляет 80% от всей РНК в клетке. На рибосомах идет синтез белка. Информационная РНК (и-РНК) составляет от 1 до 10% от всей РНК в клетке. По строению и-РНК комплементарна участку молекулы ДНК, несущему информацию о синтезе определенного белка. Длина и-РНК зависит от длины участка ДНК, с которого считывали информацию. И-РНК переносит информацию о синтезе белка из ядра в цитоплазму (рис. 9).
-13-
Рис. 9. Схема синтеза и-РНК.
Транспортная РНК (т-РНК) составляет около 10% всей РНК Она имеет
короткую цепь нуклеотидов и находится в цитоплазме. Т—РНК присоединяет определенные аминокислоты и подвозит их к месту синтеза белка к рибосомам. Т- РНК имеет форму трилистника. На одном конце находится триплет нуклеотидов (антикодон), кодирующий определенную аминокислоту. На другом конце имеется триплет нуклеотидов, к которому присоединяется аминокислота (рис. 10).
При комплементарности триплета т-РНК (антикодона) и триплета и-РНК
(кодона), аминокислота занимает определенное место в молекуле белка.
Рис. 10. Схема т-РНК.
РНК находится в ядрышке, в цитоплазме, в рибосомах, в митохондриях и пластидах.
В природе есть еще один вид РНК. Это вирусная РНК. У одних вирусов она
-14-
выполняет функцию хранения и передачи наследственной информации. У других вирусов эту функцию выполняет вирусная ДНК.
2.1.2.4.3. АДЕНОЗИНТРИФОСФОРНАЯ КИСЛОТА
Аденозинмонофосфорная кислота (АМФ) входит в состав всех РНК. При присоединении еще двух молекул фосфорной кислоты (Н3РО4) АМФ превращается в аденозинтрифосфорную кислоту (АТФ) и становится источником энергии,
необходимой для биологических процессов, идущих в клетке.
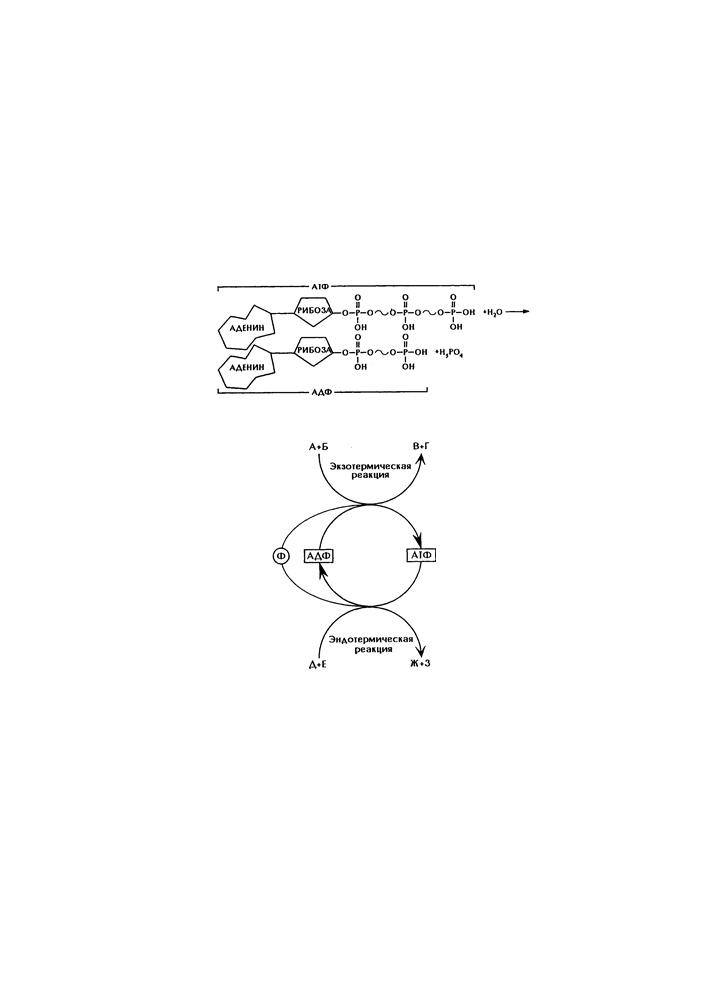
Рис. 11. Структура АТФ. Превращение АТФ в АДФ (- - макроэргическая связь).
Рис. 12. Передача энергии.
Схема передачи энергии с помощью АТФ из реакций, в результате которых энергия освобождается (экзотермические реакции), в реакции, потребляющие эту энергию (эндотермические реакции). Последние реакции очень разнообразны: биосинтез, мышечные сокращения и т.д.
Аденозинтрифосфорная кислота (АТФ) состоит из азотистого основания — аденина, сахара — рибозы и трех остатков фосфорной кислоты. Молекула АТФ очень неустойчива и способна отщеплять одну или две молекулы фосфата с выделением большого количества энергии, расходуемой на обеспечение всех жизненных функций клетки (биосинтез, трансмембранный перенос, движение,
образование электрического импульса и др.). Связи в молекуле АТФ называют

-15-
макроэргическими (рис. 11, 12).
Отщепление концевого фосфата от молекулы АТФ сопровождается выделением 40 кДж энергии.
Синтез АТФ происходит в митохондриях.

-16-
