
- •Химическая связь. Типы взаимодействия молекул
- •Ковалентная связь
- •Метод валентных связей Основные положения мвс
- •Механизмы образования химической связи
- •Донорно-акцепторный механизм
- •Валентность
- •Гибридизация атомных орбиталей и геометрия молекул
- •Метод молекулярных орбиталей
- •Ионная связь Ионные молекулы существуют только в парах над нагретыми солями. Энергия разрыва ионной связи не определяется энергией притяжения ионов.
- •Потенциальная энергия для однозарядных ионов:
- •Поляризующее действие ионов тем больше, чем меньше радиус и чем устойчивее электронная оболочка иона. Наибольшее поляризующее действие оказывают те ионы, которые слабо поляризуются.
- •Понять механизм восприятия цвета нашими глазами может помочь "круг цветов",
- •Энергия связи
- •1649 КДж/моль. В молекуле метана имеются четыре равноценные связи с-н поэтому средняя энергия такой связи равна
- •При переходе от одинарной связи двойной и тройной (между одними и теми же атомами) энергия связи возрастает, однако связь укрепляется непропорцианально увеличению её кратности.
- •Б)что длина связи уменьшается с возрастанием порядка или кратности связи, а прочность увеличивается с уменьшением длины связи.
Метод валентных связей Основные положения мвс
1)Ковалентная химическая связь образуется двумя электронами с противоположно направленными спинами, причем эта электронная пара принадлежит двум атомам.
2)Ковалентная связь тем прочнее, чем в большей степени перекрываются взаимодействующие электронные облака.
3)При образовании молекулы электронная структура составляющих её атомов в основном сохраняется, а все химические связи в молекуле могут быть представлены набором фиксированных(локализованных) двух центровых двухэлектронных связей. (не для всех соединений).
В целом электронная структура молекулы выглядит как набор различных валентных схем(метод локализованных пар).
Ковалентная связь образуется за счет перекрывания электронных облаков связываемых атомов. Существуют разные способы перекрывания этих электронных облаков.
1. Прямое перекрывание:

В этом случае единственная область перекрывания электронных облаков лежит на прямой, соединяющей ядра атомов. Связь, образованная таким образом, называется σ-связью.
В зависимости от вида перекрывающихся облаков может образоваться s-s,
s-p, p-p, s-d, p-d σ-связи.
σ-связь - ковалентная связь между атомами, образованная при прямом перекрывании их электронных облаков.
2. Боковое перекрывание:

В этом случае две области перекрывания электронных облаков находятся по разные стороны от плоскости, в которой лежат ядра связываемых атомов. Связь, образованная при таком перекрывании ЭО, называется π- связью. Как и в случае σ-связи, в зависимости от вида перекрывающихся облаков могут образоваться различные разновидности π-связи: p-p, p-d, d-d π-связи.
π-связь –ковалентная связь между атомами образованная при боковом перекрывании их электронных облаков.
При возникновении ковалентной связи происходит перекрывание электронных облаков атомов с образованием молекулярного электронного облака, сопровождающееся выигрышем энергии. Молекулярное электронное облако располагается между центрами обоих ядер и обладает повышенной электронной плотностью по сравнению с плотностью атомного электронного облака.
Механизмы образования химической связи
В методе валентных связей различают обменный и донорно-акцепторный механизмы образования химической связи.
Обменный механизм. К обменному механизму образования химической связи относятся случаи, когда в образовании электронной пары от каждого атома участвует по одному электрону.
В молекулах Н2, Li2, Na2 связи образуются за счет неспаренных s-электронов атомов. В молекулах F2 и Cl2 – за счет неспаренных р-электронов. В молекулах HF и HCl связи образуются s-электронами водорода и
p-электронами галогенов. Особенностью образования соединений по обменному механизму является насыщаемость, которая показывает, что атом образует не любое, а ограниченное количество связей. Их число, в частности, зависит от количества неспаренных валентных электронов.
Из квантовых ячеек N и Н можно видеть,
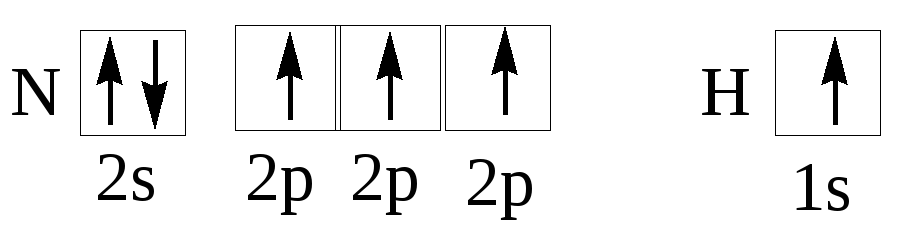
что атом азота имеет 3 неспаренных электрона, а атом водорода – один. Принцип насыщаемости указывает на то, что устойчивым соединением должен быть NH3, а не NH2, NH или NH4. Однако существуют молекулы, содержащие нечетное число электронов, например, NO, NO2, ClO2. Все они характеризуются повышенной реакционной способностью.
На отдельных стадиях химических реакций могут образовываться и валентно ненасыщенные группы, которые называются радикалами, например, H, NH2, O, CH3. Реакционная способность радикалов очень высока и поэтому время их существования, как правило, мало.
