
- •Раздел 2
- •Глава 11
- •11.1. Общая характеристика
- •11.2. Виды гравиметрических определений
- •11.3. Понятие о механизме образования осадка
- •11.4. Коллоидная стадия образования осадка
- •11.5. Причины загрязнения осадка и способы их устранения
- •11.6. Основные этапы методики гравиметрического определения методом осаждения
- •11.7. Гравиметрия в фармацевтическом анализе
- •Глава 12
- •12.1. Основные понятия титриметрии
- •12.2. Классификация титриметрических методов анализа и способов титрования
- •12.3. Стандартные растворы и стандартные вещества
- •12.4. Расчёты, связанные с приготовлением растворов титрантов и титрованием Расчёты, связанные с приготовлением растворов
- •Расчёты, связанные с титрованием
- •Глава 13
- •13.1. Титранты и стандартные вещества
- •13.2. Обнаружение конечной точки титрования. Кислотно-основные индикаторы
- •Метиловый красный
- •Тимолфталеин (бесцветный синий)
- •Феноловый красный
- •13.3. Кривые титрования
- •0,10 М раствором NaOh
- •Расчёты для построения кривой титрования
- •Расчёты для построения кривой титрования
- •0,10 М Na2co3 0,10 м раствором hCl
- •13.4. Факторы, влияющие на величину скачка титрования
- •13.5. Погрешности титрования
- •13.6. Некоторые случаи практического применения кислотно-основного титрования в водных растворах
- •Глава 14
- •14.1. Ограничения возможностей кислотно-основного основного титрования в водных растворах
- •14.2. Критерии выбора растворителя для кислотно-основного титрования
- •14.3. Применение в фармацевтическом анализе Титрование в кислотных растворителях
- •Глава 15
- •15.1. Общая характеристика
- •15.2. Меркуриметрическое титрование
- •15.3. Комплексонометрическое титрование
- •15.3.1. Понятие о комплексонах
- •15.3.2. Свойства этилендиаминтетрауксусной кислоты и её взаимодействие с катионами металлов
- •15.3.3. Кривые титрования
- •1,010-3 М раствором эдта при рН 9,50 в присутствии 510-2 м nh3
- •15.3.4. Способы обнаружения конечной точки титрования. Металлоиндикаторы
- •Пирокатехиновый фиолетовый – металлоиндикатор из группы сульфофталеиновых красителей. Представляет собой четырёхосновную кислоту. Комплексы с металлами обычно окрашены в синий цвет.
- •15.3.5. Индикаторные погрешности
- •15.3.6. Титранты и стандартные вещества
- •15.3.7. Способы комплексонометрического титрования и его применение
- •Глава 16
- •16.1. Общая характеристика
- •16.2. Аргентометрическое титрование
- •16.2.1. Кривые титрования
- •Расчёты для построения кривой титрования
- •16.2.2. Способы обнаружения конечной точки титрования
- •Метод Мора
- •Метод Фольгарда
- •Особенность определения хлоридов
- •Особенность определения иодидов
- •Метод Фаянса
- •16.2.3. Титранты и стандартные вещества
- •16.2.4. Применение в фармацевтическом анализе
- •16.3. Меркурометрическое титрование
- •Глава 17
- •17.1. Общая характеристика и классификация
- •17.2. Кривые титрования
- •17.3. Способы обнаружения конечной точки титрования. Окислительно-восстановительные индикаторы
- •Глава 18
- •18.1. Иодометрическое титрование
- •Титранты и стандартные вещества
- •Обнаружение конечной точки титрования
- •18.2. Хлориодометрическое титрование
- •18.3. Иодатометрическое титрование
- •18.4. Броматометрическое титрование
- •18.5. Нитритометрическое титрование
- •18.6. Перманганатометрическое титрование
- •18.8. Дихроматометрическое титрование
- •18.8. Цериметрическое титрование
Глава 16

16.1. Общая характеристика
Осадительное титрование - группа титриметрических методов анализа, основанных на реакциях образования малорастворимых соединений, выделяющихся из раствора в виде осадка.
Лишь немногие из реакций образования осадков пригодны для титриметрии. Для того чтобы реакция могла быть использована в осадительном титровании
-
она должна протекать количественно (величина KS осадка для бинарных электролитов не должна быть больше 10-8-10-10) и быстро при обычных условиях, не сопровождаться образованием пересыщенных растворов;
-
образующийся осадок должен иметь постоянный состав и не должен загрязняться в процессе осаждения;
-
должен существовать способ обнаружения конечной точки титрования.
Среди всех методов осадительного титрования практическое значение имеют аргентометрическое и меркурометрическое титрование. Однако и данные методы, несмотря на большой круг возможных определяемых объектов среди лекарственных веществ, применяются нечасто.

16.2. Аргентометрическое титрование
Аргентометрическим титрованием называется титриметрический метод анализа, основанный на образовании малорастворимых соединений серебра.
Основным титрантом в аргентометрии является AgNO3. Аргентометрия используется для определения галогенидов, тиоцианатов, цианидов, фосфатов и других ионов.
16.2.1. Кривые титрования
Рассмотрим кривую титрования 0,10 М NaCl 0,10 М раствором AgNO3. Кривая титрования будет представлять собой зависимость pCl = -lg[Cl-] от степени оттитрованности. Произведение растворимости AgCl равно 1,810-10, а pKs – 9,74.
До точки эквивалентности pCl можно рассчитать как
![]()
В точке эквивалентности [Ag+] = [Cl-], поэтому:
![]()
После точки эквивалентности формулу для расчёта рСl можно получить, исходя из того, что:
![]() ;
;![]()
Расчёты, необходимые для построения кривой титрования, показаны в табл. 16.1, а сама кривая приведена на рис. 16.1.
Табл. 16.1
Расчёты для построения кривой титрования
0,10 М NaCl 0,10 М AgNO3
|
f |
Расчётная формула |
pCl |
pAg |
|
0 |
|
1,00 |
- |
|
0,100 |
|
1,09 |
8,65 |
|
0,500 |
аналогично |
1,48 |
8,26 |
|
0,900 |
аналогично |
2,28 |
7,46 |
|
0,990 |
аналогично |
3,30 |
6,44 |
|
0,999 |
аналогично |
4,3 |
5,4 |
|
1,000 |
|
4,87 |
4,87 |
|
1,001 |
|
5,4 |
4,3 |
|
1,01 |
аналогично |
6,44 |
3,30 |
|
1,10 |
аналогично |
7,42 |
2,32 |
|
1,50 |
аналогично |
8,04 |
1,70 |
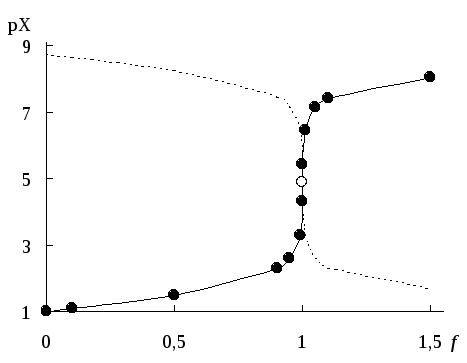
Рис. 16.1. Кривая титрования 0,10 М NaСl 0,10 M AgNO3
Пунктиром показано изменение pAg в процессе титрования
Величина скачка титрования в аргентометрии зависит от исходной концентрации титруемого аниона и титранта и растворимости образующегося осадка (рис. 16.2)
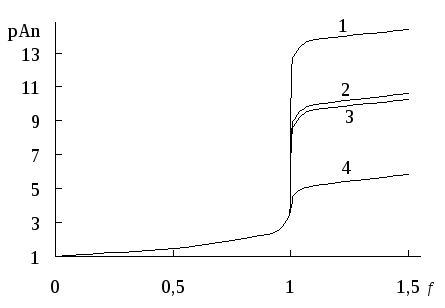
Рис. 16.2. Кривые титрования 0,1 М растворов анионов 0,1 М AgNO3
1 – иодид (pKS = 16,08); 2 – бромид (12,28); 3 – тиоцианат (11,96); 4 – иодат (7,52).
Факторы, способствующие увеличению растворимости (нагревание, увеличение ионной силы), приводят к уменьшению величины скачка титрования.
