
- •Раздел 3
- •Глава 19
- •19.1. Природа и свойства электромагнитного излучения
- •19.2. Классификация спектроскопических методов анализа
- •Вид используемого электромагнитного излучения
- •Глава 20
- •20.1. Основной закон поглощения электромагнитного излучения
- •20.2. Отклонения от основного закона светопоглощения
- •20.3. Атомно-абсорбционная спектроскопия
- •20.3.1. Процессы, приводящие к появлению аналитического сигнала
- •20.3.2. Измерение аналитического сигнала
- •20.3.3. Практическое применение
- •20.4. Молекулярная абсорбционная спектроскопия в уф- и видимой области
- •20.4.1. Молекулярные спектры поглощения в уф- и видимой области
- •20.4.2. Измерение аналитического сигнала
- •20.4.3. Практическое применение и основные приёмы фотометрического анализа
- •Фотометрические реакции
- •Дифференциальная (разностная) фотометрия
- •Производная спектрофотометрия
- •20.5.1. Процессы, приводящие к появлению аналитического сигнала
- •20.5.2. Общая характеристика ик-спектров
- •20.5.3. Измерение аналитического сигнала
- •20.5.4. Практическое применение
- •Глава 21
- •21.1. Атомно-эмиссионная спектроскопия
- •21.1.1. Процессы, приводящие к появлению аналитического сигнала
- •21.1.2. Измерение аналитического сигнала
- •21.1.3. Практическое применение
- •20.2. Люминесцентная спектроскопия
- •20.2.1 Классификация видов люминесценции
- •21.2.2 Механизм молекулярной фотолюминесценции. Флуоресценция и фосфоресценция
- •21.2.3 Основные характеристики и закономерности люминесценции
- •21.2.4. Влияние различных факторов на интенсивность флуоресценции растворов
- •Природа вещества
- •21.2.5. Измерение аналитического сигнала
- •21.2.6. Практическое применение и основные приёмы люминесцентного анализа
- •Глава 22
- •22.1. Общая характеристика
- •22.2. Классификация хроматографических методов
- •22.3. Хроматографические параметры
- •Хроматографические характеристики, используемые для идентификации веществ (характеристики удерживания)
- •Хроматографические характеристики, используемые для количественного определения веществ
- •22.4. Теории хроматографического разделения
- •Глава 23
- •23.1. Общая характеристика
- •23.2. Устройство газового хроматографа
- •Хроматографическая колонка
- •Детекторы
- •23.3. Особенности газотвёрдофазной хроматографии
- •23.4. Особенности газожидкостной хроматографии
- •23.5. Индексы удерживания Ковача
- •23.6. Практическое применение
- •Глава 24
- •24.1. Общая характеристика
- •24.2. Плоскостная хроматография
- •24.2.1. Методика получения плоскостной хроматограммы
- •24.2.2. Анализ плоскостной хроматограммы
- •24.2.3. Практическое применение
- •24.3. Колоночная жидкостная хроматография
- •24.3.1. Устройство жидкостного хроматографа
- •24.3.2. Практическое применение
- •24.4. Характеристика отдельных видов жидкостной хроматографии
- •24.4.1. Ионообменная хроматография
- •Неподвижные и подвижные фазы
- •24.4.2. Эксклюзионная хроматография
- •Глава 25
- •25.1. Основные понятия, связанные с электрохимическими методами анализа
- •25.2. Классификация электрохимических методов анализа
- •В табл. 25.1 приведена классификация основных электрохимических методов анализа в зависимости от измеряемого параметра.
- •25.3. Кондуктометрия
- •25.3.1. Теоретические основы и классификация
- •25.3.2. Измерение аналитического сигнала
- •25.3.4. Практическое применение
- •25.3.5. Понятие о высокочастотной кондуктометрии
- •Глава 26
- •26.1. Потенциометрический метод анализа
- •26.1.1. Общая характеристика и классификация
- •26.1.2. Условия измерения аналитического сигнала
- •26.1.3. Индикаторные электроды
- •26.1.4. Прямая потенциометрия
- •26.1.5. Потенциометрическое титрование
- •26.2. Кулонометрический метод анализа
- •26.2.1. Общая характеристика и классификация
- •26.2.2. Прямая кулонометрия
- •1) Рабочий электрод;
- •2) Электрод сравнения;
- •3) Вспомогательный электрод
- •26.2.3. Кулонометрическое титрование
- •Глава 27
- •27.1. Принцип измерения аналитического сигнала.
- •27.2. Вольтамперограмма
- •27.3. Некоторые современные разновидности вольтамперометрии
- •27.4. Практическое применение вольтамперометрии. Амперометрическое титрование
21.1.3. Практическое применение
АЭС используется для обнаружения и количественного определения различных элементов, обычно металлов. В качественном анализе используется наличие характерных линий в получаемых спектрах испускания. Наиболее подходящий атомизатор для качественного анализа - дуговой разряд, так как пламя даёт спектры бедные спектральные линиями, атомизатор с ИСП - наоборот, очень сложные спектры, которые можно расшифровать только с помощью компьютера.
Количественный анализ в АЭС основан на зависимости интенсивности испускания от концентрации данного элемента в анализируемой пробе. Зависимость между интенсивностью спектральных линий и концентрацией элемента в пробе является более сложной, чем, например, в ААС, и описывается уравнением Ломакина-Шайбе
![]() или
или
![]()
где a и b - эмпирические константы, которые характеризуют процессы, происходящие на поверхности электродов (a) и самопоглощение излучения (b).
Зависимость I от C не является линейной (в отличие от зависимости lgI от lgC). Самый большой диапазон линейности наблюдается при использовании атомизатора с ИСП.
Для определения концентрации в АЭС применяют метод градуировочного графика и метод добавок. Для построения градуировочного графика часто используют внутренние стандарты.
Предел обнаружения в АЭС при определении хорошо атомизируемых и легковозбудимых элементов с использованием пламенного атомизатора составляет 10-7-10-2%, других элементов (ИСП-атомизатор) - 10-8 - 10-2%.
Воспроизводимость при использовании пламени и ИСП - Sr = 0,01-0,05, при использовании искры и дуги Sr = 0,05 - 0,2.
20.2. Люминесцентная спектроскопия
Люминесцентной спектроскопией называют группу эмиссионных спектроскопических методов анализа, основанных на явлении люминесценции.
Люминесценцией (в переводе с лат. - «слабое свечение») называется свечение атомов, молекул и других более сложных частиц, возникающее в результате электронного перехода при их возвращении из возбуждённого состояния в основное. Люминесценцию иногда называют холодным светом, так как обычно температура люминесцирующего тела не отличается от температуры окружающей среды.
20.2.1 Классификация видов люминесценции
Понятие “люминесценция” включает в себя множество различных явлений. Существует несколько систем их классификации.
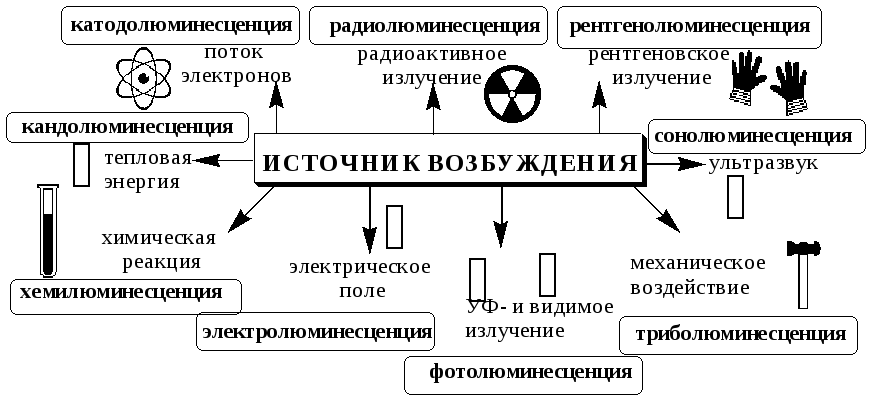

В аналитической химии чаще всего используется молекулярная фотолюминесценция. В зависимости от природы основного и возбуждённого состояния молекулы её подразделяют на флуоресценцию и фосфоресценцию.
21.2.2 Механизм молекулярной фотолюминесценции. Флуоресценция и фосфоресценция
При поглощении кванта света молекула вещества переходит из основного электронного состояния в возбуждённое. Одной из характеристик электронного состояния является мультиплетность
![]() ,
,
где S - суммарный спин данного электронного состояния.
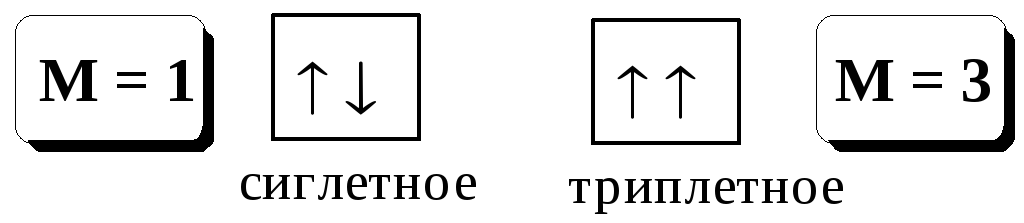
Рис.
21.3.
Фотопроцессы
в молекуле (диаграмма Яблонского)
КР -
колебательная релаксация; ВК - внутренняя
конверсия; ИКК - интеркомбинационная
конверсия; ФЛ - флуоресценция; Ф -
фосфоресценция.
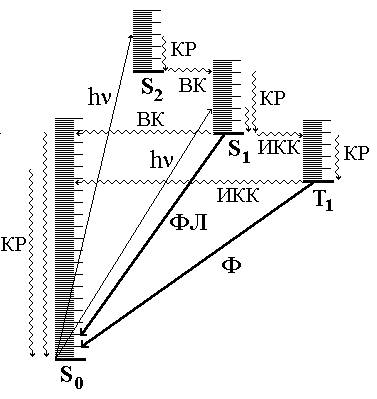
Для описания физических процессов, которым подвергаются молекулы в возбуждённом состоянии, обычно используют энергетические диаграммы типа показанной на рис. 21.3.
Когда молекула поглощает свет, она за очень короткое время (10-15 с) переходит на какой-то колебательный и вращательный уровень одного из возбуждённых синглетных состояний (обычно S1 или S2). Далее с возбуждённой молекулой могут происходить 2 типа процессов: безызлучательные (показаны на диаграмме волнистой линией) и излучательные (показаны на диаграмме прямой линией). Молекула может отдавать свою энергию небольшими порциями (например, при столкновении с другими молекулами). При этом электрон возвращается с более высоких колебательных уровней на более низкие в пределах данного электронного уровня. Такой процесс называется колебательной релаксацией. Безызлучательный переход между состояниями, имеющими одинаковую энергию и одинаковую мультиплетность, называется внутренней конверсией. Безызлучательный переход между состояниями, имеющими одинаковую энергию, но разную мультиплетность называется интеркомбинационной конверсией.
Флуоресценция - излучательный переход между состояниями, имеющими одинаковую мультиплетность.
В подавляющем большинстве случаев флуоресценция сложных органических молекул обусловлена переходом с нулевого колебательного уровня возбуждённого состояния S1 на какой-то из колебательных уровней S0, реже S2 S0 (например, в молекуле азулена) и очень редко Sk Sm или Tm Tn. Флуоресценция - быстрый процесс (10-9 - 10-6 с).
Фосфоресценция - излучательный переход между состояниями, имеющими разную мультиплетность.
Обычно фосфоресценции соответствует переход T1 S0. Переходы между состояниями с различной мультиплетностью имеют очень малую вероятность, то есть являются “запрещёнными”. Излучательный переход, обуславливающий фосфоресценцию, имеет в 106 раз меньшую вероятность, чем переход, определяющий флуоресценцию, поэтому фосфоресценция имеет гораздо большую длительность (в среднем 10-3 - 10 с), чем флуоресценция.
