- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •Получение алканов
- •2. Каталитическое гидрирование (Ni, Pd, Pt) ненасыщенных углеводородов при нагревании:
- •4. Гидролиз карбидов
- •5. Декарбоксилирование солей низших карбоновых кислот
- •Химические свойства алканов
- •2. Нитрование (реакция Коновалова)- реакция радикального замещения sr.
- •3. Реакции дегидрирования
- •5. Реакции горения
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •1. Крекинг и пиролиз нефтепродуктов.
- •2. Каталитическое (Ni, Pt, Pd) дегидрирование алканов при нагревании :
- •Химические свойства алкенов.
- •2. Реакции полимеризации:
- •3. Реакции окисления
- •Решение:
- •1) Условию задачи отвечает следующее строение:
- •Задачи и упражнения для самостоятельного решения
- •97. Смесь этена с бутаном, с плотность по водороду 21,5, сожгли. Продукты сгорания 20 л этой смеси пропустили через избыток раствора гидроксида кальция. Определите массу выпавшего осадка.
- •Диеновые углеводороды
- •1. Галогенирование
- •4. Полимеризация.
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •Алкины.
- •2. Взаимодействие карбидов металлов с водой
- •4. Дегидрогалогенирование дигалогеналканов:
- •5. Из галогеналканов под действием цинка:
- •Химические свойства алкинов
- •1. Галогенирование
- •3. Гидратация.
- •4. Гидрирование.
- •6. Кислотные свойства алкинов
- •8. Горение
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •Циклоалканы
- •Получение циклоалканов
- •2. Циклогексан и его производные получают гидрированием бензола:
- •Химические свойства циклоалканов
- •Примеры решения задач Пример 18.
- •Решение:
- •Пример 19.
- •Решение:
- •Пример 20.
- •Задачи и упражнения для самостоятельного решения
- •Получение аренов
- •Химические свойства аренов
- •1. Электрофильное замещение в бензольном кольце
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •2. Гидролиз алкилгалогенидов в кислой или щелочной среде:
- •3. Гидролиз сложных эфиров:
- •4. Восстановление более высокоокисленных соединений
- •5. Биохимические методы.
- •1. Кислотные свойства.
- •3. Дегидратация(отщепление воды).
- •5. Окисление спиртов
- •1. Многие из химических свойств двухатомных и трёхатомных спиртов походят на таковые одноатомных спиртов. Отличия:
- •Задачи и упражнения для самостоятельного решения
- •1. Кислотные свойства
- •2. Реакции электрофильного замещения в бензольном кольце
- •3. Окислительно-восстановительные реакции
- •4. Реакции комплексообразования
- •Задачи и упражнения для самостоятельного решения
- •Карбонильные соединения
- •Получение карбонильных соединений
- •1. Окисление спиртов
- •4. Гидратация алкинов(реакция Кучерова).
- •5. Получение ацетона в промышленности
- •Химические свойства карбонильных соединений
- •1. Окисление
- •2. Восстановление.
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •Карбоновые кислоты
- •1. Растворимые кислоты диссоциируют в воде:
- •2. Карбоновые кислоты (особенно растворимые в воде)
- •9. Окисление
- •11. Реакции в бензольном ядре ароматических кислот
- •12. Реакции ненасыщенных кислот
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •Сложные эфиры. Жиры.
- •2. Взаимодействие ангидрида карбоновой кислоты со спиртом
- •3. Взаимодействие хлорангидрида карбоновой кислоты со спиртом
- •Углеводы
- •1. Окисление
- •3. Алкилирование аминов:
- •4. Взаимодействие с ангидридами и хлорангидридами
- •7. Особенности ароматических аминов(анилина)
- •8. Окисление анилина
- •2. Обработка галогенсодержащих карбоновых кислот избытком аммиака:
- •3. Реакции, обусловленные наличием двух функциональных групп в
3. Алкилирование аминов:
CH3NH2 + CH3Cl (CH3)2NH +HCl,
(CH3)2 NH + CH3Cl (CH3)3N +HCl
C6H5NH2 + CH3Cl C6H5NHCH3
4. Взаимодействие с ангидридами и хлорангидридами
карбоновых кислот
C2H5NH2 + CH3 COCl C2H5 –NH- CO-CH3 + HCl
этилацетатамид
C2H5NH2 + (CH3-CO)2O C2H5-NH-CO-CH3 + CH3COOH
этилацетатамид
5. Комплексообразование (аналогично аммиаку)
CuSO4 + 4NH3 [Cu(NH3)4]SO4
CuSO4 + C2H5NH2 [Cu(NH2C2H5)4]SO4
6. Горение – при их горении образуется углекислый газ, вода и азот.
4С3H7NH2 + 21O2 12CO2 + 18H2O + 2N2
4C6H5NH2 + 31O2 24CO2 + 14H2O + 2N2
7. Особенности ароматических аминов(анилина)
Образуют соли только с сильными кислотами:
C6H5NH2 + HCl C6H5NH3Cl (хлорид фениламмония
или гидрохлорид анилина)
Аминогруппа сильно активирует ароматическое кольцо в реакциях замещения – анилин реагирует с бромной водой при комнатной температуре и без катализатора с выпадением осадка 2,4,6-триброманилина (качественная реакция на ароматические амины):

8. Окисление анилина
Другая качественная реакция - при действии хлорной извести образуются продукты с интенсивным фиолетовым окрашиванием.
АМИНОКИСЛОТЫ И ПЕПТИДЫ
Аминокислоты – амфотерные соединения, содержащие карбоксильную (кислотную) и аминогруппу (основную).
Классификация
1. В зависимости от взаимного расположения функциональных групп различают α,β,γ…- и т.д. аминокислоты, однако многообразные пептиды и
белки состоят из остатков α-аминокислот.
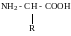
2. В зависимости от строения радикала R различают:
- алифатические аминокислоты (не имеют других функциональных групп в радикале);
- ароматические (содержат бензольное кольцо);
- гидроксиаминокислоты (содержат ОН-группу);
- серосодержащие (содержат SH-группу);
- гетероциклические (содержат цикл с гетероатомом);
- аминокислоты кислотного характера (содержат дополнительную СООН-группу);
- основные аминокислоты (содержат дополнительную NH2-группу).
3. В зависимости от возможности синтеза в живом организме аминокислоты делят на заменимые (могут быть синтезированы из других продуктов метаболизма) и незаменимые (не могут синтезироваться в организме и должны поступать с пищей).
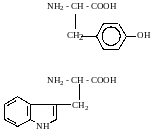
Всего в состав белков входит 20 (25) аминокислот. Для 10 из них желательно знать структурные формулы (это глицин, аланин, серин, валин, фенилаланин, тирозин, цистеин, лизин, триптофан и глутаминовая кислота).
|
Глицин
Аланин
Валин
Серин
Цистеин
Лизин
Глутаминовая кислота
Фенилаланин |
|
Тирозин
Триптофан |
Все аминокислоты, как в твердом состоянии, так и в растворе, существуют в виде внутренних солей (биполярных ионов, цвиттер-ионов, амфионов) и кристаллизуются в ионную кристаллическую решетку.
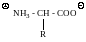
В зависимости от характера среды аминокислоты превращаются в катионы или анионы и при наложении электрического поля могут перемещаться к катоду или аноду, что используют для разделения смесей аминокислот.
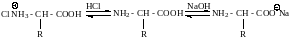
Получение аминокислот
1. Гидролиз пептидов и белков .