
- •1. Понятие об электродном потенциале. Равновесный электродный потенциал.
- •2. Гальванический элемент Якоби-Даниэля.
- •3. Газовые электроды: водородный, кислородный
- •4. Эдс гальванического элемента. Связь эдс с энергией Гиббса
- •5. Водородный электрод. Стандартные потенциалы металлов.
- •6. Ряд напряжений металлов. Уравнение Нернста.
- •7. Концентрационный гальванический элемент.
- •8. Окислительно-восстановительные г.Э.
- •9. Поляризация электродов в г.Э.
- •10. Понятие об электролизе. Электролиз расплавов солей.
- •11. Электролиз водных растворов солей.
- •12. Поляризация электродов при электролизе. Потенциал разложения.
- •13. Электролиз с растворимыми анодами.
- •14. Электрохимическое рафинирование металлов.
- •15. Практическое применение электролиза.
- •16. Влияние кислотности среды на процесс коррозии.
- •17. Устройство и принцип действия свинцового аккумулятора.
- •18. Устройство и принцип действия сухого марганцево-цинкового элемента.
- •19. Устройство и принцип действия щелочных аккумуляторов.
- •20. Химическая и электрохимическая коррозия металлов.
- •21. Коррозия металлов в кислой и нейтральной среде.
- •22. Коррозия технического железа.
- •23. Электрохимическая коррозия при контакте двух металлов.
- •27. Диэлектрики и полупроводники.
- •28. Полупроводники примесного типа.
- •29. Собственные полупроводники.
- •30. Закон сохранения энергии. Энтальпия системы.
- •31. Закон Гесса. Термодинамические уравнения.
- •32. Энтропия и её изменение при химических процессах.
- •33. Энергия Гиббса и энергия Гельмгольца.
- •34. Связь между различными термодинамическими функциями.
- •35. Скорость гомогенных химических реакций.
- •36. Молекулярность и порядок реакций. Константа скорости реакции первого порядка.
- •37. Скорость гетерогенных химических реакций.
- •38. Зависимость скорости химической реакции от температуры. Правило Вант-Гоффа и уравнение Аррениуса.
- •39. Энергия активации химических реакций.
- •40. Химическое равновесие, константа равновесия, её связь с термодинамическими функциями.
- •41. Смещение химического равновесия. Принцип Ле-Шателье.
- •42. Зонная теория кристаллов.
- •43. Типы и свойства кристаллов.
- •44. Строение кинофотоматериалов.
- •45. Химизм основных стадий фотографического процесса.
- •46. Связь между различными термодинамическими функциями.
- •47. Структура и свойства полимеров.
- •48. Химические свойства полимеров.
- •49. Материалы на основе полимеров.
- •50. Методы получения полимеров.
44. Строение кинофотоматериалов.
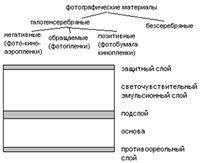
В качестве основы могут быть использованы стеклянные пластинки толщиной 0,8-1 мм. Полимерная пленка из триацетата целлюлозы или полиэтилентерефталата. Толщина таких пленок 50-150 микрон. В качестве основы может быть использована бумага/картон (150-600 микрон). В качестве основы может быть использована ткань, керамика, металл. Важнейшим слоем является эмульсионный, светочувствительный слой – суспензия микрокристаллов галогенида серебра в природном полимере – желатине (3-25 микрон). В качестве галогенидов серебра используются для малочувствительных пленок AgCl b AgBr, для высокочувствительных – AgBr+AgI. Чувствительность материала зависит от величины кристаллов галогенида серебра (0,1-2 микрон). Важную роль в фотоматериале несет желатин, он выполняет несколько функций: - Является носителем галогенидов серебра, обволакивает кристаллы галогенида серебра – предотвращает их от слипания - содержит светочувствительные примеси, которые позволяют увеличивать светочувствительность материала - создает взаимодействие основы с эмульсионным слоем Желатин – природный, белковый материал, который получают при гидролизе кологена. Противоореольный слой и защитный слои служат для защиты от механических повреждений.
45. Химизм основных стадий фотографического процесса.
основные стадии фотографического процесса: 1) фотолиз 2) проявление 3) фиксирование и проявка при фотолизе в фотографическом материале образуется скрытое фотографическое изображение. Центрами такого изображения являются атомы серебра. Механизм образования скрытого фотографического изображения: кванты света, попадая на кристалл серебра выбивают е (AgBr Br+hν->Br+e), который попадает в зону проводимости кристалла, движется по кристаллу и находит «ловушку», где взаимодействует с ионом серебра, в результате выделяется атом серебра. В качестве «ловушек» служат примеси в желатин или дефекты кристаллической решетки. В эту же «ловушку» может попасть еще несколько е, в результате выделяется еще несколько атомов серебра кристалл в дальнейшем может быть проявлен, он будет являться центром светочувствительности, если в нем образовалось минимум 4 атома серебра. Обычно образуется 6-12 атомов серебра. Большая часть галогенидов серебра не будут являться центрами скрытого изображения – не проявятся. Чем больше квантов света попадает на кристаллы, тем больше кристаллов будут иметь скрытое изображение. Стадия проявления – получение видимого фотографического изображения. При этом количество атомов серебра увеличивается в 109 раз. Проявление – избирательный процесс восстановления галогенида серебра. Восстанавливаются только те кристаллы, которые имеют центр скрытого изображения. Проявление осуществляется в специальных растворах – проявителях. В состав проявителя входят: 1) проявляющее вещество (специально подобрано таким образом, чтобы восстановились только кристаллы, имеющие центр скрытого изображения) – гидрохенон, митол. 2) антиокислитель (предотвращает процесс окисления) – аскорбиновая кислота, сульфат натрия и другие. 3) ускоряющие вещества – щелочи (при увеличении рН среды – скорость возрастает) 4) активирующие вещества
в результате проявления образуется серебряное металлическое изображение. Однако в эмульсионном слое остается большое число галогенидов серебра, не ставших центрами скрытого изображения, по этому эти галогениды серебра надо удалить. На стадии фиксирования галогениды серебра переводят в комплексные соединения, хорошо растворимые в воде, с тем, чтобы в дальнейшем их удалить на стадии промывки. В качестве фиксирующего вещества используется тиосульфат натрия (Na2S2O3)
AgBr + 2Na2S2O3 -> Na3[Ag(S2O3] + NaBr
От количества используемого тиосульфата натрия зависит скорость фиксирования (40-50 % vmax). В цветной фотографии используются 3 эмульсионных светочувствительных слоя – зеленый – синий – красный. При изготовлении в каждый из этих слоев вносится цветообразующий компонент – бесцветное вещество. Кроме него в каждом эмульсионном слое имеются галогениды серебра (на прядок меньше, чем в черно-белой фотографии) В цветной фотографии используются другие проявляющие вещества. Во время экспонирования в каждом из 3х эмульсионных слоев образуется скрытое изображение. Процесс проявления происходит одновременно в 3х эмульсионных слоях, в результате образуются атомы серебра и окисленная форма проявляющего вещества, которое взаимодействует с цветообразующей компонентой – образуется краситель (зеленый, синий, красный). Процесс отбеливания – удаление атомов серебра (перевод их в растворенную форму) Фиксирование.
