
- •1. Понятие об электродном потенциале. Равновесный электродный потенциал.
- •2. Гальванический элемент Якоби-Даниэля.
- •3. Газовые электроды: водородный, кислородный
- •4. Эдс гальванического элемента. Связь эдс с энергией Гиббса
- •5. Водородный электрод. Стандартные потенциалы металлов.
- •6. Ряд напряжений металлов. Уравнение Нернста.
- •7. Концентрационный гальванический элемент.
- •8. Окислительно-восстановительные г.Э.
- •9. Поляризация электродов в г.Э.
- •10. Понятие об электролизе. Электролиз расплавов солей.
- •11. Электролиз водных растворов солей.
- •12. Поляризация электродов при электролизе. Потенциал разложения.
- •13. Электролиз с растворимыми анодами.
- •14. Электрохимическое рафинирование металлов.
- •15. Практическое применение электролиза.
- •16. Влияние кислотности среды на процесс коррозии.
- •17. Устройство и принцип действия свинцового аккумулятора.
- •18. Устройство и принцип действия сухого марганцево-цинкового элемента.
- •19. Устройство и принцип действия щелочных аккумуляторов.
- •20. Химическая и электрохимическая коррозия металлов.
- •21. Коррозия металлов в кислой и нейтральной среде.
- •22. Коррозия технического железа.
- •23. Электрохимическая коррозия при контакте двух металлов.
- •27. Диэлектрики и полупроводники.
- •28. Полупроводники примесного типа.
- •29. Собственные полупроводники.
- •30. Закон сохранения энергии. Энтальпия системы.
- •31. Закон Гесса. Термодинамические уравнения.
- •32. Энтропия и её изменение при химических процессах.
- •33. Энергия Гиббса и энергия Гельмгольца.
- •34. Связь между различными термодинамическими функциями.
- •35. Скорость гомогенных химических реакций.
- •36. Молекулярность и порядок реакций. Константа скорости реакции первого порядка.
- •37. Скорость гетерогенных химических реакций.
- •38. Зависимость скорости химической реакции от температуры. Правило Вант-Гоффа и уравнение Аррениуса.
- •39. Энергия активации химических реакций.
- •40. Химическое равновесие, константа равновесия, её связь с термодинамическими функциями.
- •41. Смещение химического равновесия. Принцип Ле-Шателье.
- •42. Зонная теория кристаллов.
- •43. Типы и свойства кристаллов.
- •44. Строение кинофотоматериалов.
- •45. Химизм основных стадий фотографического процесса.
- •46. Связь между различными термодинамическими функциями.
- •47. Структура и свойства полимеров.
- •48. Химические свойства полимеров.
- •49. Материалы на основе полимеров.
- •50. Методы получения полимеров.
23. Электрохимическая коррозия при контакте двух металлов.
Электрохимическая коррозия протекает в среде электролита и сопровождается возникновением микротоков внутри металла
Коррозия может возникать также при контакте двух разнородных металлов или в результате химической неоднородности металла. Каждый металл имеет определенные электрические свойства, характеризуемые рядом напряжений. Роль анода выполняет металл, φ которого меньше, при этом металл в виде ионов переходит в раствор. Катодная реакция протекает на металле, φ которого больше. В зависимости от кислотности среды могут протекать два процесса. В кислотной среде (pH<7) окислителем являются ионы водорода 2H++2e=H20. Если среда нейтральная (рН=7), то окислителем является кислород воздуха O2+2H2O+4e=4OH-.
24. Защитные покрытия от коррозии.
1) Катодные
Покрытия, материал которых имеет φ больше φ материала защищаемого изделия (Sn, Pb, Cu, Ag, Ar). Защищают основной металл только механически. При нарушении материала покрытия коррозии подвергается изделие.
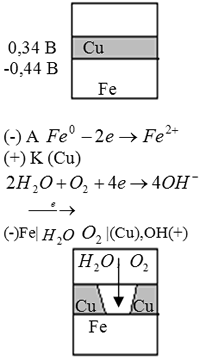
2) Анодные
Покрытия, материал которых имеет φ меньше φ материала защищаемого изделия (Zn, Cr). Защищают не только механически но и электрически. При нарушении материала покрытия коррозии подвергается материал покрытия.

25. Электрохимическая защита металлов от коррозии.
1) Анодная (протекторная)
К защищаемому изделию подсоединяют протектор – листы металла, имеющего φ меньше φ изделия. Возникает Г. Э., в котором протектор выполняет роль анода и постепенно окисляется (Mg, Zn, Al).
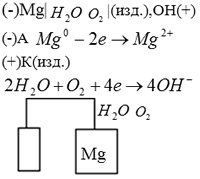
1) Катодная (защита с постоянным электрическим током)
Защищаемое изделие подсоединяется к отрицательному полюсу источника постоянного тока, и на него постоянно подаются е, тем самым тормозится процесс окисления. Fe - 2e = Fe2+.
26. Металлы, металлическая связь.
К металлам относятся около 80 элементов, которые обладают следующими свойствами : 1 высокая тепло- и электропроводность 2 металлический блеск 3 высокая ковкость элементы, имеющие небольшое число электронов на внешнем валентном слое (1-3) и большое число вакантных (незаполненных) орбиталей
при кристаллизации атомы упаковываются с максимальной плотностью так, чтобы небольшое число свободных е было доступно для нескольких соседних атомов (8-12) – координационное число свободные е оказываются не фиксированными у определенного атома и они могут перемещаться внутри кристалла – электродный газ химическая связь – металлическая по энергии кристаллической решетки металлы занимают промежуточные состояния между ковалентными и ионными кристаллами
