
- •3. Свойства органических соединений различных классов и методы их синтеза
- •3.1 Галогенопроизводные углеводородов
- •3.1.1.Свойства галогенопроизводные углеводородов
- •3.2.Тема: Эфиры с открытой цепью и циклические эфиры
- •3.2.1.Теоретическая часть
- •3.2.2. Практическая часть. Получение простого эфира Лабораторная работа №4 «Получение бутилового эфира»
- •3.2.3. Практическая часть. Получение сложных эфиров
- •Литература
3. Свойства органических соединений различных классов и методы их синтеза
3.1 Галогенопроизводные углеводородов
Галогенопроизводными называют органические соединения, молекулы которых содержат один или несколько атомов галогена, заместивших атомы водорода органического соединения. Введение атомов галогена в молекулу органические соединения с образованием связи углерод –галоген называется реакцией галогенирования.
В зависимости от числа водородных атомов в углеводороде, заме-щенных на галогены, различают моно- и полигалогенопроизводные (ди-, три- и более).
Характер радикала, связанного с галогеном, определяет предельность. Моногалогенопроизводные предельных углеводородов (моногалогеналкилы) образуют гомологический ряд, который выражают общей формулой CnH2n+1X, где X — галоген.
Атом галогена может быть связан с первичным, вторичным и третичным углеродным атомом. Поэтому галогеналкилы делятся на первичные (I), вторичные (II) и третичные (III):

Прочность связи С—X (в кДж/моль) возрастает от иода к фтору:
С–I С–Вr С–Сl С–F
214 285 340 485
(напомним: прочность связи С–Н в алканах составляет 415—420 кДж/моль).
Таким образом, наиболее реакциопноспособными являются иодпро-изводные (атом иода отщепляется легче), а самыми прочными — фторпроизводные.
Связь С–Х в галогеналкилах отличается повышенной полярностью. Это связано со значительной электроотрицательностью атома галогена, соединенного с углеродом. Поэтому электронная плотность в галогеналкилах смещена в сторону атома галогена, который проявляет — I-индуктивный эффект:
δ+ δ-
R–СН2→Х
В результате связь С—X становится поляризованной и это проявляется высокой реакционной активностью в химических реакциях. Поляризуемость связи С—X изменяется в ряду:
С – I > С – Вr > С – Сl > С – F
Моногалогеналкилы можно получать следующими способами:
1. Замещением атомов водорода в алканах на галоген. Например, в
промышленности широко применяется реакция хлорирования метана:
![]()
При определенных условиях реакция идет с образованием одного из продуктов хлорирования (СН3С1, CH2Cl2 или СНС13). Этот способ используется и для получения этилхлорида C2H5CI.
2. Присоединением галогеноводородов к алкенам:
![]()
В зависимости от условий эта реакция может протекать по правилу Марковникова или против него.
3. Замещением гидроксильной группы в спиртах на галоген. При действии на спирты пентахлорида фосфора PCI5 или галогеноводорода гидро ксильная группа в молекуле спирта замещается на атом галогена:
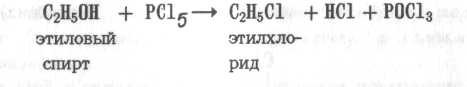
![]()
Действием фторидов серебра (ртути, кобальта и др.) на галогенал-килы получают фтористые алкилы:
С2Н5–Br + АgF→ С2Н5– F + АgBr
этил фторид
Прямое фторирование углеводородов затруднено. Это связано с высокой активностью фтора — реакция часто сопровождается взрывом.
Существующие способы получения галогенопроизводных делятся на две группы:
1) прямое галогенирование – замещение атомов водорода на галогены и присоединение галогенов или галогеноводородов по кратным связям ненасыщенного соединения;
2) непрямое галегенирование – замещение галогеном различных групп (ОН, Н2) и отдельных атомов, кроме водорода (атомов кислорода, других галогенов).
