
- •Ю.С. Рыбаков процессы и аппараты защиты окружающей среды
- •280202 – Инженерная защита окружающей среды Екатеринбург
- •Оглавление
- •Глава 1. Научные основы технологических процессов . . . 10
- •1.2.1. Теплопроводность . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 15
- •1.4. Процессы разделения неоднородных и гетерогенных систем . . . . . . . . . 35
- •Глава 2. Защита атмосферного воздуха от загрязнения . . . 61
- •Глава 3. Защита водного бассейна от загрязнения . . . . . . . . . 102
- •Глава 4. Утилизация и ликвидация бытовых
- •Глава 5. Защита окружающей среды от энергетического
- •Предисловие
- •Введение
- •Глава 1. Научные основы технологических процессов
- •1.1. Основные понятия и законы природоохранных технологий
- •1.1.1. Два вида переноса вещества и энергии
- •Это уравнение будем называть материальным балансом. Из уравнения (1.1) видно, что в процессе производства происходит перенос массы из одних компонентов, входящих в аппарат, в другие.
- •1.1.2. Движущая сила технологического процесса
- •1.1.3. Закономерности переноса массы и энергии
- •1.1.4. Классификация и принципы оптимизации основных
- •Классификация основных процессов природоохранных технологий
- •1.2. Теплообменные процессы
- •1.2.1. Теплопроводность
- •1.2.2. Конвекция
- •1.2.3. Тепловое излучение
- •1.2.4. Теплоносители и их свойства
- •1.2.5. Теплоотдача при конденсации пара
- •1.2.6. Теплопередача при кипении жидкостей
- •1.2.7. Процессы выпаривания
- •1.3. Массообменные процессы
- •1.3.1. Массопередача, массоотдача и массопроводность
- •1.3.2. Абсорбция
- •1.3.3. Ректификация
- •1.3.4. Адсорбция
- •1.3.5. Ионный обмен
- •1.3.6. Экстракция
- •1.3.7. Сушка
- •1.3.8. Кристаллизация
- •1.4. Процессы разделения неоднородных и гетерогенных систем
- •1.4.1. Классификация неоднородных и гетерогенных систем
- •Классификация неоднородных и гетерогенных систем
- •1.4.2. Процессы осаждения под действием силы тяжести
- •1.4.3. Фильтрование
- •1.4.4. Коагуляция и флокуляция
- •1.4.5. Флотация
- •1.5. Химические и биохимические процессы, протекающие при очистке вод
- •1.5.1. Химические процессы
- •1.5.2. Сущность отдельных химических процессов и их роль
- •1.5.3. Биохимические процессы
- •1.6. Воздействие транспорта на окружающую среду
- •1.6.1. Влияние предприятий железнодорожного транспорта
- •1.6.2. Основные процессы, протекающие при воздействии
- •1.6.3. Характеристика топлив, используемых на объектах транспорта
- •1.6.4. Характеристика основных токсичных веществ, содержащихся
- •Глава 2. Защита атмосферного воздуха от загрязнения
- •2.1. Общие вопросы защиты атмосферы от загрязнения
- •2.1.1. Источники загрязнения атмосферы
- •2.1.2. Нормирование качества атмосферного воздуха
- •Предельно допустимые концентрации некоторых веществ в воздухе, мг/м3
- •2.1.3. Классификация источников загрязнения
- •2.2. Пассивные методы защиты атмосферы от загрязнения
- •2.2.1. Стадия проектирования предприятия
- •2.2.2. Инвентаризация и расчет предельно допустимых выбросов
- •2.2.3. Установление санитарно-защитной зоны вокруг предприятия
- •2.2.4. Расчет высоты трубы для рассеивания газовоздушных выбросов
- •2.3. Методы очистки отходящих газов от аэрозолей
- •2.3.1. Сухие пылеуловители
- •2.3.2. Мокрые пылеуловители
- •2.3.3. Электрофильтры
- •2.3.4. Фильтры
- •3.6. Туманоуловители
- •2.4. Очистка промышленных выбросов от токсичных газовых примесей
- •2.4.1. Метод абсорбции
- •2.4.2. Метод хемосорбции
- •2.4.3. Адсорбционные методы
- •2.4.4. Методы каталитической очистки газов
- •2.4.5. Метод термической очистки газов
- •2.5. Методы и устройства для очистки выхлопных газов карбюраторных и дизельных двигателей
- •2.5.1. Нейтрализаторы отработавших газов
- •2.5.2. Фильтры для улавливания дисперсных частиц
- •2.5.3. Использование новых рабочих процессов и видов энергоресурсов
- •2.5.4. Очистка отработавших газов при реостатных
- •Глава 3. Защита водного бассейна от загрязнения
- •3.1. Общие вопросы защиты водных объектов от загрязнения
- •3.1.1. Характеристика водопользования и водопотребления
- •3.1.2. Критерии качества воды
- •Критерии оценки загрязненности воды по пдк вредных веществ
- •3.1.3. Качество вод, используемых в промышленности
- •3.2. Пассивные методы защиты гидросферы от загрязнения
- •3.2.1. Особенности канализования сточных вод
- •3.2.2. Условия выпуска производственных сточных вод
- •3.2.3. Расчет предельно допустимого сброса вредных веществ
- •3.2.4. Установление водоохранных зон и прибрежных защитных полос
- •3.3. Классификация сточных вод
- •3.3.1. Классификация по принципу допустимости
- •3.3.2. Классификация сточных вод по дисперсному составу примесей
- •3.3.3. Классификация сточных вод в зависимости
- •4. Механические (физические) методы очистки сточных вод
- •3.4.1. Процеживание и отстаивание примесей
- •4.2. Осветление сточных вод, улавливание жиров и нефтепродуктов
- •4.3. Фильтрование
- •4.4. Гидроциклонирование
- •3.5. Химические, физико-химические и биологические методы очистки и обезвреживания сточных вод
- •3.5.1. Химическая очистка сточных вод
- •3.5.2. Физико-химические методы очистки
- •3.5.3. Методы биологической очистки сточных вод
- •3.5.4. Методы биологической очистки сточных вод
- •3.5.5. Доочистка сточных вод
- •Глава 4. Утилизация и ликвидация твердых отходов
- •4.1. Опасность отходов для окружающей природной среды
- •4.1.1. Источники возникновения твердых отходов
- •4.1.2. Классификация отходов
- •4.1.3. Нормирование допустимого количества отходов
- •Классификация опасности отходов производства
- •4.2. Основные технологические принципы утилизации, обезвреживания и захоронения отходов
- •2.1. Размещение отходов
- •4.2.2. Переработка отходов на месте складирования
- •4.2.3. Переработка отходов пластических масс
- •4.2.4. Сжигание отходов
- •4.2.5. Обезвреживание и захоронение радиоактивных отходов
- •4.3. Утилизация и ликвидация осадков сточных вод
- •4.3.1. Технологический цикл обработки осадков сточных вод
- •4.3.2. Уплотнение, стабилизация и кондиционирование осадков
- •4.3.3. Обезвоживание и ликвидация осадков сточных вод
- •Глава 5. Защита окружающей среды от энергетического воздействия
- •5.1. Защита окружающей среды от шума и вибраций
- •5.1.1. Шум и его характеристики
- •5.1.2. Нормирование шума
- •5.1.3. Расчет шумовых характеристик
- •5.1.4. Меры борьбы с шумовым загрязнением
- •5.2. Защита от электромагнитного загрязнения
- •5.2.1. Электромагнитное загрязнение среды и его источники
- •5.2.2. Предельно допустимые уровни электромагнитных полей
- •5.2.3. Защита от электромагнитных полей
- •Заключение
- •Библиографический список
- •620034, Екатеринбург, ул. Колмогорова, 66 УрГупс
- •Ю.С. Рыбаков
- •Процессы и аппараты защиты
- •Окружающей среды
- •Екатеринбург
3.5.2. Физико-химические методы очистки
К физико-химическим методам очистки относятся: коагуляция, флокуляция, сорбция, флотация, экстракция, ионный обмен, гиперфильтрация, ультрафильтрация, эвапорация, термоокисление, выпаривание, испарение, кристаллизация, высаливание, вымораживание, магнитная обработка, а также методы, связанные с наложением электрического поля – электрокоагуляция, электрофлотация, электродиализ и другие.
Коагуляция – слипание частиц коллоидной системы при их столкновении в процессе теплового движения, перемешивания или направленного перемещения во внешнем силовом поле. В результате коагуляции образуются агрегаты – более крупные (вторичные) частицы, состоящие из скопления мелких (первичных). Первичные частицы в таких агрегатах соединены силами межмолекулярного взаимодействия непосредственно или через прослойку окружающей дисперсной среды. Коагуляция сопровождается прогрессирующим укрупнением частиц и уменьшением общего их числа в объеме дисперсной среды. Слипание однородных частиц называется гомокоагуляцией, а разнородных – гетерокоагуляцией.
Для очистки сточных вод применяют следующие коагулянты:
1. Соли алюминия: сульфат алюминия (глинозем) Al2(SO4)3 ∙18H2O, алюминат натрия NaAlO2, оксихлорид алюминия Al2(OH)2Cl, полихлорид алюминия [Al2(OH)nCl6-n]m(SO4)x где 1<n<5m<10, алюмокалиевые [AlK(SO4)2 ∙18H2O] и алюмоаммонийные [Al(NH4)(SO4)2 ∙12H2O] квасцы.
2. Соли железа: сульфат двухвалентного железа FeSO4 ∙7H2O, гидроксид железа, хлорид железа FeCl3∙6H2O, сульфат трехвалентного железа Fe2(SO4)3∙9H2O.
3. Соли магния: хлорид магния MgCl2∙6H2O, сульфат магния MgSO4∙∙7H2O.
4. Известь – Са(ОН)2 .
5. Шламовые отходы и отработанные растворы отдельных производств, содержащие перечисленные выше реагенты.
Количество коагулянта зависит от его вида, расхода, состава и требуемой очистки воды и определяется экспериментально.
Флокуляция – процесс, при котором мелкие частицы, находящиеся во взвешенном состоянии, под влиянием специально добавляемых неорганических и органических веществ–флокулянтов образуют интенсивно оседающие рыхлые хлопьевидные скопления.
Типы флокулянтов:
1. Неорганические флокулянты – активная кремниевая кислота или жидкое стекло mNa2O ∙ nSiO2. m , n модули жидкого стекла (чаще всего равны 2 и 5);
2. Вещества, получаемые из растительного сырья – крахмал, эфиры;
3. Синтетические органические флокулянты – полиакриаламид, полиэтиленамин.
Коагуляцию и флокуляцию взвешенных частиц в сточных водах проводят в специальных камерах смешения. После камер смешения сточные воды направляют на осветление в отстойниках или фильтрах с зернистой загрузкой, то есть на механическую очистку.
Сорбция – процесс поглощения вещества из окружающей среды твердым телом или жидкостью. Поглощающее тело называется сорбентом, а поглощаемое – сорбатом. Различают поглощение вещества всей массой жидкого сорбента (абсорбция) и поверхностным слоем твердого или жидкого сорбента (адсорбция). Сорбция, сопровождающаяся химическим взаимодействием сорбента с поглощаемым веществом, называется хемосорбцией.
В качестве сорбентов применяют различные искусственные и природные пористые материалы: золу, коксовую мелочь, торф, силикагели, алюмогели, активные глины. Эффективными сорбентами являются активированные угли различных марок.
Активность сорбента характеризуется количеством поглощаемого вещества на единицу объема или массы сорбента (кг/т), и она колеблется в пределах от 1 до 50 кг/т.
Процесс сорбции может осуществляться в статических условиях, при которых частица жидкости не перемещается относительно частицы сорбента (аппараты с перемешивающими устройствами), а также в динамических условиях, при которых частица жидкости перемещается относительно сорбента. Поэтому различают статическую и динамическую активность сорбента. При этом динамическая активность составляет 45–90% относительно статической.
Следует указать, что сорбционные процессы являются обратимыми, то есть сорбат может переходить с сорбентом обратно в раствор. Скорости протекания сорбционного и десорбционного процессов пропорциональны концентрации веществ в растворе и на поверхности сорбента. Наиболее простым адсорбером является насыпной фильтр, схема которого приведена на рис. 3.18.
Скорость фильтрования через фильтры – 1– 6 м/ч, а крупность зерен сорбента составляет 1,5–5 мм. Основные характеристики сорбционных фильтров типа ФСУ представлены в табл. 3.6.
Таблица 3.6
Конструктивные и технологические показатели сорбционных фильтров
с активированным углем
Марка фильтра |
Диаметр, мм |
Площадь, м2 |
Высота слоя сорбента, м |
Объем, м3 |
|
фильтра общий |
сорбционного слоя |
||||
ФСУ-2-0,6 |
2000 |
3,14 |
2,5 |
10,7 |
7,85 |
ФСУ-2,6-0,6 |
2600 |
5,3 |
2,5 |
19,0 |
13,2 |
ФСУ-3-0,6 |
3000 |
7,1 |
2,5 |
26,0 |
17,8 |
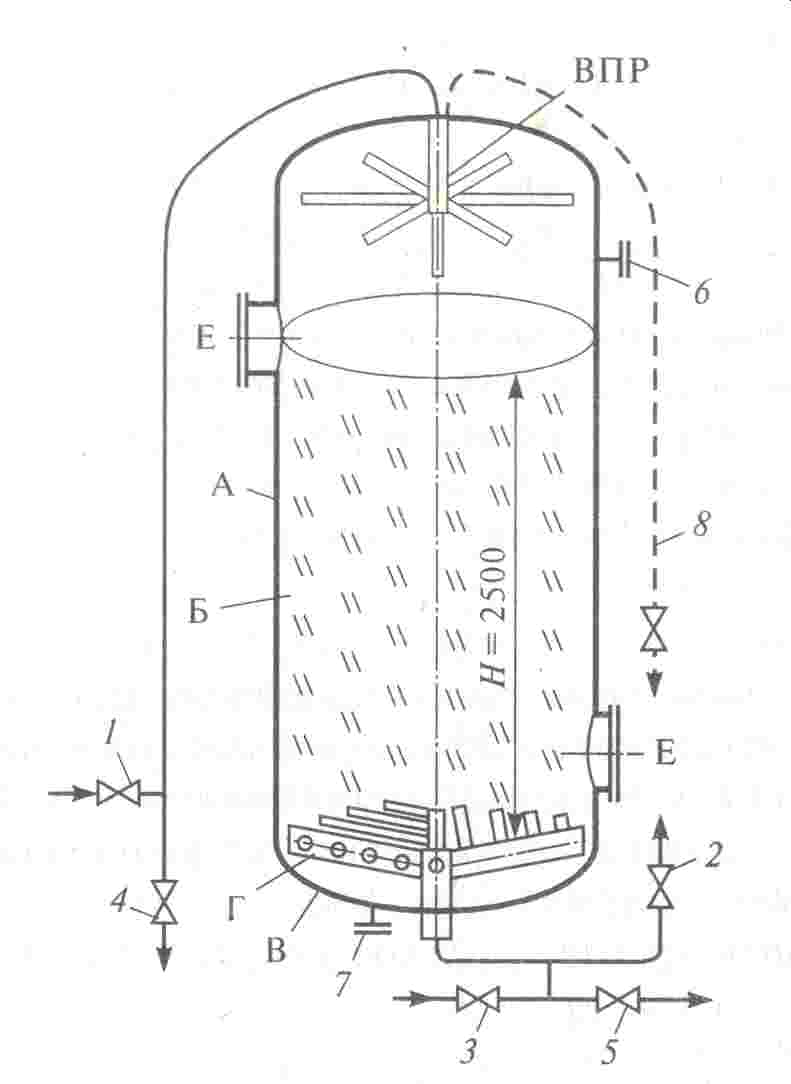
Рис. 3.18. Схема насыпного сорбционного фильтра (типа ФСУ)
1 – вход обрабатываемой воды (конденсата); 2 – выход обрабатываемой воды (конденсата); 3 – подача промывочно-взрыхляющей воды; 4 – сброс промывочной воды; 5 – спуск первого фильтрата и опорожнение фильтра; 6, 7 – штуцеры для гидрозагрузки и гидровыгрузки активированного угля; 8 – воздушник; А – корпус; Б – активированный уголь; В – нижнее днище; Г – нижний дренаж (копирующий); ВРП – верхнее распредустройство; Е – лаз
Сорбционная очистка может быть регенеративной, когда извлеченные вещества утилизируются или десорбируются, или деструктивной, когда извлеченные вещества уничтожаются. В зависимости от назначения сорбционной очистки применяют различные методы регенерации сорбента.
К одному из видов сорбции относится ионный обмен. Ионообменная сорбция – процесс обмена между ионами, находящимися в растворе, и ионами, присутствующими на поверхности твердой фазы – ионита.
Очистка сточных вод методом ионного обмена позволяет извлекать и утилизировать ценные примеси, ПАВ, радиоактивные вещества, очищать сточную воду до ПДК с последующим использованием ее в технологических процессах или в системах оборотного водоснабжения.
По знаку обменивающихся ионов иониты делятся на катиониты и аниониты. Ведущая роль принадлежит синтетическим органическим ионитам – ионообменным смолам, которые подразделяются на следующие виды:
сильнокислотные катиониты, содержащие сульфогруппы SO3H и сильноосновные аниониты, содержащие четвертичные аммониевые основания;
слабокислотные катиониты, содержащие карбоксильные СООН и фенольные группы, диссоциирующие при рН>7, а также слабоосновные аниониты, содержащие первичные NH2 и вторичные NН аминогруппы, диссоциирующие при рН <7;
иониты смешанного типа, проявляющие свойства смеси сильных и слабых кислот или оснований.
Иониты характеризуются полной и рабочей емкостью. Полная емкость – количество ионов, которое может поглотить 1 кг ионита до полного насыщения, а рабочая емкость – количество находящихся в воде ионов, которое может поглотить 1 кг ионита до начала проскока в фильтрат.
Если катиониты находятся в Н- или Na-форме, обмен катионов будет проходить по реакциям (1.43-1.44).
Регенерация катионитов осуществляется промывкой кислотой (при Н-катионите) или раствором хлористого натрия (при Na-катионите) по реакциям (1.45-1.46).
Поскольку в сточных водах, как правило, содержится несколько катионов, большое значение имеет селективность их поглощения. Для каждого вида катионита установлены ряды катионов по энергии их вытеснения.
Слабоосновные аниониты поглощают анионы сильных кислот.
Регенерация слабоосновных анионитов достигается фильтрованием через слой анионита 2-4%-ных водных растворов NaOH, Na2CO3, NH4OH.
На рис. 3.19 представлена схема ионообменной очистки сточных вод ванн хромирования от соединений хрома. Сточные воды поступают в приемный резервуар 1, откуда насосом 2 подаются в фильтр 3 для очистки от механических примесей. Очищенная от механических примесей сточная вода поступает в последовательно расположенные анионитовые фильтры 4 и 5, заполненные иономебменной смолой АВ-17 в ОН-форме. Очищенная таким образом вода вновь подается в ванну хромирования 12. Вспомогательный катионовый фильтр 6 предназначен для дополнительной обработки сточной воды в пусковой период. В бак 7 поступают выделенные соединения хрома. Бак 8 предназначен для сбора отработанного раствора. Емкости 13 – со щелочью и 14 – с кислотой предназначены для промывки фильтров. Промывной раствор нейтрализуется в баке 11, куда дозатором 9 одновременно подается необходимое для нейтрализации количество извести из бака 10.
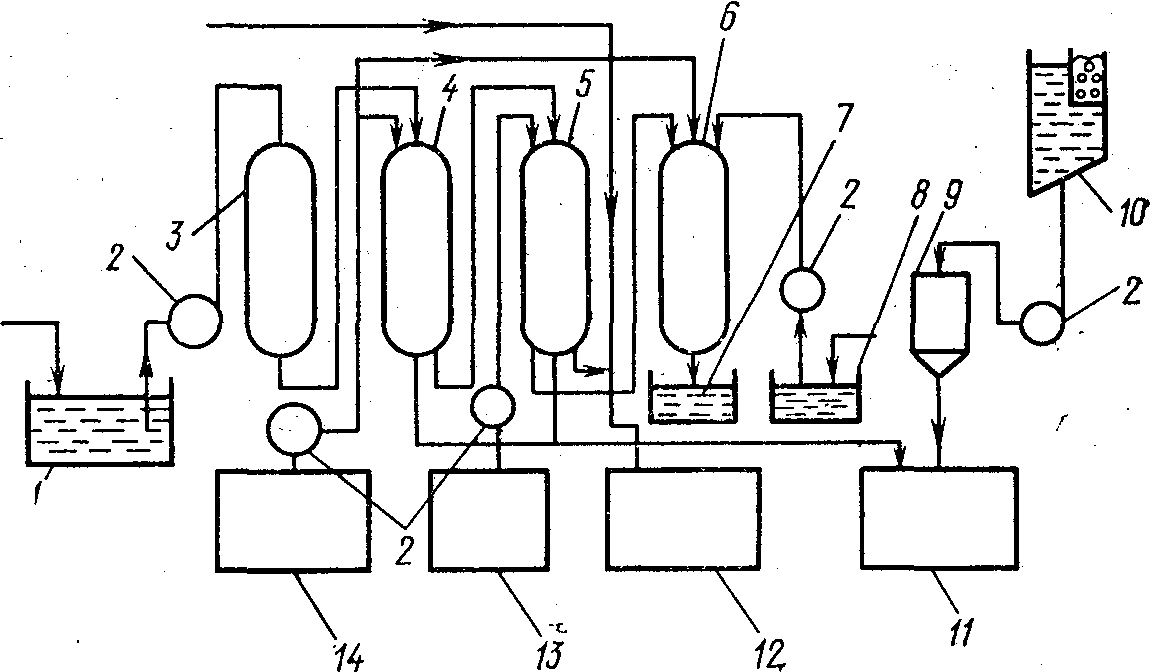
Рис. 3.19. Схема ионообменной очистки сточных вод ванн хромирования
1 – приемный резервуар; 2 – насос; 3 – фильтр; 4 и 5 – анионитовые фильтры, заполненные ионообменной смолой; 6 – катионитовый фильтр; 7 – бак для сбора соединений хрома;
8 – бак для сбора отработанного раствора; 9 – дозатор; 10 – бак для известкового молока;
11 – бак для нейтрализации промывного раствора; 12 – ванна хромирования;
13 и 14 – емкости со щелочью и кислотой
Жидкостная экстракция – процесс извлечения веществ из водного раствора в жидкую органическую фазу (раствор экстрагента), не смешивающуюся с водой. Процесс жидкостной экстракции используется для выделения из сточных вод ценных органических веществ (например, фенолов и жирных кислот), а также тяжелых цветных металлов (меди, никеля, цинка, кадмия, ртути и др.).
Экстрагент – органическое вещество, образующее с извлекаемым загрязняющим веществом соединение, способное переходить в органическую фазу. Обычно экстрагенты находятся в аморфном состоянии и требуют разбавления.
Разбавителем называют органическую жидкость, не смешивающуюся с водой и служащую растворителем экстрагента (керосин, бензол, ксилол, уайт-спирит и др.).
Органическая и водная фаза после проведения экстракционной стадии называются соответственно экстрактом и рафинатом.
Загрязняющие компоненты выделяются из экстракта двумя путями: либо ректификацией, либо реэкстракцией, в результате которых обычно достигается и регенерация экстрагента. В качестве реэкстрагирующих растворов (реэкстрактов) используют водные растворы кислот, солей и оснований. Водный раствор после реэкстракции называют реэкстрактом.
Основные количественные характеристики экстракционного процесса следующие: коэффициент распределения экстрагируемого вещества; коэффициент разделения или коэффициент селективности и степень извлечения загрязняющего вещества.
Коэффициент распределения экстрагируемого вещества (Кр) в двух несмешивающихся растворителях при достижении равновесия определяется по формуле 1.50.
Данные о коэффициенте распределения некоторых органических загрязняющих веществ между экстрагентом и водой представлены в табл. 3.7.
Таблица 3.7
Значение коээфициента распределения некоторых загрязняющих веществ между экстрагентом и водой при комнатной температуре
Экстрагируемое из воды вещество |
Экстрагент |
Коэффициент распределения |
Анилин |
Бутилацетат |
27 |
Толуол |
8-19 |
|
Бензойная кислота |
Диэтиловый эфир |
71-91 |
Бутилацетат |
30 |
|
Толуол |
6-12 |
|
Муравьиный альдегид |
Амиловый спирт |
3 |
Пикриновая кислота |
Толуол |
1,7-8,7 |
Бензол |
0,7-5,3 |
|
Хлороформ |
1,2-2,6 |
|
Пиридин |
Толуол |
1.4-9,3 |
Салициловая кислота |
Ацетон |
126 |
Толуол |
1,7-2,5 |
|
Бензол |
1,7-4,5 |
|
Хлороформ |
2,9-4,3 |
|
n-Толуидин |
Бензол |
51-61 |
Фенол |
Бутилацетат |
51 |
Амиловый спирт |
14-16 |
|
Толуол |
1,7-9,4 |
|
Бензол |
2,3-12,5 |
|
Хлороформ |
3,4-12,5 |
|
Хлоруксусная кислота |
Амиловый спирт |
3,6 |
Степень извлечения Е – это процент извлечения веществ в органическую фазу от общего его количества в обеих фазах:
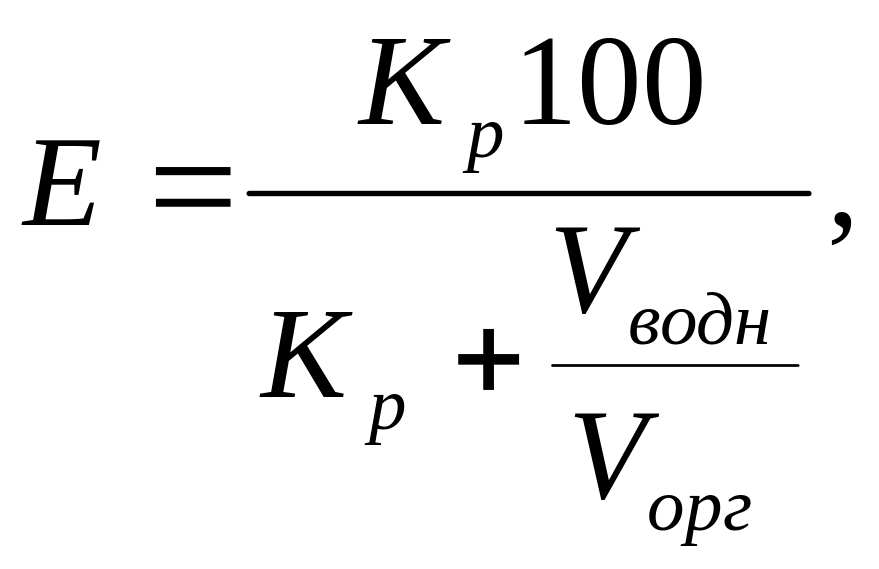 (3.18)
(3.18)
где Vводн и Vорг – соответственно объем водной и органической фаз.
Коэффициент разделения или коэффициент селективности β характеризуется отношением коэффициентов распределения двух разделяемых компонентов А и В. Так, селективность какого-либо экстрагента по отношению к компоненту В определяют из выражения
![]() .
(3.19)
.
(3.19)
Из выражения (3.19) видно, что с увеличением КрВ селективность возрастает. При β = 1 селективность равна нулю, и экстракционное разделение компонентов невозможно.
Сведения о наиболее распространенных экстрагентах, предназначенных для выделения из сточных вод тяжелых металлов, приведены в табл. 3.8.
Таблица 3.8
Основные экстрагенты, предназначенные для выделения из сточных вод
тяжелых металлов и железа
Реагент |
Структура |
Типичное применение для очистки сточных вод |
Ди (2–этилгексил) фосфорная кислота (Д2ЭГФК) |
(СН3(СН2)3СНСН2О2)2Р ==О | | СН2СН3 ОН |
Очистка сточных вод от меди, никеля и мышьяка |
Lix 64 N |
|
Очистка вод от меди и никеля |
SMЕ-529 |
|
Очистка вод от меди |
Триалкиламин (Alamine 336) |
R3N(R==C8–C10) R – углеводородный радикал |
Очистка вод от кадмия и цинка |
Четвертичные аммониевые соединения (Adogen 464) |
(R3NCH3)+Cl– (R==C8–C10) |
Очистка сточных вод от ртути |
Трибулилфосфат (ТБФ) |
(C4H9O)3P=O |
Очистка от железа, хрома, никеля, молибдена и мышьяка |
Алкилсалицилальдоксим (АСАО-РТ) |
|
Очистка от меди и цинка |
Смесь алкилфенола и карбоновой кислот (ОМГ) |
|
Очистка от меди и цинка |
За счет смешения растворенного в растворителе экстрагента с загрязненной водой происходит перераспределение загрязняющих веществ между экстрагентом и водой. По достижении равновесия концентрация экстрагируемого вещества в экстрагенте значительно выше, чем в сточной воде. После экстракции вода и насыщенный экстрагент разделяются. Затем сконцентрированное в экстрагенте вещество отделяется от растворителя на стадии реэкстракции и может быть утилизировано. Экстрагент после этого используется вновь в технологическом процессе очистки.
Флотация – процесс молекулярного прилипания частиц флотируемого материала к поверхности раздела двух фаз, обычно газа и жидкости.
Способы флотации отличаются между собой методами насыщения жидкости пузырьками воздуха определенной крупности. По этому принципу выделяются следующие способы флотации:
- флотация с выделением воздуха из раствора (вакуумные, напорные, эрлифтные флотационные установки);
- флотация с механическим диспергированием воздуха (импеллерные, безнапорные и пневматические флотационные установки);
- флотация с подачей воздуха через пористые материалы;
- электрофлотация;
- биологическая и химическая флотация.
Флотация с выделением воздуха из раствора применяется при очистке сточных вод, содержащих очень мелкие частицы загрязнений, поскольку позволяет получать самые мелкие пузырьки воздуха. На рис. 3.20 показана схема вакуумной флотации.
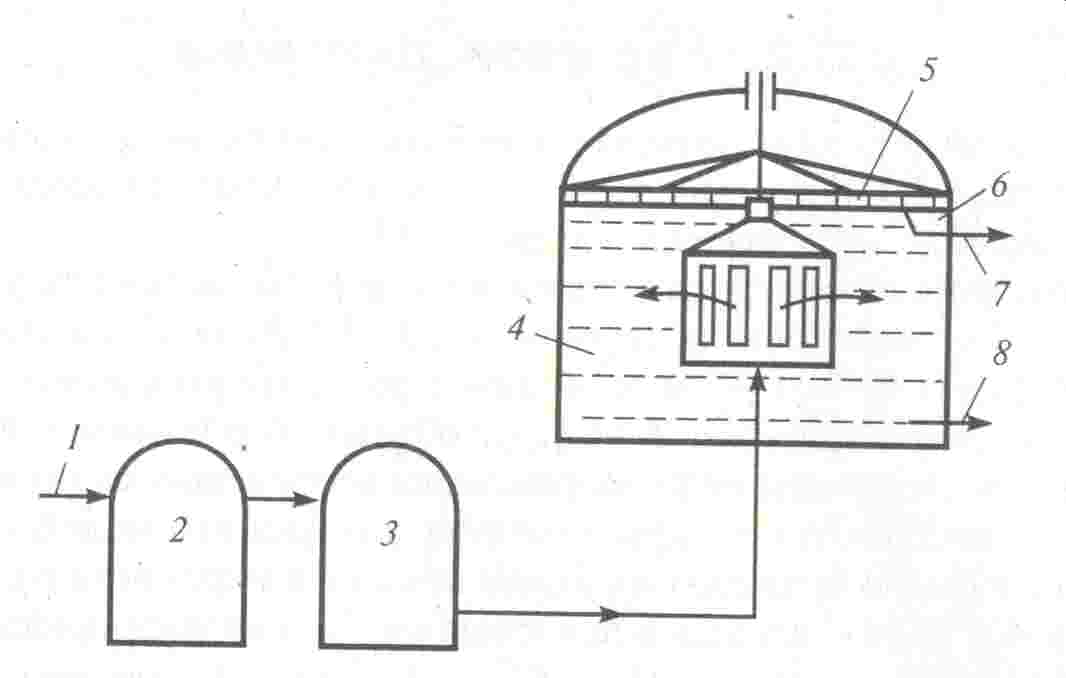
Рис. 3.20. Схема процесса вакуумной флотации
1 – подача сточной воды; 2 – аэратор; 3 – деаэратор; 4 – флотационная камера; 5 – механизм сгребания пены; 6 – пеносборник; 7 – отвод пены; 8 – отвод обработанной сточной воды
Сточную воду в течение нескольких минут (1-3 мин.) насыщают воздухом, потом ее направляют в деаэратор, где удаляется нерастворившийся воздух, и под действием разряжения (0,02-0,03 МПа) сточные воды поступают во флотационную камеру. В ней воздух под действием вакуума выделяется в виде пузырьков, которые взаимодействуют с частицами загрязнений и переносят их на поверхность жидкости в пенный слой, откуда пена вращающимися скребками удаляется в пеносборник. Продолжительность обработки сточной воды в камере 20 мин., производительность 1 м2 поверхности флотатора – до 200 м3/сут.
Напорная флотация позволяет очищать сточные воды с начальной концентрацией загрязнений 4-5 г/л и более. Схема процесса напорной флотации представлена на рис. 3.21. Сущность процесса заключается в создании перенасыщенного раствора воздуха в сточной воде (воду обрабатывают в аэрационной камере 1-3 мин. под избыточным давлением 0,3-0,5 МПа). Затем ее перемещают во флотационную камеру. Выделяющийся из такого раствора воздух образует микропузырьки, которые и флотируют содержащиеся в сточной воде загрязнения. Продолжительность флотации около 20 мин. Количество воздуха, которое должно выделиться из пересыщенного раствора, обычно составляет 3-5% объема обрабатываемой сточной воды. Расход сточной воды на 1 м2 площади камеры составляет 6-10 м3/ч.
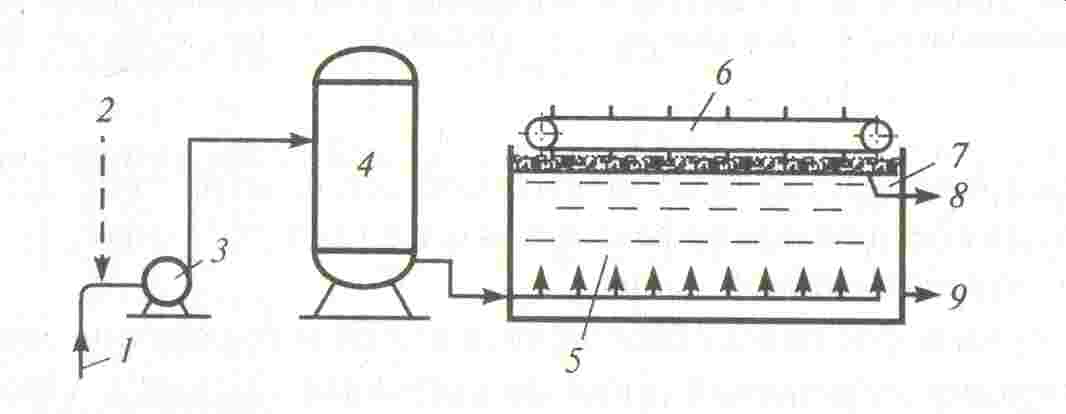
Рис. 3.21. Схема процесса напорной флотации
1 – подача сточной воды; 2 – подача воздуха; 3 – насос; 4 – сатуратор (напорный бак); 5 – флотационная камера; 6 – механизм для сгребания пены; 7 – пеносборник;
8 – отвод пены; 9 – отвод обработанной сточной воды
Флотация с механическим диспергированием воздуха. При перемещении струи воздуха в воде в ней создается интенсивное вихревое движение, под действием которого воздушная струя распадается на отдельные пузырьки. Энергичное перемешивание сточной воды во флотационных установках создает в ней большое число мелких вихревых потоков, что позволяет получить пузырьки определенной величины.
Флотация с подачей воздуха через пористые материалы отличается простотой аппаратурного оформления и относительно малым расходом энергии. Воздух во флотационную камеру подается через мелкие фильтросные пластины, трубы, насадки, уложенные на дне камеры. Величина отверстий должна быть 4-20 мкм, давление воздуха – 0,1-0,2 МПа, продолжительность флотации 20-30 мин, расход воздуха определяется экспериментально.
Пенное фракционирование (пенная сепарация) применяется для очистки сточных вод от поверхностно-активных веществ (ПАВ). При реализации этого метода протекают процессы селективной адсорбции загрязняющих воду веществ на поверхности газовых пузырьков и концентрирование указанных веществ в слое пены. Степень извлечения ПАВ при пенной сепарации можно определить из следующего выражения
![]() (3.20)
(3.20)
где СН – концентрация ПАВ в сточной воде до извлечения;
СК – остаточная концентрация растворенного ПАВ в объеме воды.
Наиболее эффективное извлечение загрязнений наблюдается в интервале рН 9,5-12,3. Положительное влияние на повышение степени извлечения оказывают добавки следующих электролитов (≤0,0005 моль/л): КСl, K2SO4, K4P2O7, KNO3, NaNO3, NH4NO3. Повышение степени извлечения загрязняющих веществ из сточных вод объясняется поглощением ионами указанных электролитов части воды за счет гидратации, в результате чего возрастает эффективная концентрация ПАВ. Степень извлечения из сточных вод ПАВ при их высокой концентрации больше, чем при извлечении из малоконцентрированных сточных вод. Кроме того, на величину Е оказывают влияние температура и вязкость очищаемой воды.
Для характеристики распределения ПАВ между пенным продуктом и сточной водой используют коэффициент распределения, который определяют по формуле
![]() (3.21)
(3.21)
где СК – концентрация ПАВ в пене.
Степень изменения объема сточной воды при проведении процесса пенного фракционирования определяется выражением
![]() (3.22)
(3.22)
где Vп – объем пенного продукта (пеноконденсата);
Vост – остаточный объем сточной воды.
Схема установки для очистки сточных вод от ПАВ методом пенной сепарации приведена на рис. 3.22. Процесс ведется в сепараторе, который состоит из нескольких камер. Высота слоя обрабатываемой воды в каждой камере составляет 0,5-0,8 м. Очищенная вода поступает в сборник, а пена под напором воздуха, создаваемого вентилятором, поступает в циклон, в котором происходит первая стадия разделения жидкой и газовой фаз, а вторая стадия разделения воды и пены происходит в отстойнике. Воду из отстойника возвращают в сепаратор, а пену – в камеру концентрирования. Как правило, ПАВ из пены не выделяют, а направляют в отходы.
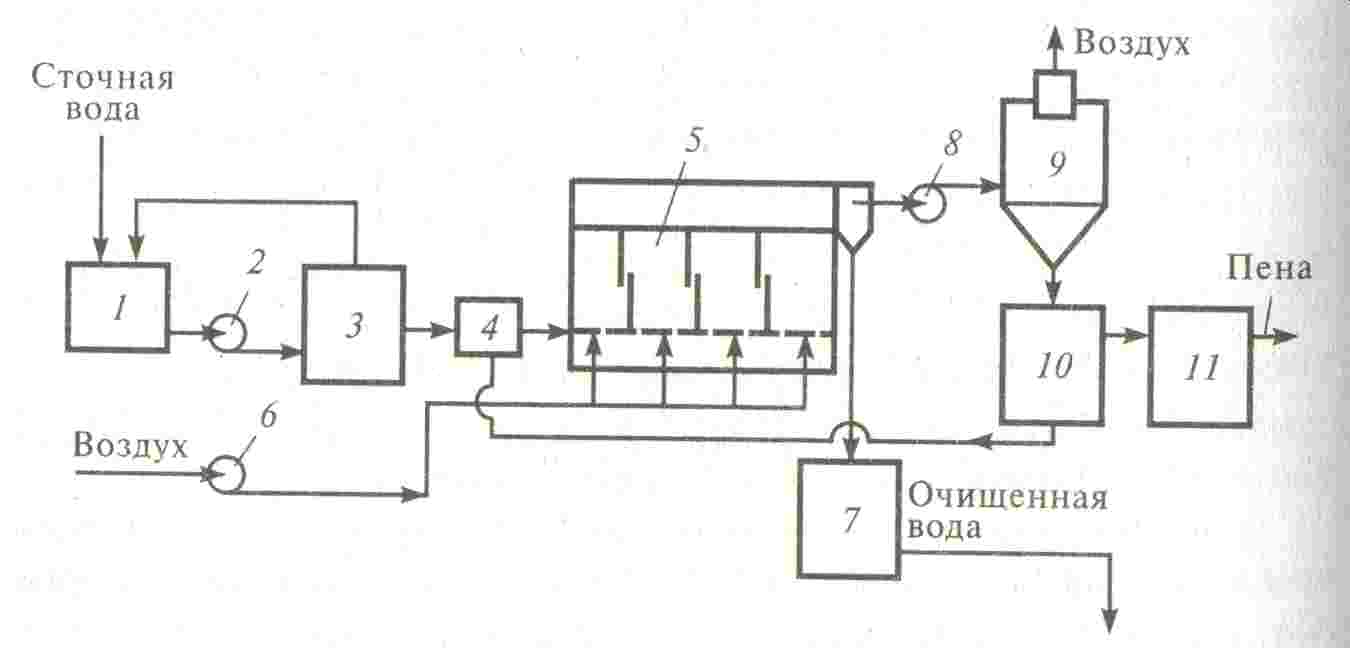
Рис. 3.22. Схема установки очистки сточных вод методом пенной сепарации
1 – емкость; 2 – насос; 3 – промежуточный сборник; 4 – расходомер; 5 - сепаратор;
6 – воздуходувка; 7 – сборник; 8 – вентилятор; 9 – циклон; 10 – отстойник;
11 – камера концентрирования пены
Электрофлотация. Сущность электрофлотационного способа очистки сточных вод заключается в переносе загрязняющих частиц из жидкости на поверхность с помощью пузырьков газа, образующихся при электролизе воды. В процессе электролиза воды на катоде выделяется водород, а на аноде – кислород. Основную роль играют мелкие пузырьки, образовавшиеся на катоде. При применении растворимых анодов (в основном железных и алюминиевых) происходит переход катионов железа и алюминия, приводящий к образованию хлопьев гидроокиси. Одновременное образование хлопьев коагулянта и пузырьков газа в стесненных условиях межэлектродного пространства создает предпосылки для надежного закрепления газовых пузырьков на хлопьях и интенсивной коагуляции загрязнений, что обеспечивает эффективность флотационного процесса. Такие установки называются электрокоагуляционно-флотационными.
Электродиализ – процесс сепарации ионов солей, осуществляемый в мембранном аппарате под действием постоянного электрического тока, применяемый для опреснения высокоминерализованных сточных вод (рис. 3.23).
Электродиализатор разделен чередующимися катионитовыми и анионитовыми мембранами, образующими концентрирующие (рассольные) и обессоливающие (дилюатные) камеры. Под действием постоянного тока катионы, двигаясь к катоду, проникают через катионитовые мембраны, но задерживаются анионитовыми, а анионы, двигаясь в направлении анода, проходят через анионитовые мембраны, но задерживаются катионитовыми. В результате этого из одного ряда камер ионы обоих знаков выводятся в один ряд камер.
Ультрафильтрация – мембранный процесс разделения растворов, осмотическое давление которых мало. Этот метод используется при отделении сравнительно высокомолекулярных веществ, взвешенных частиц, коллоидов. Ультрафильтрация по сравнению с обратным осмосом более высокопроизводительный процесс, так как высокая производительность мембран достигается при давлении 0,2-1 МПа.

Рис. 3.23. Схема процесса электродиализа
А – анионитовые мембраны; К – катионитовые мембраны;
1 – выход газообразного водорода; 2 – подача сточной воды; 3 – выход газообразных хлора и кислорода; 4 – выпуск обессоленной воды; 5 – выпуск рассола
Обратный осмос (гиперфильтрация) – непрерывный процесс молекулярного разделения растворов путем их фильтрования под давлением, через полунепроницаемые мембраны, задерживающие полностью или частично молекулы или ионы растворенного вещества. При приложении давления на водный раствор выше осмотического (равновесного) осуществляется перенос растворителя в обратном направлении (от раствора к чистому растворителю через мембрану) и обеспечивается достаточная селективность очистки (рис. 2.24). Необходимое давление, превышающее осмотическое, составляет при концентрации солей 2-5 г/л 0,1-1 МПа и при концентрации солей 20-30 г/л – 5-10 МПа.
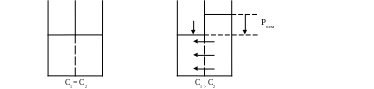
Рис. 2.24. Схема обратного осмоса
