
Занятие 20(10)
Рассеянный склероз
Рассеянный склероз - хроническое демиелинизирующее заболевание, развивающееся вследствие воздействия внешнего патологического фактора (наиболее вероятно, инфекционного) на генетически предрасположенный организм, при этом заболевании наблюдается многоочаговое поражение белого вещества ЦНС, в редких случаях с вовлечением и ПНС. На фоне хронического воспалительного процесса, в основе которого лежат аутоиммунные механизмы, наблюдается повреждение миелиновых оболочек нервных волокон (демиелинизация). Одновременно развиваются очаговые и диффузные нейродегенеративные изменения. В большинстве случаев рассеянный склероз имеет неуклонно прогрессирующее, чаще волнообразное течение, которое в последующем, по мере нарастания нейродегенеративных изменений, может сменяться постепенным прогрессированием, при этом заболевании пациенты молодого и среднего возраста сначала утрачивают работоспособность, а в более поздних стадиях - способность к передвижению и самообслуживанию.
Эпидемиология. Рассеянный склероз начинается практически в 60% случаев в возрасте от 20 до 40 лет, средний возраст клинического начала колеблется в разных популяциях от 29 до 33 лет.
Распространенность (болезненность) и заболеваемость рассеянным склерозом выше в географических зонах, максимально удаленных от экватора. В последние годы эта зависимость выражена меньше и заболевание стало часто встречаться и во многих южных регионах. Существенное влияние на риск развития заболевания оказывают особенности питания, социально-экономические и экологические характеристики.
Основные эпидемиологические характеристики рассеянного склероза:
• болеют преимущественно лица европейской расы, есть этнические группы (майори, эскимосы и народности Крайнего Севера), где рассеянный склероз встречается очень редко;
• наличие семейного РС, т.е. нескольких случаев заболевания у кровных родственников
• во всех популяциях среди больных РС преобладают женщины, но у мужчин выше вероятность развития неблагоприятного первично прогрессирующего течения РС;
• изменение частоты РС среди перемещенного населения выявило изменение риска РС при смене зон проживания (миграции) в зависимости от возраста переезда (до и после 15 лет);
• существуют «кластеры РС» - зоны резко повышенной частоты РС и «микроэпидемии РС» - резкое увеличение заболеваемости РС на ограниченной территории в определенный временной промежуток;
• в ряде регионов отмечено, что в соседних странах, даже в пределах одной страны, показатели распространенности и заболеваемости РС могут значительно варьировать, что определяется суммой наследственных, внешних и социальных факторов.
Этиология. В настоящее время рассеянный склероз определяют как мультифакториальное заболевание. Под этим понимается участие как внешних, так и наследственных факторов.
• вирусы (ретровирусы, группы herpes VI, JC и др., вероятно, в сочетании с эндогенными ретровирусами), бактериальная инфекция (стрептококк, стафилококк и др.);
• хронические интоксикации (органические растворители, бензин, металлы, другие химикаты); большое значение имеет пребывание в экологически неблагоприятных условиях проживания, особенно в детском возрасте;
• особенности питания (в частности, преобладание животных жиров и белков), особенно в возрасте до 15 лет;
• хронический психоэмоциональный стресс.
Патогенез. Большое значение в патогенезе рассеянного склероза имеет состояние иммунной системы. Локально активируется небольшая группа клеток, которые вырабатывают хемокины и цитокины, вызывают повышение адгезии и проницаемости гематоэнцефалического барьера, что приводит к проникновению в ткань мозга большого количества клеток крови и развитию воспалительной реакции. Активированные лимфоциты могут проникать через гематоэнцефалический барьер, что является важной составной частью пускового механизма аутоиммунных реакций в ЦНС. В последующем происходит срыв толерантности к антигенам миелина, и в патологический процесс включаются различные клеточные и в меньшей степени гуморальные аутоиммунные реакции.
Не исключена возможность прямого цитопатического влияния вирусов, цитокинов, продуктов распада миелина и других токсичных веществ на олигодендроциты (миелинсинтезирующие клетки). Большое значение в патогенезе рассеянного склероза имеют особенности обмена в ткани мозга, изменения реологических свойств крови, нарушения обмена микроэлементов, жирных кислот, аминокислот и другие факторы. Нервные волокна подвергаются необратимым дегенеративным изменениям. Цитокины, продукты перекисного окисления и другие вещества могут повреждать нервные волокна уже в ранних стадиях заболевания.
Длительный аутоиммунный процесс приводит к истощению иммунной системы с развитием вторичного иммунодефицита и снижению гормональной активности коры надпочечников.
Клинические проявления. В типичных случаях первые клинические симптомы рассеянного склероза появляются у лиц молодого возраста (от 18 до 45 лет), хотя в последнее время все чаще описывают дебют заболевания как у детей, так и у лиц старше 50 лет. Первыми симптомами заболевания часто бывают ретробульбарные невриты, проявляющиеся снижением остроты зрения, скотомы, ощущением нечеткости изображения, пелены перед глазами, преходящей слепотой на один или оба глаза (при двустороннем процессе). Заболевание может начинаться с глазодвигательных расстройств (диплопия, косоглазие, межъядерная офтальмоплегия, вертикальный нистагм), неврита лицевого нерва, головокружения, пирамидных симптомов (центральный моно-, гемиили парапарез с высокими сухожильными и периостальными рефлексами, клонусами стоп, патологическими пирамидными рефлексами, исчезновением брюшных кожных рефлексов), мозжечковых нарушений (пошатывание при ходьбе, статическая и динамическая атаксия, интенционное дрожание, горизонтальный нистагм), расстройств поверхностной (гип-, диз- и парестезии) или глубокой чувствительности (сенситивная атаксия, сенситивный парез, гипотония). Наиболее ранними симптомами поражения проводящих путей могут быть повышенная истощаемость и исчезновение брюшных рефлексов, снижение вибрационной чувствительности, асимметрия сухожильных рефлексов. Значительно реже первыми признаками болезни становятся невротические расстройства, нарушения функций тазовых органов (задержка мочеиспускания, императивные позывы).
В аналитических ретроспективных исследованиях установлено, что дебют рассеянного склероза с ретробульбарного неврита и чувствительных расстройств и длительная первая ремиссия указывают на более благоприятное течение заболевания, а появление признаков поражения пирамидного тракта или путей мозжечка и короткая первая ремиссия прогностически неблагоприятны.
Прогрессирование рассеянного склероза сопровождается поражением других отделов ЦНС и возникновением новых симптомов. Уже в начальных стадиях отмечается повышенная утомляемость (синдром «хронической усталости»). В более поздних стадиях наблюдаются эмоциональная неустойчивость, эйфория или депрессия, раздражительность, вялость, апатия, нарушения памяти и снижение интеллекта различной степени вплоть до деменции. Когнитивные нарушения выявляются уже в ранних стадиях заболевания и нарастают по мере прогрессирования патологического процесса. Эпилептические припадки встречаются редко, у некоторых больных могут быть пароксизмальные изменения тонуса, невралгические боли и другие пароксизмальные нарушения чувствительности. Наиболее ярким проявлением сенсорных пароксизмов при рассеянном склерозе служат простреливающие боли по типу синдрома Лермитта, который заключается в приступах интенсивной боли, ощущении покалывания, напряжении, «прохождении тока» по ходу позвоночника, чаще при разгибании шеи. Предполагаемая причина - очаг демиелинизации в шейном отделе спинного мозга с выраженным отеком и раздражением проходящих через него чувствительных волокон.
В большинстве случаев у больных имеются симптомы поражения и головного, и спинного мозга (цереброспинальная форма). В некоторых случаях в клинической картине преобладают симптомы поражения спинного мозга (спинальная форма) или мозжечка (мозжечковая или гиперкинетическая форма). В последнем случае интенционное дрожание может быть настолько выраженным, что достигает степени гиперкинеза и делает невозможным любое целенаправленное движение. Возникают дисметрия, адиадохокинез, скандированная речь, выраженная атаксия. У некоторых больных рассеянным склерозом, чаще у длительно болеющих, выявляются симптомы поражения ПНС, как правило, по типу полинейропатии.
Ряд симптомокомплексов отражает особенности клинического проявления демиелинизирующего поражения при рассеянном склерозе. Наиболее распространены синдромы «клинической диссоциации или расщепления», «непостоянства клинических симптомов» и «горячей ванны». Синдром «клинического расщепления» заключается в несоответствии между симптомами поражения различных структур, что отражает сочетание у одного больного признаков поражения разных проводящих путей или разных уровней поражения. Синдром «горячей ванны»: при повышении температуры окружающей среды состояние больных ухудшается (нарастают парез, атаксия). Усугубление симптомов, как правило, преходящее, что является более специфичным для рассеянного склероза признаком, чем само ухудшение состояния. Этот синдром неспецифичен и отражает повышенную восприимчивость нервного волокна, лишенного миелиновой оболочки («изоляции»), к внешним воздействиям.
В целом клинические проявления рассеянного склероза можно разделить на 7 основных групп:
• поражение пирамидной системы с геми-, пара- и тетрапарезами с соответствующим повышением сухожильных рефлексов и патологическими пирамидными симптомами;
• поражение мозжечка и его связей с развитием статической и динамической атаксии, мышечной гипотонии;
• нарушения чувствительности по проводниковому типу, сначала глубокой, с развитием сенситивной атаксии и сенситивных парезов, а затем болевой и температурной;
• поражение ствола мозга с нарушениями черепной иннервации, чаще всего с развитием глазодвигательных симптомов, поражением лицевого нерва (периферический парез мышц лица);
• невриты зрительного нерва (в том числе ретробульбарные невриты) со снижением остроты зрения и появлением скотом;
• нарушения функции тазовых органов, чаще по типу императивных позывов, задержек мочеиспускания, в последующем - недержания мочи, иногда сочетание задержек и эпизодов недержания мочи;
• нейропсихологические изменения: снижение памяти, скорости сенсомоторных реакций, способности концентрировать внимание, эйфория или депрессия, синдром хронической усталости.
Диагностика и дифференциальная диагностика. Основой диагностики является специфическая клиническая картина заболевания, подтвержденная данными параклинических методов обследования. Данные МРТ и результаты исследования вызванных потенциалов головного мозга (чаще зрительных, реже соматосенсорных и слуховых), позволяющие выявить субклинические очаги поражения. В крови часто обнаруживаются неспецифическая лейкопения, нейтропения, а в стадии обострения - лимфоцитоз. Наблюдаются увеличение агрегации тромбоцитов, тенденция к повышению содержания фибриногена и одновременно - активация фибринолиза. При обострении и прогрессирующем течении заболевания выявлено нарушение функции коры надпочечников, проявляющееся резким снижением экскреции с мочой С21-кортикостероидов (особенно глюкокортикоидной фракции), а также снижением уровня кортизола в плазме крови. Во время ремиссии содержание стероидных гормонов в моче и кортизола в плазме часто возвращается к норме. Определенное диагностическое значение имеет выявление повышенного содержания IgG в цереброспинальной жидкости вследствие стимуляции гуморального иммунитета, что указывает на определенные нарушения иммунорегуляции в мозге. При изоэлектрическом фокусировании эти IgG формируют олигоклональные группы, поэтому они получили название «олигоклональные иммуноглобулины». Косвенное значение имеют изменения показателей иммунных реакций периферической крови, свидетельствующие о дисбалансе в иммунной системе: уменьшение содержания Т-клеток, особенно супрессорного фенотипа, снижение функциональной активности специфических и неспецифических супрессоров, относительное увеличение содержания В-клеток и признаки их поликлональной активации in vivo, повышенные уровни продукции активационных цитокинов и антител к
Таблица 12.1. Диагностические критерии рассеянного склероза (МакДональд, 2001)
Лечение. В
связи с тем, что этиология заболевания
неясна, этиотропного лечения рассеянного
склероза в настоящее время нет. Принципы
лечения больных основываются на
индивидуальном подходе с учетом
особенностей течения и активности
иммунопатологического процесса,
выраженности отдельных неврологических
симптомов. Препарат назначают строго
индивидуально на основе и под контролем
иммунного статуса и с учетом всех
показаний и противопоказаний. В последние
годы появилась группа новых препаратов,
способных при длительном использовании
уменьшать частоту обострении и замедлять
прогрессирование заболевания, т.е.
оказывающих профилактическое действие.
Большое значение имеют адекватно
подобранное симптоматическое лечение,
медико-социальная реабилитация больных.
Симптоматическая терапия направлена
на поддержание и коррекцию функций
поврежденной системы, компенсацию
нарушений, повышение качества жизни
больных. Определенное значение имеет
группа метаболических препаратов,
способствующих регенерации поврежденной
ткани и усилению собственных механизмов
контроля за патологическим процессом.
Все большее внимание сейчас уделяется
методам немедикаментозного лечения и
реабилитации больных, предупреждению
осложнений.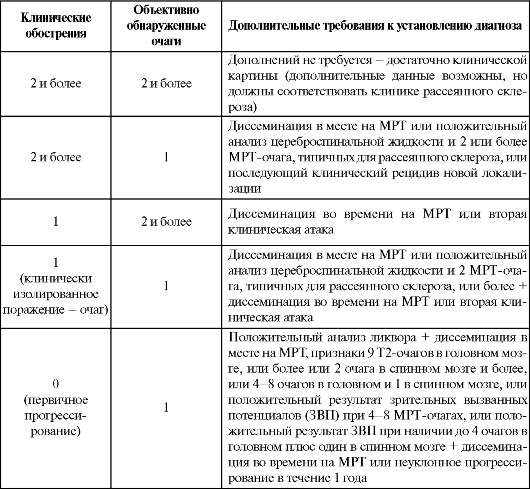
Патогенетическая терапия состоит из лечения обострений и периодов резкого нарастания активности заболевания и предупреждения обострений и прогрессирования инвалидности. При обострении заболевания препаратами выбора остаются кортикостероиды и в меньшей степени препараты адренокортикотропного гормона (АКТГ), оказывающие противовоспалительное и иммуносупрессивное действие. Наибольшее распространение в настоящее время получили короткие курсы растворимых кортикостероидов в больших дозах, которые вводят внутривенно во время острой стадии активации патологического процесса.
При злокачественном течении заболевания возможно комбинированное использование кортикостероидов с плазмаферезом или с цитостатиками, но последнее используется редко, так как повышается риск суммирования побочных эффектов.
Ангиопротекторы и антиагреганты, препаратов, снижающих проницаемость гематоэнцефалического барьера, антиоксидантов. Метаболические препараты (актовегин, церебролизин, карнитина хлорид, кортексин, глицин и другие), аминокислоты (глутаминовая, метионин), витамины группы В, Е, производные альфа-липоевой кислоты (тиоктацид, эспалипон, берлитион) способствуют более ранней компенсации нарушенных неврологических функций.
Можно не только вводить иммуноактивные препараты, но и выводить патологические агенты из крови с помощью плазмафереза.
Основным методом предупреждения обострений и увеличения длительности ремиссии сейчас является длительное использование иммуномодуляторов и иммуносупрессоров, снижающих активность воспалительного и аутоиммунного процесса (ПИТРС)
Симптоматическая терапия проводится в тесной связи с медико-социальной реабилитацией больных и во многих случаях оказывает большое влияние на состояние больного рассеянным склерозом и на течение заболевания. Важным аспектом симптоматической терапии является снижение патологического мышечного тонуса. Для этого назначают миорелаксанты (тизанидин, баклофен, толперизон), препараты бензодиазепинового ряда (дантролен), иглорефлексотерапию, точечный массаж, применяют методы физической релаксации.
При умеренном повышении мышечного тонуса, особенно при спинальных формах рассеянного склероза, эффективны сеансы гипербарической оксигенации (ГБО). Нарушения функций тазовых органов, включая нарушения половой функции, можно также корректировать с помощью магнитостимуляции. При гиперрефлексии детрузора используют антихолинергические препараты, трициклические антидепрессанты. Большую проблему для больных с нижним парапарезом представляют частые императивные позывы и недержание мочи в дневное и ночное время. В этих случаях препаратом выбора является десмопрессин (аналог вазопрессина), в дозе 20 мкг эффективно снижающий продукцию мочи. Для лечения гиперактивного мочевого пузыря наиболее часто применяют антихолинергические препараты. Важным моментом в лечении расстройств функций тазовых органов является профилактика уроинфекций. В некоторых случаях для полного освобождения пузыря необходима периодическая катетеризация, так как любые нарушения пассажа мочи стимулируют развитие инфекционных заболеваний. Назначают уросептики: 5-НОК или производные нитрофурана (фуразолидон, фуразолин, фурадонин).
Для коррекции дисфункции вегетативной нервной системы применяют вегетотропные средства, при системном головокружении - бетагистин (бетасерк), циннаризин (стугерон), по показаниям - психотропные препараты. У тяжелобольных с гипотрофиями возможно проведение курсов лечения анаболическими стероидами, например ретаболилом.
Важное направление реабилитационного лечения - компенсация двигательных нарушений. Наряду с широким применением лекарственных препаратов, разрабатываются методы коррекции этих нарушений с помощью электро- и магнитостимуляции. Большое значение имеет подбор комплекса ЛФК.
Эпилепсия
Эпилепсия - хроническое заболевание, проявляющееся повторными судорожными или другими припадками, не провоцированными какими-либо немедленно определяемыми причинами и сопровождающееся изменениями личности. Эпилептический припадок - клиническое проявление аномального и избыточного разряда группы нейронов головного мозга.
Заболеваемость эпилепсией составляет 50-70 на 100 000 населения, распространенность - 5-10 на 1000 человек. Считается, что 1 припадок и более в течение жизни переносят около 5% населения. Наибольшая частота заболевания у детей и лиц пожилого возраста.
Этиология и патогенез. Примерно в 2/3 случаев эпилепсия идиопатическая, в остальных она обусловлена органическим поражением головного мозга. У новорожденных и младенцев наиболее частыми причинами припадков являются тяжелая гипоксия, генетические дефекты метаболизма, а также перинатальные поражения. В детском возрасте припадки во многих случаях обусловлены инфекционными заболеваниями нервной системы.
В молодом возрасте основной причиной эпилептических нарушений является черепно-мозговая травма, возможно развитие припадка как в остром, так и в более позднем периоде. Важной причиной является изменение гиппокампа - мезиальный височный склероз.
У больных старше 50 лет ведущими этиологическими факторами эпилепсии являются сосудистые и дегенеративные заболевания головного мозга.
Наследственная предрасположенность играет определенную роль при некоторых типах эпилепсии.
В патогенезе эпилепсии ведущее значение имеет изменение нейрональной активности головного мозга, которая вследствие воздействия патологических факторов становится чрезмерной и периодичной. Эпилептические приступы являются следствием патологических разрядов, связанных с изменением возбуждения нейронов, их клинические проявления зависят от места происхождения, длительности и распространенности разряда. Биохимической основой припадков являются избыточный выброс в синаптическую щель возбуждающих нейротрансмиттеров: аспартата и глутамата - и недостаток тормозных нейромедиаторов, прежде всего ГАМК.
В основе эпилептогенеза лежат нарушения баланса между активностью тормозных и возбуждающих нейротрансмиттеров, изменение чувствительности рецепторов к ним, нарушение функционирования ионных клеточных каналов.
Клинические проявления. В клинической картине эпилепсии выделяют период припадка, или приступа, и межприступный период. Следует подчеркнуть, что в межприступном периоде неврологическая симптоматика может отсутствовать или определяться обусловливающим эпилепсию заболеванием (черепно-мозговая травма, инсульт и т.д.).
Характер эпилептических припадков может быть различным. Выделяют парциальные (фокальные, локальные) и генерализованные припадки. Соответственно эпилепсия может быть фокальной и генерализованной.
Парциальные припадки подразделяются на простые, сложные (с нарушением сознания) и вторично-генерализованные. Симптоматика при парциальных припадках определяется синдромом раздражения какой-либо зоны коры мозга. Среди простых парциальных припадков выделяют припадки:
• с моторными признаками;
• с соматосенсорными или специфическими сенсорными симптомами (звуки, вспышки света или молнии);
• с вегетативными симптомами или признаками (своеобразные ощущения в эпигастрии, бледность, потливость, покраснение кожи, пилоэрекция, мидриаз);
• с психическими симптомами.
При сложных припадках в той или иной степени нарушено сознание. Сознание может быть не полностью утрачено, больной частично понимает происходящее вокруг. Часто сложные парциальные припадки обусловлены патологическим очагом в височной или лобной доле, им предшествует аура. В зависимости от локализации очага раздражения аура может быть сенсорной, вегетативной, моторной, речевой, психической.
К сенсорной ауре относят разнообразные нарушения восприятия. Зрительная аура, возникающая при поражении затылочной доли, обычно проявляется видением ярких искр, блестящих шаров, лент, ярко-красным окрашиванием окружающих предметов (простые зрительные галлюцинации) или в виде образов каких-то лиц, отдельных частей тела, фигур (сложные зрительные галлюцинации). Меняются размеры предметов (макроили микропсия). Иногда выпадают поля зрения (гемианопсия), возможна полная потеря зрения (амавроз). Возможно своеобразное ощущение «уже виденного». При обонятельной ауре (височная эпилепсия) больных преследует «дурной» запах, часто в сочетании со вкусовыми галлюцинациями (вкус крови, горечь, металлический привкус и др.). Слуховая аура представляет собой различные звуки: шум, треск, шелест,музыку, крики. Для психической ауры (при поражении теменно-височной области) типичны переживания страха, ужаса или блаженства, радости. Вегетативная аура проявляется изменениями функционального состояния внутренних органов: сердцебиением, болями за грудиной, усиленной перистальтикой кишечника, позывами на мочеиспускание и дефекацию, болями в эпигастрии, тошнотой, слюнотечением, ощущением удушья, ознобом, побледнением или покраснением лица и др. Моторная аура (при поражении сенсомоторной области) выражается в различных двигательных автоматизмах: запрокидывании или повороте головы и глаз в сторону, автоматизированных движениях конечностей, которые распространяются закономерно (нога - туловище - рука - лицо), при этом появляются сосательные и жевательные движения. Речевая аура сопровождается произнесением отдельных слов, фраз, бессмысленными восклицаниями и др.
После ауры, которая длится несколько секунд, больной теряет сознание и падает. Падение сопровождается своеобразным громким криком, обусловленным спазмом голосовой щели и судорожным сокращением мышц грудной клетки. Сразу же появляются судороги, сначала тонические: туловище и конечности вытягиваются в состоянии напряжения, голова запрокидывается и иногда поворачивается в сторону, дыхание задерживается, вены на шее набухают, лицо становится бледным, постепенно нарастает цианоз, челюсти судорожно сжаты. Тоническая фаза припадка продолжается 15-20 с. Затем появляются клонические судороги в виде толчкообразных сокращений мышц конечностей, шеи, туловища. Во время клонической фазы припадка (до 2-3 мин) дыхание нередко бывает хриплым, шумным из-за скопления слюны и западения языка, цианоз медленно исчезает, изо рта выделяется пена, часто окрашенная кровью вследствие прикусывания языка или щеки. Частота клонических судорог постепенно уменьшается, и по их окончании наступает общее мышечное расслабление. В этот период больной не реагирует даже на самые сильные раздражители, зрачки расширены, реакция на свет отсутствует, сухожильные и защитные рефлексы не вызываются, нередко происходит непроизвольное мочеиспускание. Сознание остается сопорозным и лишь через несколько минут постепенно проясняется. Выходя из сопорозного состояния, больной нередко погружается в глубокий сон. По окончании припадка больные жалуются на разбитость, вялость, сонливость, но о самом припадке ничего не помнят.
Иногда припадки происходят так часто, что развивается эпилептический статус - угрожающее жизни состояние, при котором больной не приходит в сознание между припадками или припадок продолжается более 30 мин. Наиболее частым и тяжелым является тонико-клонический эпилептический статус. Вследствие нарастающих расстройств дыхания и сердечной деятельности, отека головного мозга эпилептический статус создает реальную угрозу для жизни больного. Летальность при этом состоянии достигает 20%.
Диагностика и дифференциальная диагностика. Принципиально важно установить эпилептическое происхождение приступов и исключить иные его причины (коллапс, психогенные приступы и пр.). Необходимо выяснить, имеется ли у больного идиопатическая эпилепсия или припадки обусловлены поражением мозга, требующим лечения (опухоль мозга, абсцесс). Правильная диагностика типа и происхождения припадков является основой адекватной тактики лечения.
Одним из основных методов диагностики эпилепсии остается электроэнцефалография. Эпилептическая активность проявляется острыми волнами, пиками (спайки), комплексами «пик-медленная волна», «острая волна-медленная волна».
При обследовании больных эпилепсией необходимо проведение КТ, желательно МРТ с целью исключения курабельных заболеваний мозга, способных вызвать эпилептический синдром. МРТ необходима для выбора хирургической тактики лечения больного эпилепсией.
Целесообразно исследовать глазное дно, провести биохимическое исследование крови, выполнить ЭКГ и ЭхоКГ, особенно у лиц пожилого возраста.
Лечение. Целью лечения являются прекращение эпилептических припадков при минимальных побочных эффектах, повышение качества жизни пациентов, ведение больного таким образом, чтобы его жизнь была максимально полноценна и продуктивна.
Современная тактика лечения больных эпилепсией включает:
• выявление тех причин припадков, которые поддаются лечению (опухоль, аневризма и т.д.);
• исключение факторов, провоцирующих припадки (недосыпание, физическое и умственное перенапряжение, гипертермия, злоупотребление алкоголем);
• правильную диагностику типа эпилептических припадков и эпилепсии;
• назначение адекватной лекарственной терапии (стационарной или амбулаторной);
• внимание к образованию, трудоустройству, отдыху, социальным проблемам больного эпилепсией.
Принципы лечения эпилепсии:
• соответствие препарата типу припадков и эпилепсии (каждый препарат имеет определенную селективность в отношении типа припадков и эпилепсии);
• по возможности использование монотерапии (применение одного противоэпилептического препарата).
Лечение начинается тогда, когда отмечено не менее двух неспровоцированных приступов. Только в отдельных случаях (при высокой вероятности рецидива припадков) терапия начинается уже после первого приступа.
Начинать лечение следует с монотерапии небольшой дозой противоэпилептического препарата, рекомендуемого при данном типе припадка и форме эпилепсии. Дозу увеличивают при отсутствии побочных эффектов и сохранении припадков. При парциальных припадках Препаратами первой очереди являются карбамазепин и вальпроаты. При отсутствии эффекта применяются новые противоэпилептические препараты - топирамат (топамакс по 200-600 мг/сут), ламотриджин (ламиктал по 100-200 мг/сут), леветирацетам (кеппра по 1000-3000 мг/сут).
При генерализованных тонико-клонических припадках, абсансах, миоклонических припадках эффективны вальпроаты и ламотриджин
Лечение эпилептического статуса проводят в условиях реанимационного отделения. Для купирования припадков применяют сибазон (диазепам, седуксен): 2 мл раствора, содержащего 10 мг препарата (внутривенно медленно на 20 мл 40% раствора глюкозы). Повторное введение допустимо не ранее чем через 10-15 мин. Если нет эффекта от сибазона, применяют фенитоин, гексенал или тиопентал-натрий: 1 г препарата разводят изотоническим раствором хлорида натрия и в виде 1-5% раствора вводят внутривенно очень медленно. При этом имеется опасность угнетения дыхания и гемодинамики, поэтому следует делать минутные паузы после вливания каждых 5-10 мл раствора. В случаях продолжения припадков и при их высокой частоте следует использовать ингаляционный наркоз закисью азота в смеси с кислородом (2:1). Одновременно назначают противоотечные препараты для борьбы с отеком мозга (маннитол, глицерол), проводится коррекция кислотно-основного равновесия, микроциркуляции.
