
- •Дефильность молекул и их ориентация на межфазной поверхности. Стандартная работа адсорбции. Растворимые пав. Уравнение Шишковского. Правило Дюкло-Траубе. Связь уравнения Гиббса с уравнением Ленгмюра.
- •Билет 2 Белые золи. Определение дисперсности белого золя по оптической плотности.
- •Билет 3 Физическая и химическая адсорбция. Природа адсорбционных сил. Полярные и неполярные адсорбенты.
- •Дэс по теории Штерна. Сравнительная хар-ка термодинамич и электрокинетич потенциалов.
- •Стабилизир и моющее действие мыл и пав. Гидрофобизация и гидрофолизация поверхности.
- •Конденсационно-кристаллизационные структуры. Структурообразование разбавленных дисперсных систем – гели, студни. Синерезис.
- •Билет 5 Классиф-ция дисп-ых систем по агрегатному состоянию дисперсн фазы и дис-ой среды
- •Билет 6 Термодинамическая неравномерность и агрегатная неустойчивость дисперсных систем. Основные факторы стабилизации.
- •Адсорбция на границе жидкость – газ. Вывод адсорбционной формулы Гиббса. Применение этой формулы для случая, когда адсорбирующееся веществл растворимо в жидкости. Поверхностная активность.
- •Электрокинетический потенциал. Влияние различных факторов на электрокин потенц: индифферентных и неиндифферентных электролитов, разбавления, конц-ия, pH среды и др.
- •Ионообменная адсорбция и ее особенности. Уравнение Никольского. Ионообменная адсорбция в природе и технике.
- •Высокопористые адсорбенты корпускулярной, пористой и губчатой структуры и методы их получения. Пористость. Интегральная и дифференциальная структурные кривые адсорбции.
- •Билет 9 Поверхностное натяжение и электрический потенциал. Механизмы образования дэс. Связь межфазного электрического потенциала с поверхностным натяжением – уравнение Липмана.
- •Газообразные и конденсированные слои на границе: раствор-газ (кривая сжатия пленки нерастворимых пав). Поверхностное давление. Весы Ленгмюра. Определение размеров молекул пав с помощью весов Ленгмюра.
- •Коагуляция коллоидных систем электролитами. Порог коагуляции. Правило Шульца-Гарди. Критическое значение электрокинетического потенциала.
- •Билет 10 Кинетическая и агрегативная устойчивость колл систем. Молекулярные и ионные стабилизаторы. Механизм их действия. Приведите примы стабилизации колл систем.
- •Билет 12 Основы теории устойчивости и коагуляции длфо. Потенциальные кривые взаимодействия частиц. Расклинивающее давление. Электростатическая и молекулярная составляющие
- •Адсорбция на границе жидкость-газ. Поверхностное натяжение растворов. Пав и пиав. Мера поверхностной и адсорбционной активности. Правило Дюкло-Траубе.
- •Дисперсность. Коллоидные системы как “предельно-дисперсные системы”, их роль в создании новых материалов, применяемых в технике.
- •Билет 13 Эффективная вязкость структурированных жидкостей и пластических тел. Зависимость ее от действующего напряжения сдвига.
- •Адсорбция электролитов. Основные закономерности. Влияние радиуса и гидратации ионов на адсорбцию. Лиотропные ряды ионов.
- •Поведение дисперсных систем в постоянном электрическом поле. Электрокинетические явления. Работы Рейса.
- •Билет 15 Теория кинетики быстрой коагуляции Смолуховского. Вывод уравнения для расчетов частиц в золе. Время половинной коагуляции.
- •Адсорбция на границе раздела фаз твердое тело-жидкость. Молекулярная адсорбция из растворов: влияние природы адсорбента, растворенного вещества и растворителя на адсорбцию.
- •Получение коллоидных частиц методом конденсации. Механизм процесса конденсации. Примеры физ и хим конденсации.
- •Билет 18 Основные реологические величины при исследовании упруго-кинетических свойств структурированных частиц.
- •Особенности адсорбции паров на пористых адсорбентах. Капилярная конденсация. Уравнение Томпсона.
- •Пептизация, как метод получения золей. Способы пептизации. Правило осадка.
- •Билет 19 Определение констант уравнения Ленгмюра: их физ смысл. Константа адсорбционно-десорбционного равновесия и её связь с температурой и теплотой адсорбции.
- •Назовите виды устойчивости дисперсных систем в соотвествии с классификацией Пескова. В чем заключается различие между лиофильными и лиофобоными колл системами?
- •Оптические методы исследования коллоидных систем. Ультрамикроскопия. Нефелометрия.
- •Билет 21 Что такое хроматография? Рассмотрите физико-химические принципы хроматографического разделения.
- •Билет 22 Нерастворимые пав. Тип пленок. Анализ кривой сжатия пленки нерастворимых пав.
- •Модели Ньютона и Бингама, ньютоновские и бингамовские жидкости. Физический смысл Ps и Pd.
- •Вязкое течение жидкостей. Уравнение Ньютона и Пуазейля. Причины неподчинения коллоидных растворов этим законам.
- •Классификация дисперсных структурированных систем по Ребиндеру. Дисперсные системы с конденсационно-кристаллической структурой.
- •Билет 28 Термодинамика поверхностных явлений. Общая характеристика поверхностных явлений. Поверхностная энергия в общем уравнении 1-го и 2-го законов термодинамики.
- •Устойчивость дисперсных систем. Потенциальные кривые взаимодействия частиц дисперсной фазы. Потенциальный барьер и его зависимость от толщины диффузного слоя.
- •Что представляют собой явления тиксотропии и реопексии? Чем обусловлены эти явления и для каких структурированных систем они характерны? Приведите примеры таких структурированных дисперсных систем
- •Билет 29 Ультрамикроскопия. Определение концентрации золей и размеров частиц. Поточный ультрамикроскоп.
- •Жидкообразные и твердообразные условно-пластичные структурированные системы: их отличие от ньютоновских жидкостей. Уравнение Ньютона и Пуазейля и их анализ.
- •Капиллярная конденсация паров в пористых адсорбентах. Сорбционно-десорбционный гистерезис. Возможные механизмы этого явления.
Билет 22 Нерастворимые пав. Тип пленок. Анализ кривой сжатия пленки нерастворимых пав.
При малых концентрациях ПАВ в поверхностном слое тепловое движение нарушает пространственную ориентацию молекул и молекулы в основном расположены в поверхностном слое горизонтально, при этом полярные группы остаются в воде, а углеводородные цепи лежат на ее поверхности (псевдогазовые пленки).
![]()
Рис. 3.21. Псевдогазовые пленки
При повышении концентрации ПАВ усиливается взаимодействие углеводородных цепей между собой, их углеводородные радикалы отрываются от поверхности воды, образуя крупные конденсированные кластеры «острова», в которых тепловое движение сильно затруднено (псевдожидкие пленки).

Рис. 3.22. Псевдожидкие пленки
При насыщении адсорбционного слоя (Г∞) образуется «молекулярный частокол Ленгмюра» из вертикально расположенных молекул. В этом состоянии площадь, занимаемая молекулой, определяется лишь площадью полярной группы, постоянной для всех членной гомологического ряда.

Рис. 3.23. Молекулярный частокол
 Зависимость поверхностного давления
от площади поверхности
Зависимость поверхностного давления
от площади поверхности
Участок (а) – отвечает начальным условиям – газообразная пленка
участок (в) – область сосуществования двумерного пара и жидкости
Участок (с) отвечает состоянию жидкой пленки жидкорастянутая;
С дальнейшим ростом 𝑝𝑠 мы обнаруживаем еще один фазовый переход – участок (d);
Далее идет участок (е), характеризующийся почти полной несжимаемостью пленка– конденсированная.
Участок (f) соответствует разрушению пленки. Здесь у мономолекулярной пленки в случае жидкости возникают капли, а в случае твердой пленки образуются многослойные образования.
При резком увеличении поверхн давления при сжатии пленки образуется сплошной мономолекулярный слой, в котором молекулы плотно прижаты друг к другу.
Модели Ньютона и Бингама, ньютоновские и бингамовские жидкости. Физический смысл Ps и Pd.
Идеал. вязк. тело Ньютона – поршень с отверстиями, помещ. в цилиндр с жид-ю.
![]()
 n- вязкость y
– скорость течения жидкости.
n- вязкость y
– скорость течения жидкости.


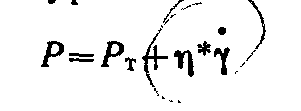 Рт – напряжен необход для разрушен
структуры
Рт – напряжен необход для разрушен
структуры
 При
малых напряжениях P<Pт
развивается только упругая деформация
При
малых напряжениях P<Pт
развивается только упругая деформация
При Р>Рт развивается пластическая деформация которая увеличивается до бесконечно (текучесть)
Бингамовские жидкости - в состоянии покоя существует более или менее жесткая пространственная структура, которая разрушается только при достижении определенного предельного напряжения сдвига.
Жидкости у которых коэффициент вязкости зависит только от природы жидкости и температуры. называются ньютоновскими и силы внутреннего трения, возникающие в них, подчиняются закону Ньютона
Причины возникновения ДЭС.
1. Неравенство электрохимических потенциалов ионов в кристаллической решетке твердого тела и ионов в растворе
2. Специфическая адсорбции ионов на поверхности твердой фазы (накопление на поверхности твердой фазы ионов под действием адсорбционных сил)
3. Ориентированная адсорбция поверхностно-активных веществ (дифильные молекулы ПАВ будут ориентироваться на поверхности определенным образом и образовывать адсорбционный двойной электрический слой.)
Билет 23 Двойной ионный слой мицеллы. Его образование путем избирательной адсорбции ионов при диссоциации молекул поверхностного слоя. Строение ДЭС на границе раздела фаз.
При погружении твердой фазы в раствор электролита происходят следующие явления: между твердой фазой и раствором возникает двойной электрический слой, появляется вполне определенная разность потенциалов между поверхностью дисперсной фазы и дисперсионной средой.
Избирательная адсорбция ионов – процесс фиксации на твердой поверхности ионов одного знака заряда при сохранении подвижности ионов противоположного знака. Поглощаться поверхностью будет тот ион, химический потенциал которого в растворе выше, чем в твердой фазе, поэтому почти всегда один из ионов адсорбируется селективно (избирательно).
Правило избирательной адсорбции Пескова – Фаянса:
На твердой поверхности адсорбента в первую очередь адсорбируются ионы, которые:
-
входят в состав кристаллической решетки адсорбента;

-
способны достраивать кристаллическую решетку адсорбента;

Согласно теории Штерна, слой противоионов состоит из двух частей. Первый слой противоионов удерживаются у поверхности под действием как электростатических, так и адсорбционных сил, образуя плоский конденсатор толщиной δ, предусмотренный теорией Гельмгольца – Перрена.
Этот слой, в котором наблюдается линейное
падение потенциала
 называют адсорбционным (плотным,
гельмгольцевским) слоем.
называют адсорбционным (плотным,
гельмгольцевским) слоем.
Другая часть противоионов находится в диффузной части ДЭС (диффузный слой Гуи), толщина которого может быть значительной и зависит от состава системы. В диффузной части ДЭС потенциал уменьшается по экспоненте, согласно теории Гуи – Чепмена.

Адсорбция на границе твердое тело-газ. Теория мономолекулярного слоя Ленгмюра. Вывод уравнения Ленгмюра. Его анализ и определение констант уравнения.
Основные положения теории Лэнгмюра
1. Каждый активный центр может адсорбировать только одну молекулу адсорбата. В результате этого на поверхности адсорбента образуется мономолекулярный слой адсорбата.
2. Адсорбированные молекулы не взаимодействуют друг с другом. Поэтому время пребывания молекул на активных центрах не зависит от того, заняты молекулами соседние активные центры или нет.
3. Адсорбция носит динамический характер. Адсорбат удерживается на поверхности адсорбента некоторое время, а потом десорбируется.
уравнение мономолекулярной адсорбции Лэнгмюра:
 . (3.11)
. (3.11)
предельная адсорбция А∞
![]() ps
-давление насыщенного пара
ps
-давление насыщенного пара
Полученное уравнение (3.11) используют для адсорбции газов. Для адсорбции из растворов используют уравнение Лэнгмюра в следующем виде:
 ,
(3.12)
,
(3.12)
где С – концентрация адсорбата.

Классификация ПАВ. Примеры мицеллобразующих ПАВ (мылоподобных). Строение мицелл МПАВ.
-
1. Истинно растворимые в воде, не образующие мицеллярных структур. Это вещества, имеющие недостаточно гидрофильную (неионизированную) полярную группу (-ОН, -NH2, -СООН и др.) либо недостаточно развитый углеводородный радикал (например, низшие члены гомологических рядов солей жирных кислот, сульфокислот, сульфоэфиров). Такие ПАВ, будучи поверхностно-активными на границе раздела «вода— воздух», проявляют слабое смачивающее и пенообразующее действие, с чем связано их практическое применение.
-
2. Коллоидные (мицеллообразующие) ПАВ (МПАВ). Способность к мицеллообразованию в сочетании с высокой поверхностной активностью обусловливает обширный комплекс практически важных свойств таких ПАВ: солюбилизирующую способность, высокую эффективность их стабилизирующего, эмульгирующего, смачивающего, моющего действия. В связи с этим коллоидные ПАВ находят самое широкое применение в качестве моющих и очищающих средств, эффективных стабилизаторов разнообразных дисперсных систем, смачивателей, флотореа- гентов, эмульгаторов.

Анионные ПАВ – органические соединения, диссоциирующие на небольшой катион и крупный анион (например, олеат натрия – С17Н33СООNa).
Катионные ПАВ – органические вещества, диссоциирующие на анион (Cl–, SO42–) и поверхностно-активный катион (алифатические и ароматические амины, их соли и др.).
Амфолитные ПАВ – органические соединения, содержащие катионную и анионную группы
Неионогенные ПАВ – вещества, не диссоциирующие на ионы в полярном растворителе.
Под мицеллой ПАВ понимают агрегат дифильных молекул, лиофильные молекулы которых обращены к растворителю, а лиофобные соединяются друг с другом образуя ядро мицеллы.
Билет 24 Что называется адсорбцией и как количественно её характеризуют? Напишите фундаментальное уравнение Гиббса и дайте определение избыточной адсорбции.
Адсорбция – процесс самопроизвольного перераспределения компонентов системы между поверхностным слоем и объемной фазой.
Количественно величину адсорбции выражают двумя способами:
1. Абсолютная адсорбция (А) – количество вещества (моль) в поверхностном слое, приходящееся на единицу площади поверхности или единицу массы адсорбента (моль/м2, моль/г).
 ,
(3.1)
,
(3.1)
где CS – концентрация компонента в поверхностном слое, объемом Vs; s – площадь поверхности адсорбента; hs – толщина поверхностного слоя адсорбента.
2. Гиббсовская (избыточная) адсорбция – избыточное число моль адсорбата в поверхностном слое (на единицу площади поверхности) по сравнению с тем числом моль, который бы находился в адсорбционном объеме в отсутствии адсорбции.
 , (3.2)
, (3.2)
где СV – равновесная объемная концентрация адсорбата; s – площадь межфазной поверхности; Cs – концентрация компонента в поверхностном слое, объемом VS; hs – толщина поверхностного слоя адсорбента.
Лиофильные дисперсии мылоподобных ПАВ.
Лиофилъные коллоидные системы характеризуются равновесным распределением частиц дисперсной фазы по размерам.
Это системы термодинамически устойчивы.ПАВ этой группы обладают специфическим свойством образовывать агрегаты мицеллы и структурированные адсорбционные слои рис 52 методички. В области низких концентраций образуется низкомолекулярный р-р ПАВ.При увеличении концентрации образуются димеры, а выше ККМ (критическая концентрация мицеллообразования – при которой образ сферич мицелла) молекулы объединяются в сферические агегаты где УВ радикалы соединяются и прячутся вовнутрь. При образовании мицеллы совершается работа образования новой фазы.
Строение ДЭС по Гуи-Чепмену. Результат второй интеграции. Физический смысл æ - параметр Дебая.



æ = 1/λ — параметр Дебая (λ — толщина диффузного слоя, зависящая от концентрации ионов в дисперсионной среде
Билет 25 Адсорбция из растворов на поверхности твердого тела. Чем отличается адсорбция из растворов от адсорбции газов и паров? Какие уравнения используют для описания изотермы обменной молекулярной адсорбции из растворов?
При адсорбции газов и паров на твердых адсорбентах допускалось, что до адсорбции поверхность адсорбента свободна от молекул адсорбата и она постепенно заполняется адсорбатом с ростом давления в соответствии с изотермой адсорбции.
При адсорбции из жидких р-ров поверхность адсорбента всегда полностью занята молеклами растворителя и растворенного вещества, поэтому растворенное вещество может адсорбироваться только вытесняя из поверхностого слоя молекулы растворителя. Таким образом при рассмотрении адсорбции из р-ров необходимо учитывать наличие как минимум 2 адсорбирующихся компонентов.




х – молярная доля x(с палкой) -молярная доля компонента в поверхн слое
K – отношение коэф распределения 1-го и 2-го компонентов
Самопроизвольное диспергирование. Условие самопроизвольного диспергирования. (d1,2<dкр) d-критическое. Лиофильные коллоидные системы.
Диспергирование – тонкое измельчение тв тела или жидкости в рез-те которого образ дисперсн системы: порошки, суспензии, эмульсии.
В случае достаточно сильного понижения удельной своб поверхн энергии на границе фаз благодаря воздействию ПАВ или повышен энергии теплов движения диспергирование может происходить самопроизвольно. Такое диспергиров наблюдается вблизи критической температуры смешения 2ух жидкостей при получении смазочно охлаждающих жидкостей из эмульсолов при образовании водных дисперсий некоторых гидрофильных минералов.


а – средний размер частиц k – постоянная Больцмана y – безразмерный коэффиц

