- •1) По величине молекулярной массы.
- •7) По составу мономеров и полимеров:
- •Способ 3. Полимеризация в растворе
- •Способ 4. Эмульсионная полимеризация.
- •Способ 5. Полимеризация в твердой фазе.
- •Ионная полимеризация.
- •Анионная полимеризация.
- •Закономерности процессов дегидрирования
- •Теоретические основы процессов дегидрирования.
- •Катализ реакции дегидрирования.
- •Кинетика реакций дегидрирования
Анионная полимеризация.
Склонность к анионной полимеризации
наиболее ярко выражена у мономеров с
электроно-акцепторными заместителями,
которые благоприятствуют поляризации
двойной связи, усиливая ее электрофильность
и стабилизирую образующиеся анионы.
Например, акрилонитрил.
![]()
![]()
Катализаторами анионной полимеризации служат вещества являющиеся донорами электронов: основания, щелочные металлы и их гидриды, амиды, металлорганические соединения и т.п.
Механизм анионной полимеризации в присутствии металлорганических соединений может быть описан следующей схемой:
1) Инициирование
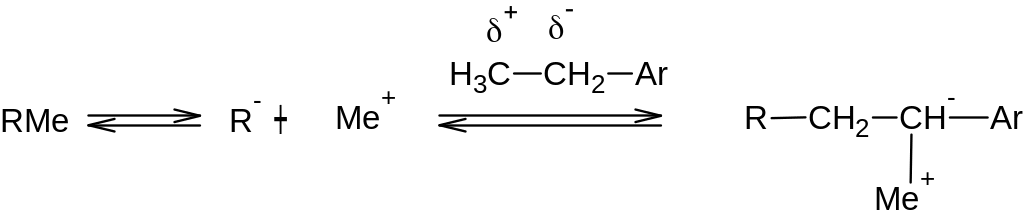
2) Рост цепи
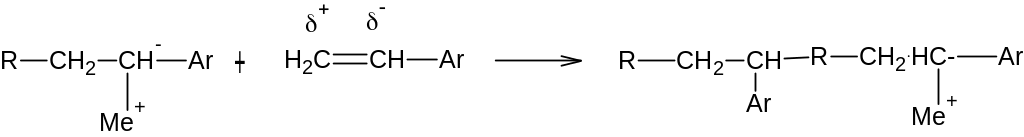

3) Прекращение роста цепи

Как и при катионной полимеризации наблюдаются следующие закономерности:
Наблюдается перемещение противоиона и заряда вдоль цепи и внедрение молекулы мономера между заряженными частицами.
Невозможен обрыв путем соединения растущих макроионов в результате наличия у них одинакового заряда.
Закономерности процессов дегидрирования
Под дегидрированием понимают химические процессы связанные с отщеплением водорода от органических соединений. Процессы дегидрирования углеводородов являются наиболее важным источником таких мономеров как бутадиен-1,3 (дивинил). Так в США его производят таким методом до 1,5 млн. тонн, а также изопрен, изобутилен, стирол, формальдегид и т.д.
Классификация реакций дегидрирования по виду связи между атомами от которых отщепляется водород приведен в мет. 681.
При С – С дегидрировании образуются соединения с двойной связью: алкены, алкодиены. Например, бутан.
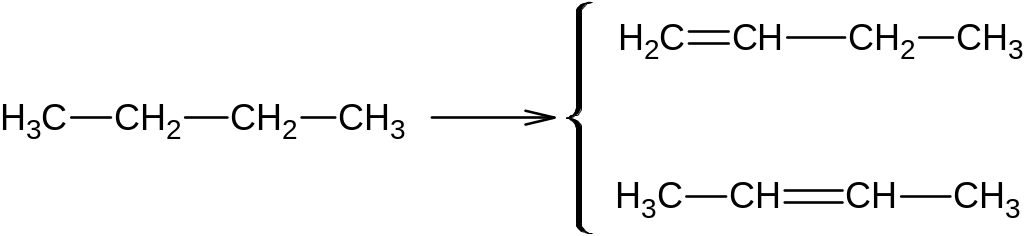
1) Процесс дегидрирования обратим, так при дегидрировании бутана образуется бутен-1, бутен-2, а при дальнейшем дегидрировании образуется бутадиен-1,3.
Дегидрированию могут подвергаться и боковые связи.
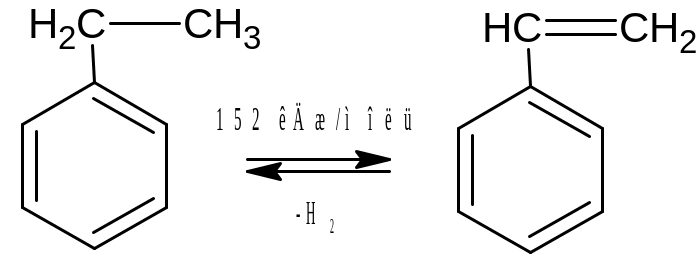
Процесс дегидрирования является обратимым.
2) При С=О дегидрировании образуются альдегиды и кетоны. Причем при дегидрировании первичных спиртов образуются альдегиды, при дегидрировании вторичных спиртов образуются кетоны.
3) По C-N дегидрировании образуются нитрилы, а кроме того следует отметить процессы дегидроциклизации и дегидроконценсации в том числе с аммиаком.
В случае дегидроциклизации из парафина или алканов получают ароматические соединения.
Например, процесс ароматизации нефти.
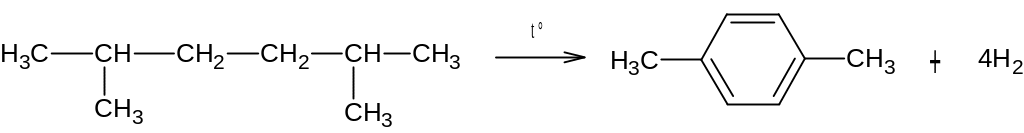
Процесс проводят в присутствии катализатора и при нагревании получают пара-ксилолы.
В случае дегидроконденсации получают конденсированные ароматические углеводороды. Например, нафталин.
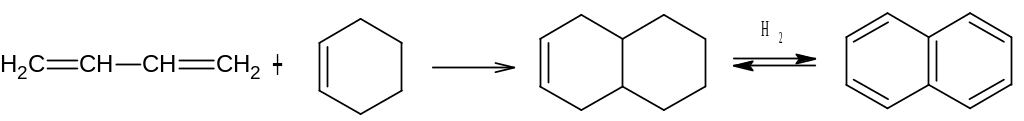
При дегидроконденсация с аммиаком образуютя новые CN связи.
![]()
Многие из этих превращений можно осуществить через окисление. Такого типа процессы называются окислительным дегидрированием. Они занимают промежуточное положение между окислением и дегидрированием. В этом случае процесс дегидрирования становится необратимым и экзотермичным.
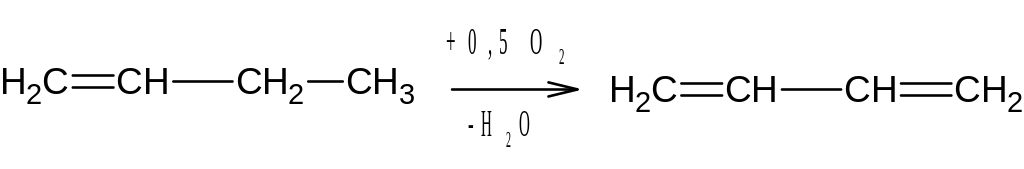
Теоретические основы процессов дегидрирования.
Термохимия процессов.
Процессы дегидрирования всегда протекают с поглощением тепла, т.е. это эндотермические процессы. Так при дегидрировании алканов до алкенов поглощается от 113 до 134 кДж/моль
![]()
При дегидрировании алканов до алкинов поглащается 311 кДж/моль.
![]()
При дегидрировании спиртов поглощаются от 67- до 83 кДж/моль
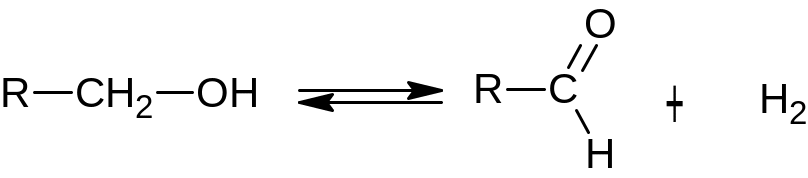
Этот момент оказывает существенное влияние на технологическое оформление процесса. В соответствии с принципом Ле-Шателье для осуществления эндотермических реакций дегидрирования благоприятна высокая температура.
Исследование температурной зависимости изобарно-изотермического потенциала для некоторых процессов дегидрирования показала, что протеканию реакций в прямом направлении благоприятствуют следующие факторы:
Повышение молекулярной массы алкана
Разветвление цепи
Наличие фенильных заместителей
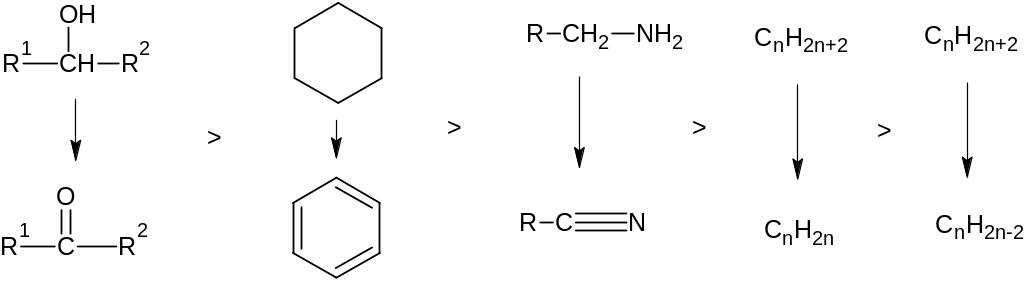
Наиболее легко происходит дегидрирование шестичленных циклоалканов, затем спиртов и аминов, особенно, вторичных спиртов и первичных аминов.
Отщепление водорода с получением сопряженных двойных связей или продуктов с тройной связью термодинамически наименее выгодно. Для получения достаточно высокой степени конверсии реагентов при дегидрировании необходимо выбрать условия при которых достигается возможно более выгодное положение равновесия, зависящая от термодинамических факторов. Процессы дегидрирования нужно проводить при сравнительно высокой температуре, которая для разных процессов колеблется от 200-650 °С. Процессы дегидрирования протекают в газовой фазе с увеличением объема газов, поэтому в соответствии с принципом Ле-Шателье повышение степени конверсии способствует низкое давление, так при дегидрировании этилбензола в стирол при t = 550 °С степень конверсии 40% при давлении 0,1 МПа и 80% при давлении 0,01 МПа.
Для снижения парциального давления реагентов в качестве технологического приема используют разбавление реакционной массы инертным газом или паром. В условиях реакции чаще всего применяют перегретый водяной пар, что позволяет сохранять общее давление 0,1 МПа. Таким образом если провести сравнение, то способность к дегидрированию с учетом только термодинамических факторов будет выглядеть следующим образом.