
- •1) По величине молекулярной массы.
- •7) По составу мономеров и полимеров:
- •Способ 3. Полимеризация в растворе
- •Способ 4. Эмульсионная полимеризация.
- •Способ 5. Полимеризация в твердой фазе.
- •Ионная полимеризация.
- •Анионная полимеризация.
- •Закономерности процессов дегидрирования
- •Теоретические основы процессов дегидрирования.
- •Катализ реакции дегидрирования.
- •Кинетика реакций дегидрирования
Катализ реакции дегидрирования.
Все реакции дегидрирования каталитические. Применение катализаторов позволяет достигнуть высокой скорости процесса при сравнительно низкой температуре, когда еще не получили развития нежелательные побочные реакции. Катализаторы способствуют достижения равновесия, т.к. ускоряют одинаково скорости как прямой так и обратной реакции.
Катализаторы делят на три группы:
Металлы 8-ой группы и их сплавы, а именно Fe, Co, Ni, Pd, Pt, а также Cu и Ag.
Оксиды металлов, оксиды MgO, ZnO, Cr2O3, Fe2O3.
Сложные оксидные катализаторы CuO·Cr2O3; ZnO·Cr2O3; хромиты, молибдаты Co·MoO2; вольфраматы Co·WO3; сульфиды
Металлические катализаторы наносят на пористые носители, добавляют различные промоутеры. Это оксиды других металлов, щелочи. Катализаторы применяют в виде тонкодиспергированных суспензий в жидкости, формованных в виде таблеток, цилиндров, колец и т.д.
Механизм процесса каталитического дегидрирования основан на взаимодействии молекулы углеводорода с активными центрами катализатора. Дегидрирование предпочтительно идет через акты образования и гибели адсорбированного на поверхности радикала.
Схематично это можно расписать следующим образом:
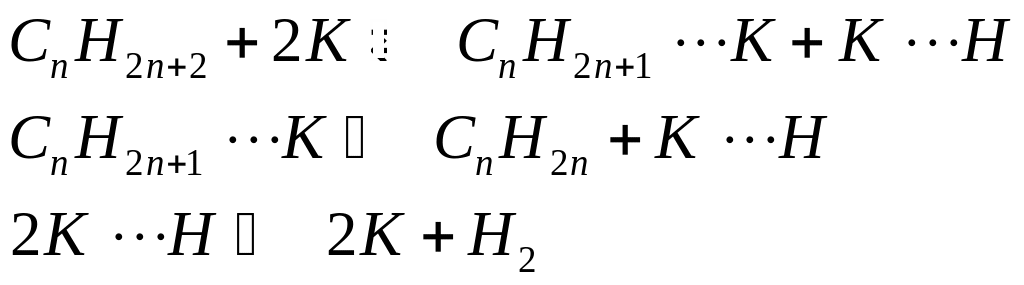
Причем в этом случае обратима каждая стадия.
На катализаторе существуют два различных типа активных центров. Первые ведут (или отвечают за) реакцию дегидрирования, а вторые крекинга. Это подтвержается резким снижением каталитической активности и скорости реакции крекинга при введении тиофена. Характерно, что сероуглерод блокирует лишь центры катализирующие крекинг, а скорость дегидрирования не изменяется. Олефины, ароматические соединения, ацетилен и его гомологи обладают более высокой способностью к сорбции.
К катализаторам предъявляются жесткие требования.
Высокая каталитическая активность по съему продукта с единицы объема или массы катализатора
Высокая селективность катализатора – это выход целевого продукта в расчете на израсходованное сырье.
Полная регенирируемость катализатора
Длительность работы катализатора 1-2 года
Низкая стоимость и доступность катализатора
Зерна катализатора должны обладать достаточной механической прочностью
Катализатор должен иметь повышенную теплопроводность
Химическая структура катализатора не должна меняться в условиях попеременного воздействия окислительной и восстановительной среды.
Отработанный катализатор должен не уничтожаться, а использоваться в качестве сырья для извлечения металлов, изготовления наполнителей, огнеупоров и т.д.
Кинетика реакций дегидрирования
Скорость реакции дегидрирования как и других гетерогенно-каталитических процессов в общем случае может зависеть от диффузионных и кинетических факторов. Роль диффузионных факторов уменьшается при:
Интенсивном перемешивании и турболизации потоков
При низких температурах,
Так при дегидрировании бутана в бутены
экспериментально получено следующее
уравнение. Это так называемое уравнение
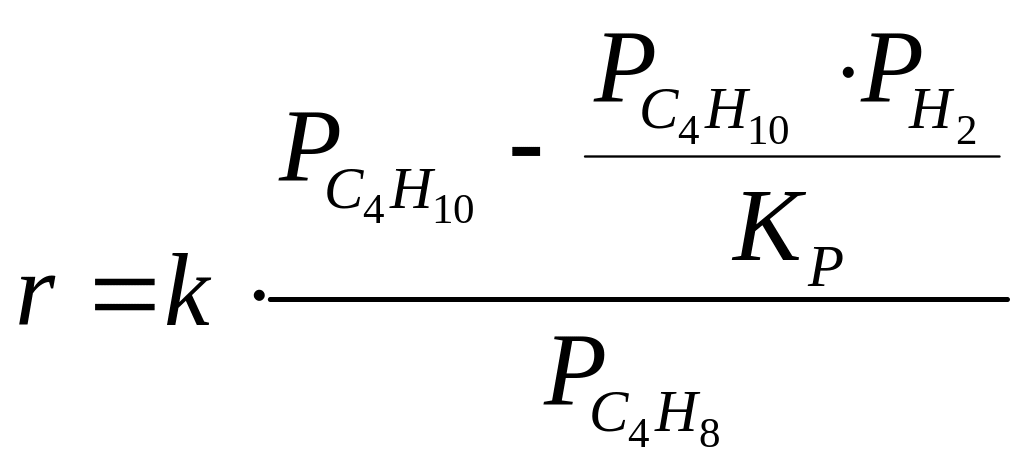 Ленгмюра-Хиншельвуда
для случая когда лимитирующий стадией
является химическая реакция на поверхности
катализатора. Р – это парциальные
давления реагентов. Из этого уравнения
видно, что накопление олефина уменьшает
скорость реакции, хемосорбция олефинов
выше, чем для насыщенных углеводородов
и водорода. Кажущаяся энергия активации
процессов дегидирования высока 170-190
кДж/моль
Ленгмюра-Хиншельвуда
для случая когда лимитирующий стадией
является химическая реакция на поверхности
катализатора. Р – это парциальные
давления реагентов. Из этого уравнения
видно, что накопление олефина уменьшает
скорость реакции, хемосорбция олефинов
выше, чем для насыщенных углеводородов
и водорода. Кажущаяся энергия активации
процессов дегидирования высока 170-190
кДж/моль
![]()
При дегидрировании этилбензола в стирол 152 кДж/моль
Это определяет сильную зависимость скорости дегидрирования от температуры, причем способность к дегидрированию на оксидных катализаторах уменьшается в следующем ряду: спирты амины н-акланы. С увеличением длины цепи скорость реакции дегидрирования увеличивается. Селективность зависит от развития при высоких температурах последовательных и параллельных реакций. Гидрогенолиз под действием образующегося водорода, реакции полимеризации, реакции дегидроконденсации ведущие к образованию смолистых веществ и кокса дезактивирующих катализатор.
Параллельные реакции – это крекинг, циклизация. При осуществлении процесса дегидрирования на одном и том же катализаторе селективность зависит от следующих факторов.
Относительной реационной способности органических веществ или функциональных групп
От способности адсорбироваться на поверхности катализатора.
Необходимо учитывать последний фактор при выборе катализатора, т.к. он способствует повышению селективности. Так металлические катализаторы не имеют специфической способности к адсорбции полярных соединений или функциональных групп на их поверхности. Легче адсорбируются одинарные С-С связи и двойные С=С. Нежелательные побочные реакции гидрогенолиза, дегироконденсации имеют более высокую энергию активации, чем дегидрирование. Например, энергия активации крекинга бутана составляет 250 кДж/моль, поэтому селективность можно повысить снижением температуры. Селективность зависит от времени контакта при более высокотемпературной дегидрировании. Время контакта составляет от долей секунды, до нескольких секунда, при этом степень конверсии равна 20-40%.
