
- •Лабораторная работа определение хлористого натрия в колбасных изделиях
- •Лабораторная работа
- •Рефрактометрические измерения. Правила работы с рефрактометром.
- •Лабораторная работа определение концентрации глюкозы в водных растворах.
- •Лабораторная работа определение массовой процентной доли ионов железа в железо-аммонийных квасцах методом фотоколориметрии
- •Лабораторная работа определение содержания соли (CuSo4, NiSo4, kCl, NaCl) в растворе с применением катионита
Лабораторная работа определение концентрации глюкозы в водных растворах.
Методика выполнения
Приготовление стандартного раствора глюкозы (раствор А). Навеску глюкозы (m=12,5г) взвешивают на технических весах, переносят в мерную колбу вместимостью 100 см3, доводят до метки дистиллированной водой и тщательно перемешивают. Концентрация раствора А 0,125 г/мл
Приготовление эталонных растворов. Серию эталонных растворов глюкозы готовят в мерных колбах вместимостью 50 см3, в соответствии с таблицей.
Таблица
Приготовление эталонных растворов глюкозы
-
№ п/п эталонного раствора
Объем стандартного раствора (раствор А), см3
Воды до общего объема раствора, см3
Содержание глюкозы, г/мл
5
50
0,0125
10
50
0,0250
15
50
0,0375
20
50
0,0500
25
50
0,0625
И
 змерение
показателя преломления эталонных
растворов.
Измеряют показатель преломления воды
n0,
затем показатели преломления
приготовленных растворов n.
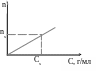
По полученным данным строят график в
координатах n
– C.
змерение
показателя преломления эталонных
растворов.
Измеряют показатель преломления воды
n0,
затем показатели преломления
приготовленных растворов n.
По полученным данным строят график в
координатах n
– C.
Определение содержания глюкозы в растворе. Измеряют показатель преломления раствора с неизвестной концентрацией глюкозы и по графику определяют содержание глюкозы.
Лабораторная работа определение массовой процентной доли ионов железа в железо-аммонийных квасцах методом фотоколориметрии
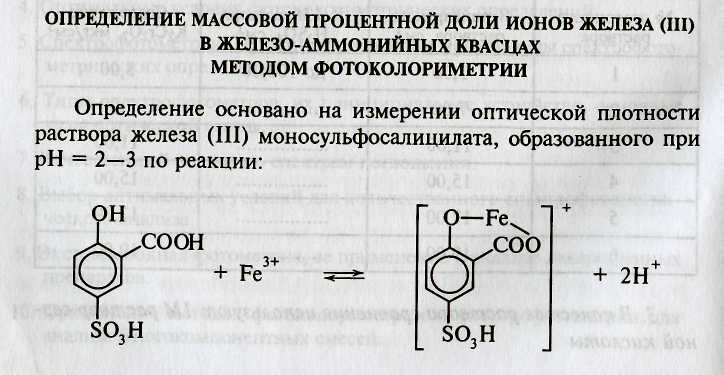
Определение основано на измерении оптической плотности раствора железа (III) моносульфосалицилата, образованного при рН=2-3 по реакции:
РЕАКТИВЫ:
Железо-аммонийные квасцы, х. ч.; стандартный раствор с концентрацией ионов Fe3+ 100 мкг/см3 (Навеску 0,8633 г (NH4)2Fe(S04)2·12H20 с помощью 25 мл 0.5М раствора H2S04 переносят в мерную колбу на 1 дм3 и доводят объем водой до метки); кислота сульфосалициловая 0,01 М раствор; кислота серная 0,5M раствор.
МЕТОДИКА ВЫПОЛНЕНИЯ РАБОТЫ
1. Приготовление эталонных растворов железа (III) моносульфосалицилата.
№ эталонного раст-вора |
Объемы растворов, см3 |
Воды до общего раствора, см3 |
Содержание ионов Fe3+ мг/50 см3 |
||
Стандартный раствор железо-аммонийных квасцов |
кислота серная 0,5M раствор
|
кислота сульфосалициловая 0,01 М раствор |
|||
1 |
1 |
2 |
10 |
50 |
0,1 |
2 |
2 |
2 |
10 |
50 |
0,2 |
3 |
3 |
2 |
10 |
50 |
0,3 |
4 |
4 |
2 |
10 |
50 |
0,4 |
5 |
5 |
2 |
10 |
50 |
0,5 |
6 |
- |
2 |
10 |
50 |
- |
Серию эталонных растворов готовят в мерных колбах в соответствии с таблицей. Раствор железо-аммонийных квасцов отбирают пипеткой, а растворы кислот цилиндром. Растворы доводят до метки по нижнему мениску и тщательно перемешивают.
2. Выбор светофильтра, позволяющего фотометрировать анализируемый раствор в оптимальном диапазоне длин волн, проводят следующим образом. В кювету с толщиной слоя 1 см наливают эталонный раствор средней концентрации (№3) и измеряют его оптическую плотность со всеми светофильтрами. В кювету сравнения наливают холостой раствор (№6). Результаты определений А записывают. Светофильтр, при котором оптическая плотность имеет максимальное значение, выбирают в качестве рабочего для последующих измерений А анализируемого раствора.
2. Измерение оптической плотности эталонных растворов. Для измерения оптической плотности растворов используют выбранный сфетофильтр и кювету на 1 см. Оптическую плотность каждого раствора измеряют 2-3 раза и вычисляют среднее арифметическое значений А для каждого раствора.
3. Построение градуировочного графика.
Полученные значения оптической плотности эталонных растворов используют для построения градуировочного графика. В координатах А=f (V стандартного раствора) или А=f (mFe).
4. Измерение оптической плотности контрольного раствора.
В колбу с контрольным раствором железо-аммонийных квасцов приливают цилиндром растворы кислот такие же объемы как и для серии стандартных растворов и доводят до метки водой.
5. Определение содержания Fe3+ в контрольной задаче.
По градуировочному графику определяют содержание Fe3+ в мг в контрольной задаче.
