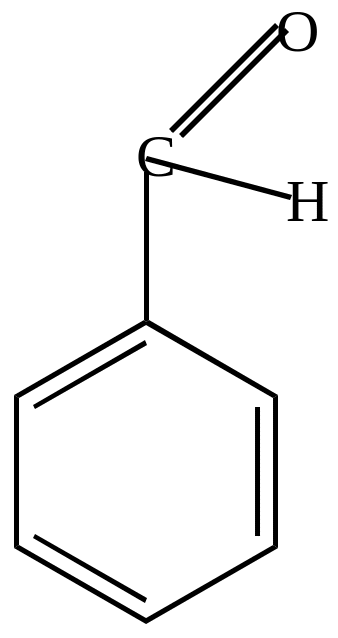
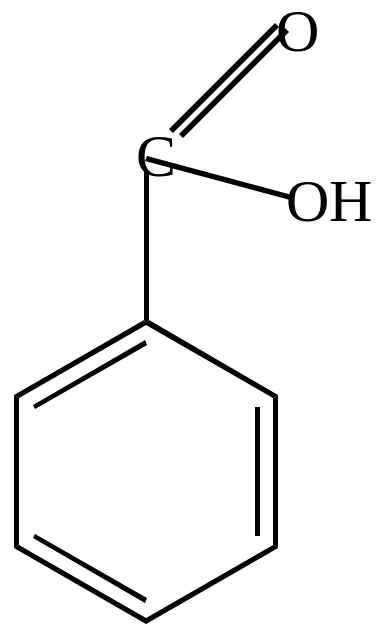
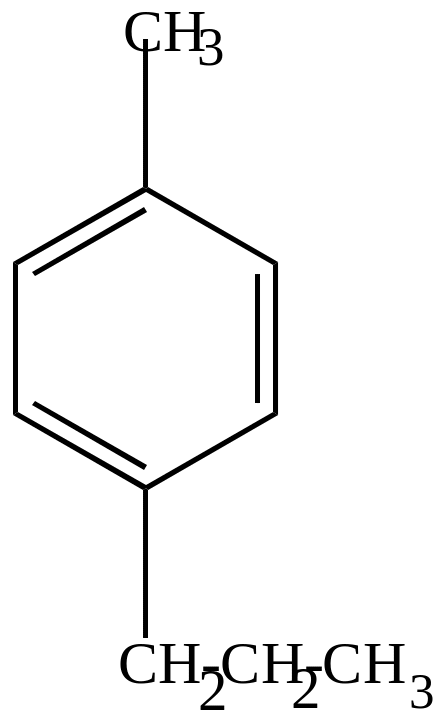
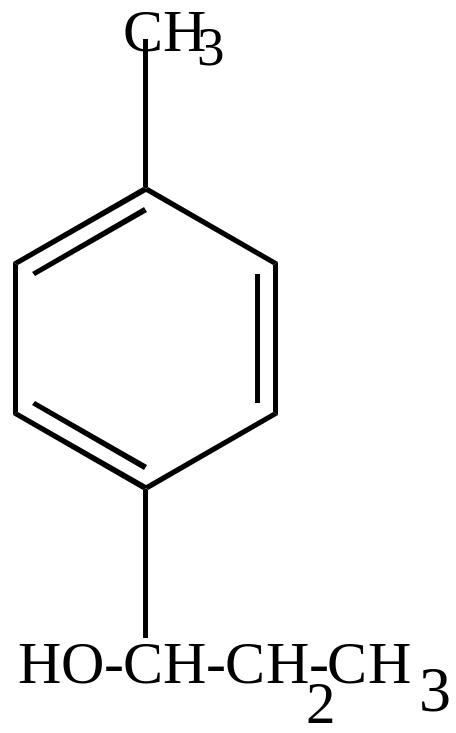
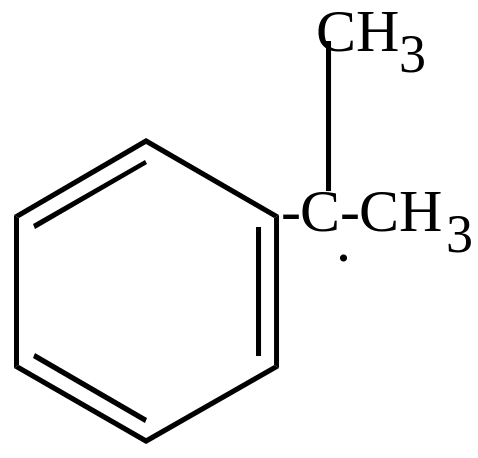
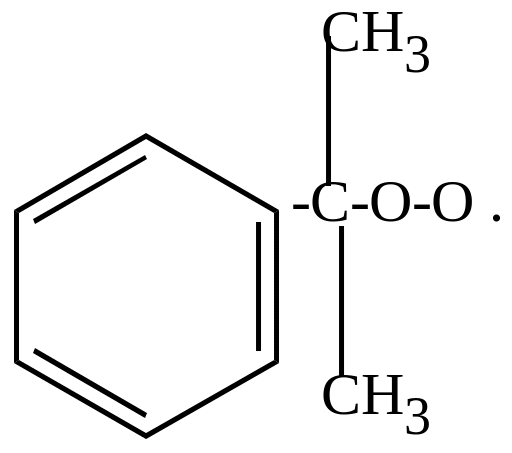
Радикал (2) намного устойчивее радикала
(1) вследствие сопряжения неспаренного
электрона с
![]() -секстетом
ядра.
-секстетом
ядра.
2.Нитрование.
Нитрование бензола гладко протекает при использовании в качестве нитрующего агента смеси концентрированной азотной и серной кислот.
Механизм реакции электрофильный.
HOSO2OH +HONO2
+
![]() H3O+
+ NO2+ +2
OSO2OH
-
H3O+
+ NO2+ +2
OSO2OH
-
HOSO2OH Нитроний-катион –
нитрующий агент
NO2+ + |
|
600C
|
|
+H+ |
H+ + OSO2OH- H2SO4
H3O+ + OSO2OH- H2O + H2SO4
При использовании избытка нитрующей смеси и повышении температуры можно ввести вторую и третью нитрогруппы.
|
1100C + HONO2 H2O + (H2SO4) |
|
HONO2 H2O + 3000C |
|
|
|
м-динитробензол |
|
|
Лекция 4 Нитрование гомологов бензола
Можно провести в двух направлениях.
а) Нитрование в ядре, если применить нитрующую смесь.
|
|
|
|
|
|
|
+ HONO2 (H2SO4) |
|
|
|
+ H2O |
|
|
|
|
|
|
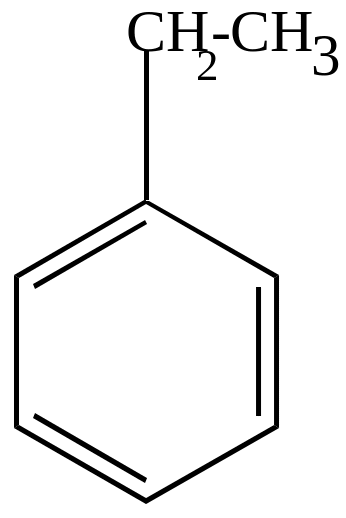
Механизм – электрофильный, идет в орто- или пара-положении к группе СН3, как к заместителю 1 рода.
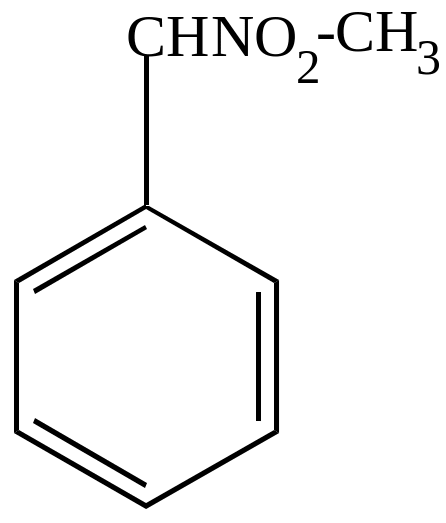
б) нитрование в боковой цепи, если нитровать разбавленной азотной кислотой в условиях реакции Коновалова – механизм свободно-радикальный.
|
+ HONO2 H2O + |
|
|
|
Метилфенилнитрометан |
3. Сульфирование.
Сульфирование бензола можно осуществлять действием олеума при комнатной температуре, или концентрированной серной кислотой при температуре 170-1800С.
При снижении концентрации серной кислоты до 65% реакция прекращается.
Реакция обратима, поэтому для достижения хорошего выхода необходимо удалять (связывать) воду, что достигается добавлением избытка серной кислоты, либо избытка углеводорода, который отгоняется вместе с водой.
Механизм – электрофильный.
2 HOSO2OH + HOS+O2OH H3O+ + 2 HOSO2O- + S+O3H
конц. гидросульфониевый
ион
|
+ S+O3H
|
|
+ H+
|
|
|
бензолсульфокислота |
|
H+ + -OSO2OH H2SO4
H3O+ + -OSO2OH H2SO4
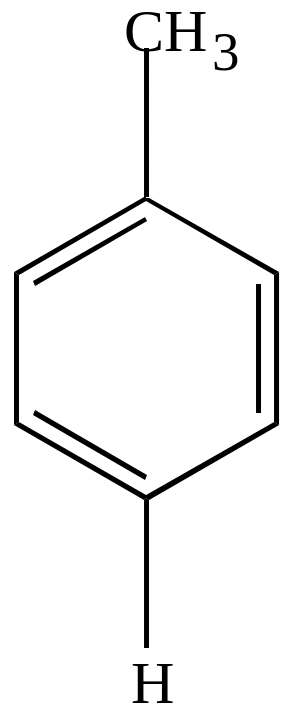
Сульфирование гомологов бензола идет гораздо легче, чем бензола, и, в основном, в пара-положение.
|
+ HOSO2OH -H2O |
|
|
|
П-толуолсульфокислота |
К реакции электрофильного замещения относятся также реакции Фриделя-Крафтса (т.е. алкилирование и ацилирование ароматического ядра в присутствии AlCl3).
Реакции присоединения (нетипичны)
У ароматических углеводородов протекают гораздо труднее, чем у ненасыщенных углеводородов, и только под действием реагентов высокой активности (H2, Cl2). При этом присоединение происходит одновременно у всех шести атомов углерода. Такие реагенты, как Br2, I2, HHal, H2SO4, HOCl, HOH к ароматическому кольцу не присоединяются.
присоединение водорода
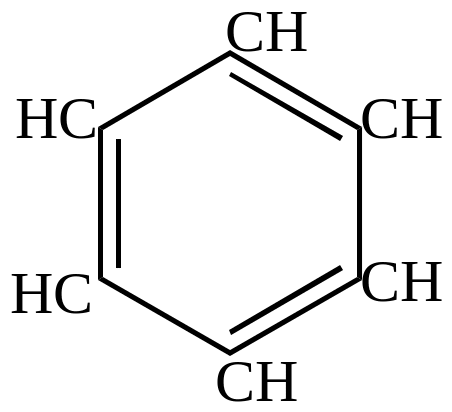
Pt, 1000C
+ 3H2
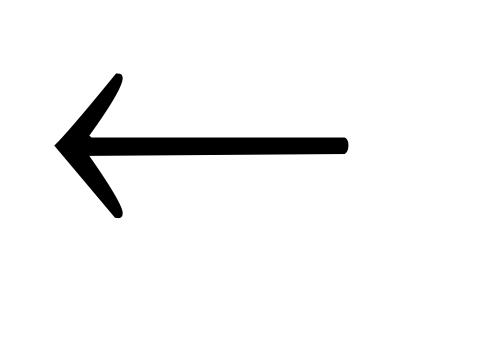
3000C
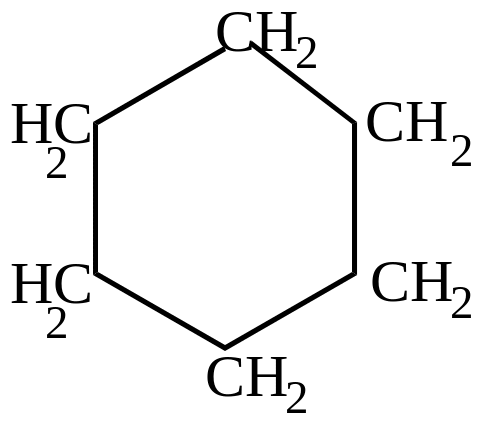
бензол
циклогексан
присоединение хлора
|
прямой солнечный свет +3Cl2 |
|
|
|
гексахлоран или гексахлорциклогексан |
Окисление
Бензольное ядро очень устойчиво к окислению. Оно не окисляется KMnO4, K2Cr2O7, азотной кислотой и другими сильными окислителями.
Гомологи бензола достаточно сильно окисляются, но эти реакции идут за счет окисления боковой цепи, бензольное кольцо при этом остается без изменения.
1) Окисление бензола.
Можно осуществить только в следующих случаях:
а) действие кислорода в присутствии катализатора при очень жестких условиях (происходит разрушение кольца).
|
V2O5 +4O2 4500C |
|
+ |
|
O
|
CO2 + H2O |
|
|
|
|
щавелевая кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
+ H2O |
|
|
|
|
Малеиновый ангидрид |
|
|
|
|
б) озонирование – окисление озоном с разрушением двойных связей кольца.
|
+3O3 |
|
+3H2O
-3H2O2 |
|
|
|
|
|
глиоксаль |
в) окисление перекисями с сохранением бензольного ядра.
|
Fe2+ + HO-OH -H2O |
|
|
|
фенол |
Механизм реакции – свободно-радикальный
2) Окисление гомологов бензола.
а) под действием сильных окислителей
(KMnO4, HNO3
и др.) или кислорода в присутствии
катализаторов происходит окисление
![]() -углеводородного
звена боковой цепочки с образованием
карбоксильной группы, связанной с ядром.
-углеводородного
звена боковой цепочки с образованием
карбоксильной группы, связанной с ядром.
|
+ O (KMnO4) |
|
+O
-H2O |
|
+O
|
|
|
|||||
Толуол |
|
бензиловый спирт |
|
бензальдегид |
|
бензойная кислота |
|
|||||
|
+O |
|
+O -H2O |
|
+3O
- CH3COOH |
|||||||
П-метилпропил-бензол |
|
этил-п-толуолкарбинол |
|
этил-п-толуилкетон |
|
|||||||
+3O
- CH3COOH |
|
|
+3O
-H2O |
|
|
|||||||
|
|
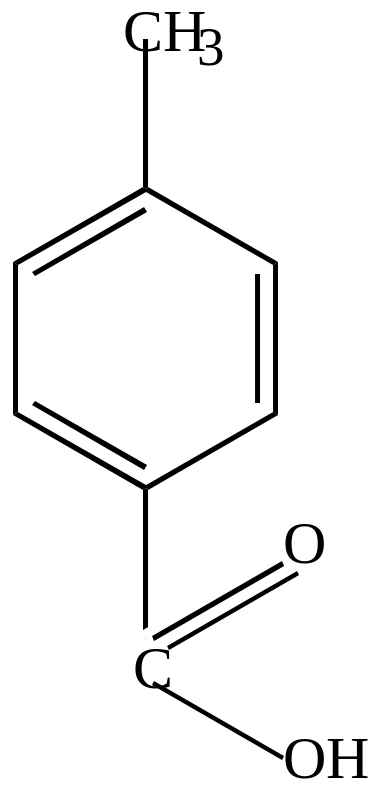
п-толуиловая кислота |
|
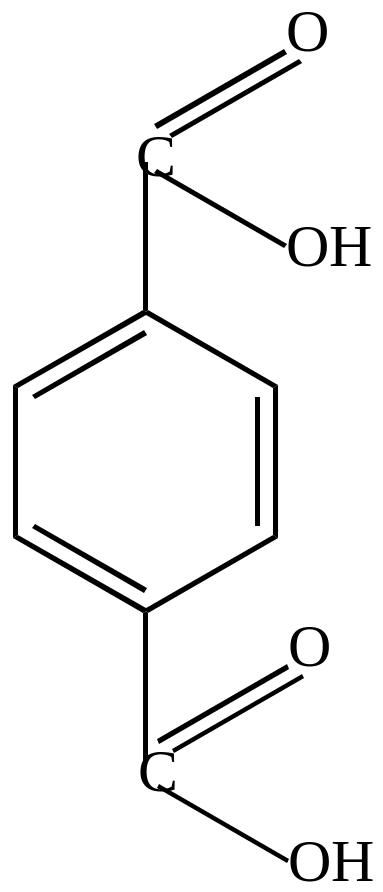
П-бензолдикарбоновая кислота (терефталевая кислота) |
|
|||||||
Промежуточные продукты окисления, как правило, не выделяются в свободном виде – окисление идет до кислот.
Реакция окисления часто используется для установления строения ароматических углеводородов (основность образующейся кислоты всегда соответствует числу боковых цепочек в исходном углеводороде).
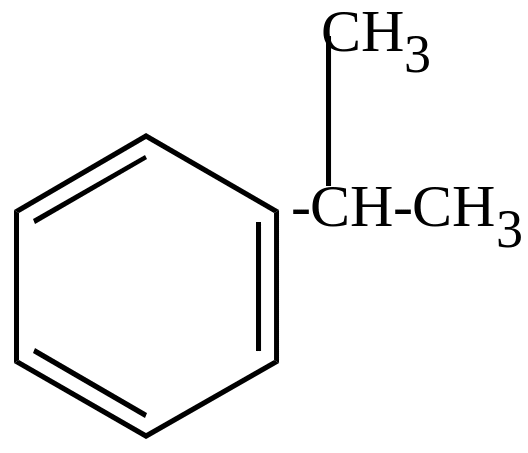
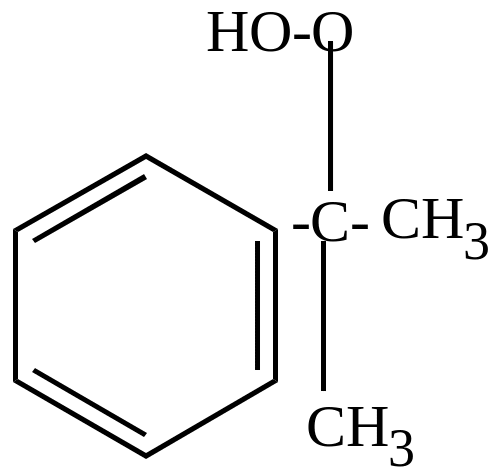
б) окисление молекулярным кислородом в присутствии перекисей идет по цепному механизму и приводит к образованию гидроперекисей, которые затем разлагаются на фенолы, кетоны, альдегиды (в зависимости от строения).
HO-OH HO . + . OH
|
+ . OH H2O + |
|
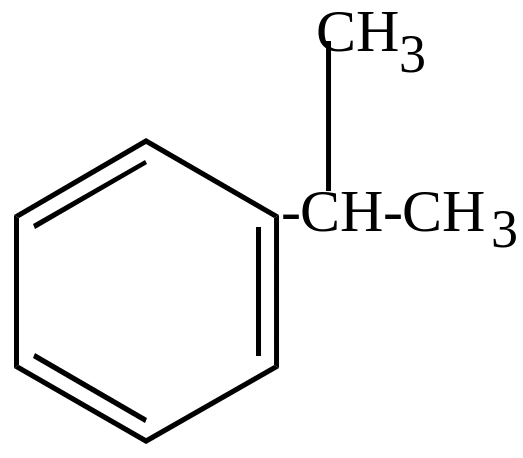
кумол |
(инициатор) |
|
|
+ O2 |
|
|
+ |
|
|
|
+ |
|
|||
|
|
|
+ |
|
|
||||
|
|
Фенол |
|
ацетон |
|
||||
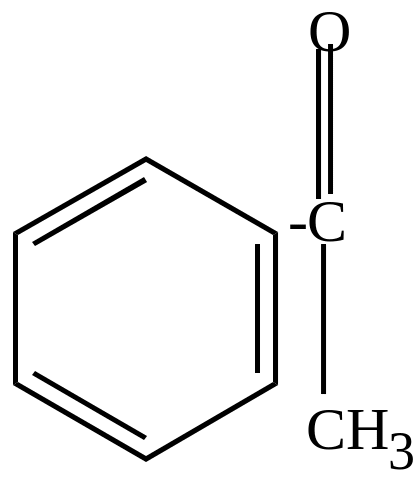
Возможно побочное направление -
![]() -распад
связи С-СН3
-распад
связи С-СН3
|
|
|
+ CH3OH |
|
|
метилфенилкетон |
|











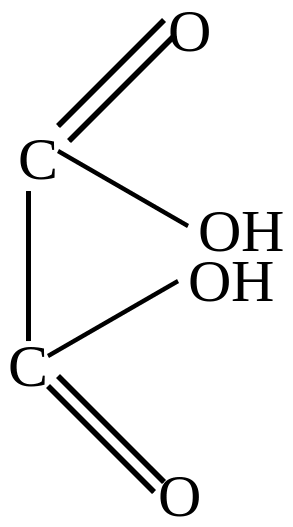
 малеиновая
кислота
малеиновая
кислота