
- •Аннотация
- •Содержание
- •Введение
- •Краткие теоретические сведения
- •1.1 Горение топлива
- •1.2 Химический состав генераторного газа.
- •2. Расчетная часть
- •2.1 Расчет расхода воздуха
- •2.2 Расчет объёма продуктов сгорания
- •2.3 Расчет изобарно-изотермического потенциала
- •2.4 Рассчитаем изобарно-изотермический потенциал при температуре 3270с(600к)
- •Заключение
- •Список используемой литературы
2.3 Расчет изобарно-изотермического потенциала
Исходные данные берем из справочника.
Диссоциация карбоната кальция проходит по реакции:
![]()
Таблица1.
|
A |
b |
c’ |
|
|
СаCO3 |
104,52 |
21920 |
-0,0002594 |
-1206830 |
91,71 |
СаO |
48.89 |
4520 |
-0,0000695 |
-635090 |
38,07 |
CO2 |
44.14 |
9040 |
-0,0000854 |
-393510 |
213.66 |
2.4 Рассчитаем изобарно-изотермический потенциал при температуре 3270с(600к)
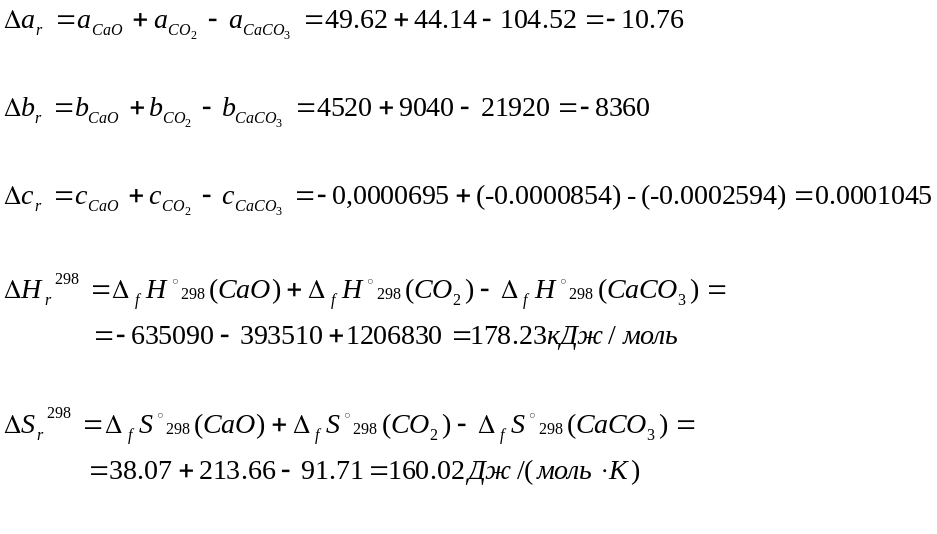
Энтальпия реакции:

Абсолютная энтропия реакции:
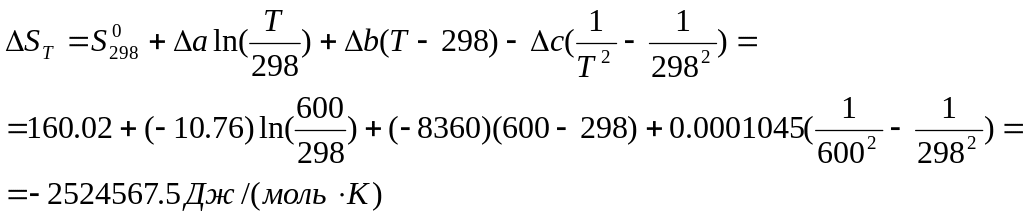
Изобарно-изотермический потенциал(энергия Гиббса):
![]()
Аналогично проводим расчеты для температур 4270 и 5270С(700К и 800К соответственно). Результаты представлены в Табл.2.
Таблица 2.
Т,К |
|
Δrb |
Δrc |
ΔH0r |
ΔS0298 |
ΔHTr |
ΔSTr |
ΔGTr |
600 |
-10,76 |
-8360 |
0,0001045 |
17823000 |
160,02 |
-2267201631000 |
-2524567,5 |
-2265686891000 |
700 |
-3354002707000 |
-3360569,17 |
-3353999346000 |
|||||
800 |
-4607998382000 |
-4196570,6 |
-4607994185000 |
Т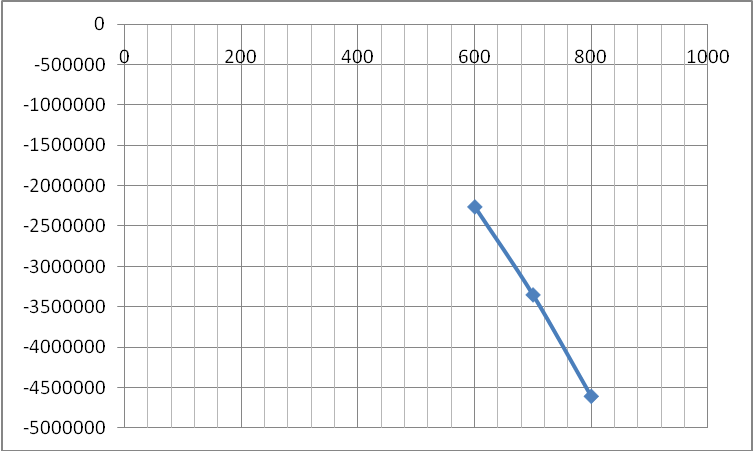 ,
К
ΔGTr,
*109,
Дж
,
К
ΔGTr,
*109,
Дж
Рис.1. Зависимость энергии Гиббса от температуры
Критерии направления протекания химических превращений.
На ход реакции оказывает влияние совокупность двух факторов: фактор изменения энтальпии и фактор изменения энтропии. Существует три возможных комбинации.
1.Реакции протекают в сторону уменьшения энтальпии и увеличения энтропии(ΔH<0, ΔS>0). В подобных случаях изменение изобарно-изотермического потенциала много меньше нуля. Для таких реакций характерно бурное и необратимое протекание.
2.Один из факторов благоприятен, другой нет: изменение энтальпии и энтропии больше нуля или, наоборот, изменение энтальпии и энтропии меньше нуля.
а) Изменение энергии Гиббса отрицательно. Реакция протекает, но, как правило, не полностью, до состояния равновесия.
б) Реакция протекает без изменения энергии Гиббса. В данном случае в системе равновесие.
в) Изменение энергии Гиббса положительно. Протекает обратная реакция.
3.Оба фактора неблагоприятны: изменение энтальпии больше нуля, а энтропии меньше. В данном случае изменение энергии Гиббса много больше нуля. Такой процесс запрещён законами термодинамики.
Расчеты для данных температур дают результаты, подходящие под случай 2.а).
Заключение
В данной работе определён расход воздуха и вычислен изобарно-изотермический потенциал (энергия Гиббса) при температурах 3270, 4270, 5270С. Показан расчет на 100 кг топлива, найден выход продуктов горения при нормальных условиях, показан расчет реакции диссоциации карбоната магния. Исходя из полученных результатов, видно, что чем больше температура, тем меньше энергия Гиббса.
