
Министерство образования и науки РФ
ФГАОУ ВПО УРФУ
Химико-технологический факультет
Кафедра химической технологии топлива и промышленной экологии
Реферат
по микробиологии и биотехнологии
«Превращение микроорганизмами соединений азота»
Студентка: Попова А.А.
Гр х-390702
Преподаватель: Безматерных М.А.
Екатеринбург
2012
Содержание
Введение
Превращение микроорганизмами соединений азота
Разложение нуклеиновых кислот
Разложение мочевины
Нитрификация
Денитрификация
Симбиотическая фиксация азота, химизм фиксации
Заключение
Список используемой литературы
Введение
Азот является одним из основных элементов питания, которые необходимы для жизни растений. Азот играет исключительно важную роль в обмене веществ. Он входит в состав таких важных органических веществ, как белки, нуклеиновые кислоты, нуклеопротеиды, хлорофилл, алкалоиды, фосфатиды и др. В среднем содержание его в белках составляет 16-18% от массы. Нуклеиновые кислоты играют важную роль в обмене веществ в растительных организмах. Они являются также носителями наследственных свойств живых организмов. Поэтому трудно переоценить роль азота в этих жизненно важных процессах у растений. Кроме того, азот является важнейшей составной частью хлорофилла, без которого не может протекать процесс фотосинтеза и, следовательно, не могут образовываться важнейшие для питания человека и животных органические вещества. Нельзя не отметить также большого значения азота как элемента, входящего в состав ферментов - катализаторов жизненных процессов в растительных организмах. Азот входит в органические соединения, в том числе в важнейшие из них - аминокислоты белков.
Превращение микроорганизмами соединений азота
Для роста растениям необходимы соединения азота. В природе азот может быть в формах, усвояемых растениями (таких как нитраты или соединения аммония) или неусвояемых ими (таких как молекулярный азот или оксид азота).
Азот находится в природе в основном в виде атмосферного азота. Растения синтезируют белки, используя нитраты из почвы, нитраты образуются из атмосферного азота и аммонийных солей, имеющихся в почве. Процесс превращения атмосферного азота в форму, усвояемую растениями и животными, называют связыванием азота.
Из аммиака и азотной кислоты получают разнообразные азотные и комплексные удобрения. Из твердых азотных удобрений наиболее концентрированным является мочевина CO(NH2)2.Также широко применяется нитрат аммония – аммонийная селитра.
Связывание азота может происходить двумя способами:
Во время разряда молний некоторое количество азота и кислорода в атмосфере соединяется с образованием оксидов азота. Они растворяются в воде и образуют разбавленную азотную кислоту, которая дает нитраты в почве.
Атмосферный азот превращается в аммиак, который затем под действием бактерий превращается в нитраты, этот процесс называется нитрификацией. Такие бактерии существуют в почве и в узелках корневой системы клубеньковых растений.
Кроме того, нитраты вносятся в почву в виде удобрений, их также усваивают растения через корневую систему.
После смерти растений и животных их белки разлагаются, образуя соединения аммония. Эти соединения превращаются бактериями в нитраты, которые остаются в почве, и азот, который возвращается в атмосферу.
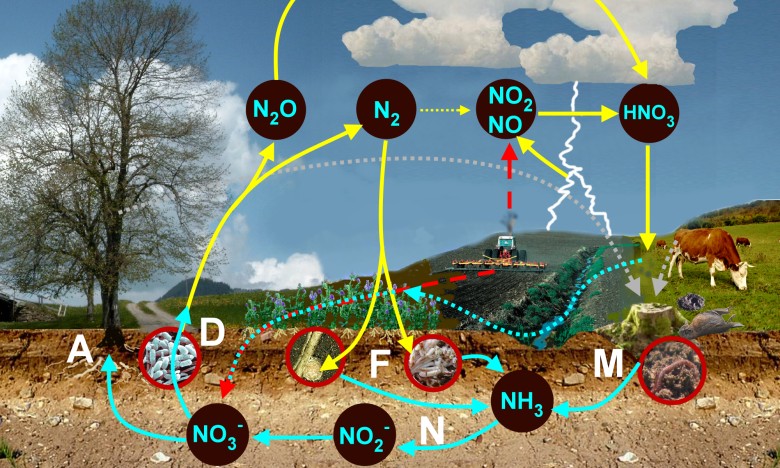
Круговорот азота: А – ассимиляция растениями, F – фиксация азота бактериями в симбиозе с растениями или бактериями, живущими в почве, N – нитрификация, D – денитрификация, М – минерализация.
Ассимиляция – переход неорганического азота (типа нитрата) в органическую форму азота как, например, аминокислоты. Нитрат переходит с помощью ферментов сначала в нитрит (редуктаза нитрата), затем в аммиак (редуктаза нитрита). Аммиак входит в состав аминокислот.
Минерализация (аммонификация) это процесс, в течение которого редуценты, такие как земляные черви, термиты, слизняки, улитки, бактерии и грибы преобразовывают органический азот отмерших растений в неорганические формы. Первый шаг это формирование аммиака и его солей (NH4+X-).
Ассимиляция и минерализация являются противоположными процессами.
Разложение нуклеиновых кислот
Нуклеи́новые кисло́ты (от лат. nucleus — ядро) — высокомолекулярные органические соединения, биополимеры (полинуклеотиды), образованные остатками нуклеотидов. Нуклеиновые кислоты ДНК и РНК присутствуют в клетках всех живых организмов и выполняют важнейшие функции по хранению, передаче и реализации наследственной информации
Полимерные молекулы нуклеиновых кислот расщепляются в тканях преимущественно гидролитическим путем при участии специфических ферментов, относящихся к нуклеазам.
Нуклеазы — большая группа ферментов, гидролизующих фосфодиэфирную связь между субъединицами нуклеиновых кислот. Различают несколько типов нуклеаз в зависимости от их специфичности: экзонуклеазы и эндонуклеазы, рибонуклеазы и дезоксирибонуклеазы, рестриктазы и некоторые другие. Рестриктазы занимают важное положение в прикладной молекулярной биологии.
Эндонуклеазы — белки группы нуклеаз, расщепляющие фосфодиэфирные связи в середине полинуклеотидной цепи. Эндонуклеазы рестрикции или рестриктазы расщепляют ДНК в определенных местах (так называемых сайтах рестрикции), они подразделяются на три типа (I, II и III) на основании механизма действия. Эти белки часто используют в генной инженерии для создания рекомбинантных ДНК, которые вводят затем в бактериальные, растительные или животные клетки.
Эндонуклеазы, разрывающие внутренние межнуклеотидные связи в молекулах ДНК и РНК, вызывающие деполимеризацию нуклеиновых кислот с образованием олигонуклеотидов.
Экзонуклеазы — белки из группы нуклеаз, отщепляющие концевые мононуклеотиды от полинуклеотидной цепи путем гидролиза фосфодиэфирных связей между нуклеотидами. В зависимости от способности гидролизовать связи на 3' и 5' концах полинуклеотидной цепи различают 3' и 5' экзонуклеазы. Экзонуклеазы встречаются в клетках как обособленно, так и в составе ферментативных комплексов. Например, ДНК-полимераза I содержит 5' экзонуклеазу, которая отщепляет РНК-праймер, прикрепленные непосредственно к тому месту, на котором происходит синтез ДНК. После этого ДНК-полимераза I начинает присоединять нуклеотиды на место отсоединенного праймера. У архебактерий и эукариот один из основных путей деградации РНКосуществляется белковым комплексом, состоящим, по большей части из 3' и 5' экзорибонуклеаз.
Помимо гидролитических нуклеаз, имеются ферменты, катализирующие распад нуклеиновых кислот, например, посредством трансферазной реакции. Они катализируют перенос остатка фосфорной кислоты от 5'-го углеродного атома рибозы одного мононуклеотида ко 2'-му углеродному атому соседнего мононуклеотида, сопровождающийся разрывом межнуклеотидной связи и образованием фосфодиэфирной связи между 2'-м и 3'-м углеродными атомами рибозы одного и того же мононуклеотида.
Дезоксирибонуклеазы I катализируют разрыв внутренних фосфодиэфирных связей в одной из двух цепей молекулы ДНК между 3'-м углеродным атомом дезоксирибозы и остатком фосфата с образованием низкомолекулярных олигодезоксирибонуклеотидов:
ДНК + (n–1) Н2O –> n-Олигодезоксирибонуклеотиды.
Дезоксирибонуклеазы II вызывают деполимеризацию молекулы ДНК в результате парных разрывов фосфодиэфирных связей обеих цепей ДНК с образованием более крупных олигодезоксирибонуклеотидов.
Помимо этих ферментов, открыты (преимущественно у микроорганизмов) еще экзодезоксирибонуклеазы, гидролизующие фосфодиэфирные связи молекулы ДНК с отщеплением концевых 5'-дезоксирибонуклеотидов. Например, из E. coli выделено четыре таких фермента, обозначаемых экзодезоксирибонуклеазами I, II, III и IV.
Рестриктазы – ферменты ДНКазного типа действия – катализируют распад чужеродной (в основном фаговой) ДНК в строго определенных участках молекулы, имеющих структуру палиндромов. Из E. coli выделены и охарактеризованы две такие рестриктазы, обозначаемые EcoRI и EcoRII соответственно. Рестриктазы оказывают строго специфическое действие, поэтому они используются для расшифровки последовательности нуклео-тидных остатков в ДНК фагов и вирусов. Кроме того, это уникальное свойство рестриктаз находит все большее практическое применение в генетической инженерии при «вырезании» определенных фрагментов ДНК и «встраивании» их в геном бактериальной ДНК (получение рекомбинантных ДНК). В результате клетке передается ряд не свойственных ей прежде наследственных признаков.
Из ферментов, осуществляющих распад ДНК и РНК не по гидролитическому пути, следует назвать полинуклеотид-фосфорилазу и группу ДНК-гликозидаз.
Механизм действия фермента сводится к переносу нуклеотидных остатков с РНК на неорганический фосфат, при этом образуется рибо-нуклеотиддифосфат (РДФ):
![]()
Открыта группа ДНК-гликозидаз, участвующих в реакциях отщепления модифицированных пуриновых и пиримидиновых оснований (например, урацила, образующегося при дезаминировании остатка цитозина в одной из цепей ДНК).
