
- •2.3. Получение фторорганических соединений
- •2.3.1. Общие методы получения фторорганических соединений
- •2.3.2. Синтез лекарственных средств
- •2.4. Диазотирование и диазореакции
- •2.4.1. Диазотирование ароматических аминов
- •2.4.2. Строение солей диазония, реакционная способность
- •2.4.3. Реакция азосочетания
- •2.4.4. Восстановление диазосоединений
- •2.4.5. Реакции диазосоединений с выделением азота
- •2.4.6. Техника безопасности, экология
- •2.5. Методы восстановления кратных связей
- •2.5.1. Методы восстановления, реагенты и катализаторы
- •2.5.2. Восстановление кратных с-с связей
- •2.5.3. Восстановление кратных c-n связей
- •2.5.4. Восстановление кетонов, альдегидов
- •2.5.5. Восстановление сложных эфиров
- •2.5.6. Восстановление азосоединений и солей диазония
- •2.5.7. Восстановление нитрозогрупп
- •2.5.8. Восстановление нитрогрупп
- •2.5.9. Техника безопасности, экология
- •2.6. ОкислениЕ и дегидрированиЕ
- •2.6.1. Реакции окисления
- •При синтезе никотиновой кислоты (витамина рр) окисление азотной кислотой не приводит к желаемому результату. Приходится использовать более сильный окислитель – перманганат калия:
- •2.6.2. Дегидрирование
- •Следует отметить интересный метод ароматизации дигидропиразола, приведенный на схеме:
- •2.6.3. Техника безопасности, экология
- •2.7. Реакции конденсации и гетероциклизации
- •2.7.1. Реакции конденсации
- •2.7.2. Реакции гетероциклизации
- •2.7.3. Синтез лекарственных препаратов
- •2.8. Основные концепции комбинаторной химии
- •Твердофазный синтез
- •2.8.2. Метод параллельных синтезов
2.4.2. Строение солей диазония, реакционная способность
Как видно из формулы соли диазония, положительный заряд находится на атоме азота, связанного с ароматическим ядром. Но все реакции с нуклеофилами идут по крайнему атому азота, формально не имеющему положительного заряда. Квантово-химические расчеты (метод CNDO) показали, что на этом азоте положительный заряд есть, хотя и меньший, чем на первом:
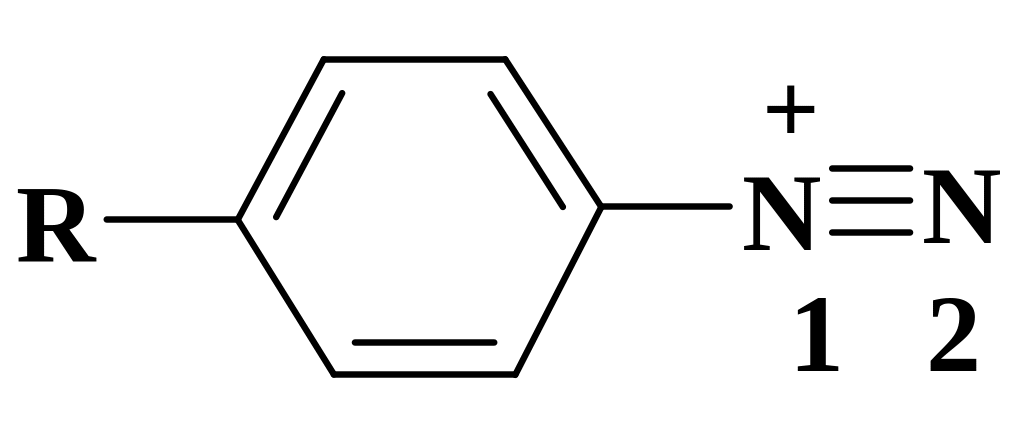
R= CH3 q2 = + 0,207; q1 = + 0,284 EНСМО = - 3,9 эВ ЕВЗМО = - 19,4 эВ
Н q2 = + 0,209; q1 = + 0,288 EНСМО = - 4,9 эВ ЕВЗМО = - 19,6 эВ
NO2 q2 = + 0,235; q1 = + 0,298 EНСМО = - 7,2 эВ ЕВЗМО = - 19,9 эВ
Более точные данные, полученные с помощью неэмпирического расчета STO-3G, показывают наличие положительного заряда на втором атоме азота (+ 0,279), который больше чем на первом (+0,083):
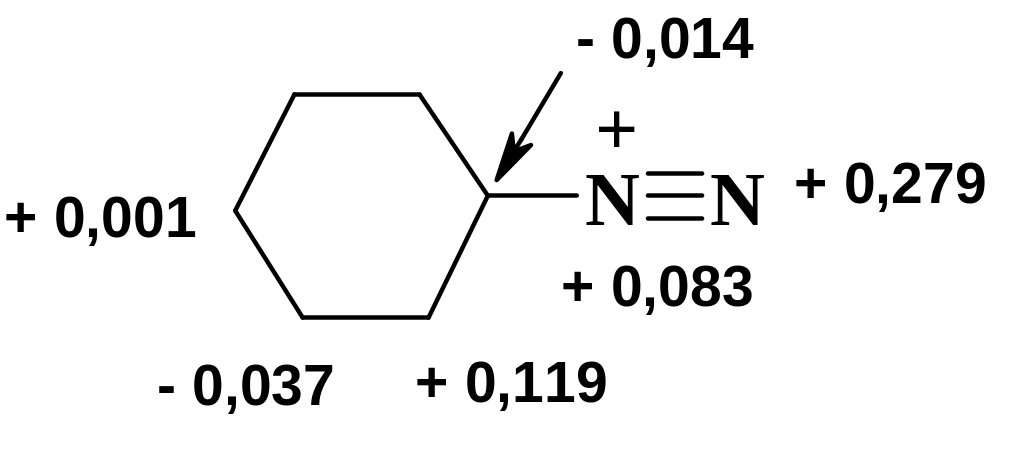
При попытке корреляции величины заряда на терминальном атоме азота с реакционной способностью в реакции азосочетания оказалось, что корреляция полностью отсутствует. В работах И.Л. Багала было показано, что реакционная способность определяется величиной энергии низшей свободной орбитали молекулы. Соли диазония являются самыми "мягкими" реагентами (в терминах ЖМКО), и реакции идут при орбитальном контроле. Введение электроноакцепторных заместителей уменьшает ЕНСМО и увеличивает реакционную способность, электронодонорные заместители действуют наоборот.
Следует отметить, что единственной реакционноспособной формой является соль диазония. В то же время при увеличении рН происходят прототропные превращения, уменьшающие концентрацию соли диазония.
При повышении рН до 3 – 5 к молекуле арилдиазоний хлорида присоединяется гидроксид анион и образуется Z-диазогидроксид (син-, цис-диазогидроксид), который находится в равновесии с солью диазония и Z-диазотатом. При этом в растворе свободный диазогидроксид содержится в пределах от 0,5 до 20 %. При дальнейшем повышении рН равновесие смещается в сторону Z-диазотата и при рН 11 – 14 это соединение становится основным. Медленно Z-диазотат переходит в более устойчивый Е-диазотат, обратный переход возможен в фотохимических условиях. Одной из устойчивых форм диазосоединений являются Е-диазотаты натрия. При подкислении они превращаются в нитрозамины, а не в диазогидроксиды. Нитрозамины при подкислении дают соль диазония и частично разлагаются до амина.
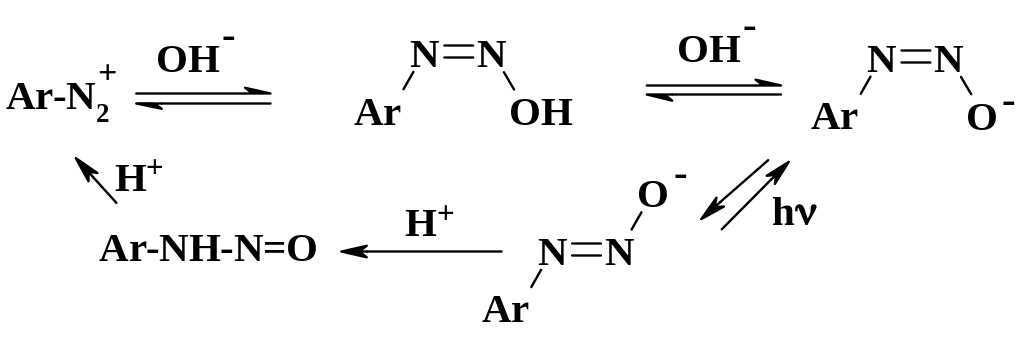
Прототропные переходы необходимо учитывать при проведении реакций солей диазония.
2.4.3. Реакция азосочетания
Одной из важнейших реакций солей диазония является азосочетание, которое используется, как отмечалось в начале раздела, в синтезе препаратов салазодиметоксин, салазопиридазин, мескамин, триазотрин и витамина В2. В настоящее время по-прежнему выпускаются тысячи тонн азокрасителей. Обычно соль диазония называют диазосоставляющей, а субстрат азосоставляющей. Азосочетание является типичной реакцией электрофильного замещения.
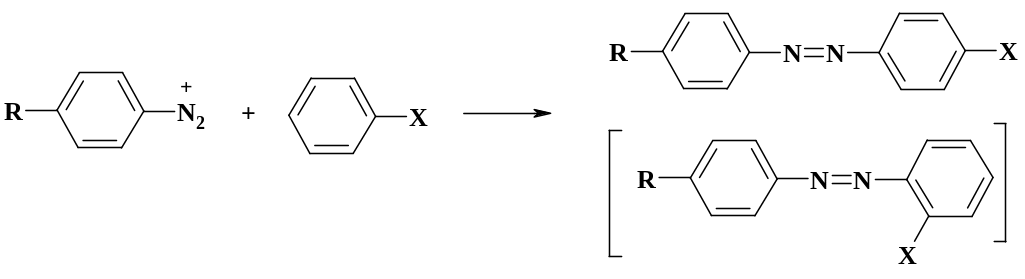
Заместитель Х должен обладать сильным электронодонорным характером – OH, NH2, NR1R2. Если Х = OCH3, CH3, то реакция идет только с наиболее реакционноспособными диазосоставляющими, такими, как пикрилдиазоний сульфат (три нитрогруппы в молекуле), или гетероциклическими солями диазония, у которых гетероцикл обладает сильным электроноакцепторным характером. При Х = Н, COOH и тем более NO2 реакция не идет. Естественно, азогруппа вступает в о-, п-положение по отношению к электронодонорному заместителю Х. Реакцию с фенолами ведут в слабощелочной среде, с аминами – в слабокислой. Это объясняется тем, что величина ЕВЗМО производных анилина выше, чем энергия производных фенола с теми же заместителями, однако существенно ниже величины ЕВЗМО фенолят иона.
ЕВЗМО (ArO-) >> ЕВЗМО (ArNH2) > ЕВЗМО (Ar-OH)
При наличии в одной молекуле азосоставляющей и гидрокси- и аминогруппы региоселективность обеспечивают за счет проведения реакции при различных значениях рН. Сочетание в о-, п-положение к фенольной группе проводят в слабощелочной среде, а азосочетание в о-, п-положение к аминогруппе – в слабокислой среде. Если рассмотреть величину коэффициента АОВЗМО на атомах углерода в молекуле, содержащей как амино-, так и гидроксигруппу, то в неионизированной молекуле величина коэффициента АОВЗМО в о- или п-положениях к аминогруппе выше, чем на атомах углерода в о- или п-положениях к гидроксигруппе. Ситуация меняется на обратную при превращении фенола в фенолят ион.
Наряду с ароматическими азосоставляющими, реакция сочетания идет и с СН-кислотами. Некоторые диазосоединения азолов реагируют аналогично арильным солям диазония, их соли диазония существенно более реакционноспособны.
Лимитирующей стадией процесса азосочетания в зависимости от условий его проведения является как образование -аддукта, так и отрыв протона. В общем случае скорость реакции может быть описана следующим уравнением
V = k1k2[ArN2+][ArX][B]/k-1+k2[B]
где k1 – константа скорости образования -аддукта, k2 – константа скорости отрыва протона, B – основание, k -1 – константа скорости обратной реакции.
Нами для гетероциклических и ароматических азосоединений было показано, что в уксусной кислоте в присутствии толуолсульфокислоты реакция азосочетания является обратимой.
Технология реакций азосочетания. В первую очередь необходимо учитывать, что к моменту окончания процесса диазотирования аппаратура для проведения азосочетания должна быть полностью подготовлена. Реакцию проводят при температуре 10 – 15 oС в емкостных аппаратах, снабженных рубашкой для охлаждения, рамной или якорной мешалкой.
При сочетании с фенолами при рН 7 – 10 к раствору азосоставляющей приливают раствор соли диазония (прямой порядок смешения). Температурный режим регулируют скоростью прибавления реагентов. При сочетании с аминами вначале готовят раствор или тонкую суспензию амина и постепенно добавляют к раствору соли диазония. Значение рН поддерживают в пределах 3 – 6 за счет одновременного прибавления раствора соды (обратный порядок смешения реагентов). Для предотвращения образования триазена из незамещенного или монозамещенного амина реакцию проводят при возможно более низких значениях рН или вводят в аминогруппу защитные группировки. При целенаправленном получении триазена реакцию ведут в органическом растворителе, например, в хлористом метилене или метаноле. При получении противоопухолевого препарата дакарбазина суспензию диазоимидазолкарбоксамида в метаноле добавляют к метанольному раствору диметиламина при низкой температуре. Как диазосоединение, так и дакарбазин высокопожаро- и взрывоопасны. По чувствительности к удару, удару со смещением они близки штатным взрывчатым веществам, а по чувствительности к искре к паровоздушным смесям к ЛВЖ. Поэтому вся аппаратура должна быть заземлена и выполнена в пожаробезопасном исполнении.
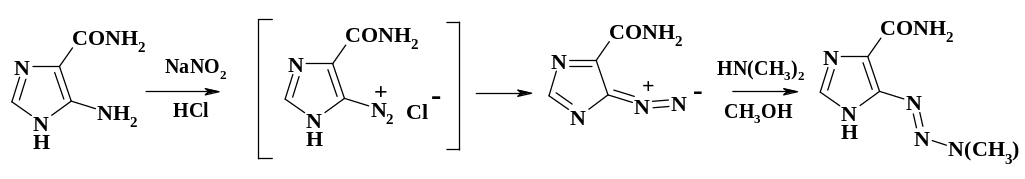
В митохондриях печени происходит гидроксилирование одной из метильных групп дакарбазина, отщепление гидрокисметильной группы, распад монотриазена до диазометана. Диазометан алкилирует гуанин ДНК, что приводит к необратимым изменениям раковой клетки.
В медицинской промышленности реакция азосочетания используется в производстве салазопиридазина и салазодиметоксина. Сульфапиридазин или сульфадиметоксин растворяют в щелочи, добавляют нитрит натрия и полученный раствор медленно приливают в охлажденную до 0 oС соляную кислоту. К выпавшей в осадок соли диазония при температуре 0 – 5 oС в один прием приливают раствор салициловой кислоты в щелочи.
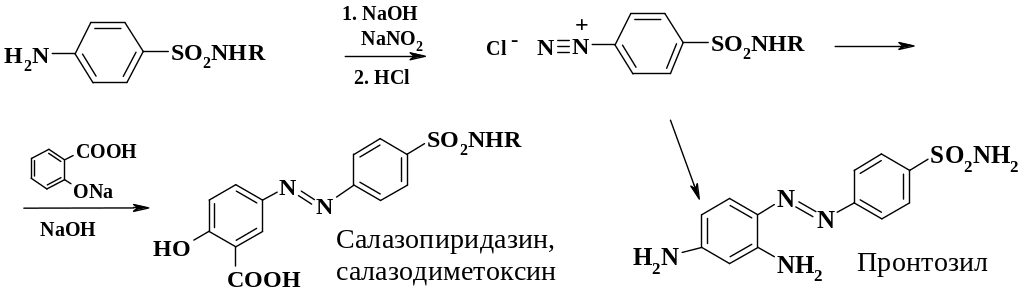
В организме азосоединения восстанавливаются до исходного сульфаниламида и аминосалициловой кислоты, также обладающей биологической активностью. Следует отметить, что первым сульфаниламидом был пронтозил (красный стрептоцид) – краситель хлопчатобумажных тканей, который получали сочетанием 1,3-фенилендиамина с п-диазобензолсульфаниламидом (R = H). Окрашенные им ткани обладали бактерицидным действием и заживляли гнойные раны. Вначале красный стрептоцид использовали в неизмененном виде. Но образующийся в организме 1,2,4-триаминобензол является токсичным соединением. Позднее было выяснено, что п-аминосульфаниламид обладает более высокой активностью, и белый стрептоцид стал применяться в практике. Это положило начало эры сульфаниламидных препаратов.
Так же, как и в организме, химически азогруппа может быть восстановлена, давая два ароматических амина. Этот синтетический прием используют при получении витамина В2 – рибофлавина. Рибитиланилин сочетают с фенилдиазоний хлоридом. Полученное азосоединение конденсируют с барбитуровой кислотой. Следует отметить, что реакцию азосочетания ведут при рН 3 – 4 для того, чтобы предотвратить N-азосочетание.
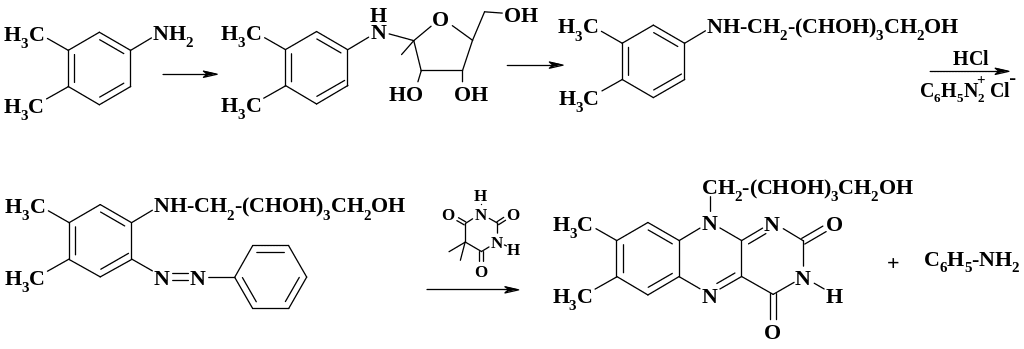
При конденсации азосоединения с барбитуровой кислотой последняя выполняет роль восстановителя азогруппы (подробно методы синтеза рибофлавина рассмотрены в разделе 3.5).
Реакцию азосочетания с СН-кислотами используют при получении препарата мескамин (радиопротектор – профилактическое средство, предупреждающее возникновение лучевой болезни), а также при синтезе серотонина. Синтез мескамина (5-метокситриптамина) представлен на схеме:
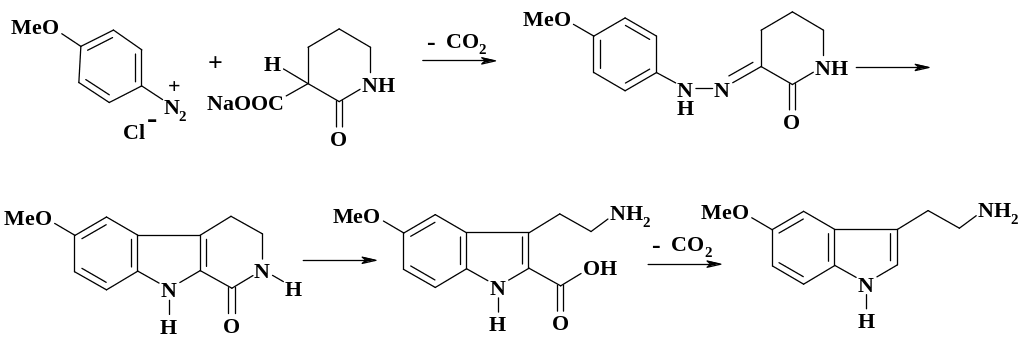
В обычных условиях диазотируют п-анизидин и раствор диазосоединения приливают к щелочному раствору 3-карбоксипиперидона-2 при температуре от 0 до минус 2 oС. При азосочетании одновременно происходит декарбоксилирование. Полученный гидразон при действии кислотного катализатора по реакции Фишера превращается в 5-метокситетрагидро-β-карболинон. Под действием щелочи происходит раскрытие пиперидонового цикла. Для получения мескамина проводят декарбоксилирование последнего продукта кипячением в соляной кислоте в атмосфере азота.
В синтезе 5-аминоимидазол-4-карбоксамида, который является биогенным предшественником пуринов, а также в синтезе противоопухолевых препаратов дакарбазина и 6-меркаптопурина (полная схема синтеза этих соединений приведена в разделе 2.7) для введения аминогруппы используют сочетание фенилдиазоний хлорида с малонамидинамидом:
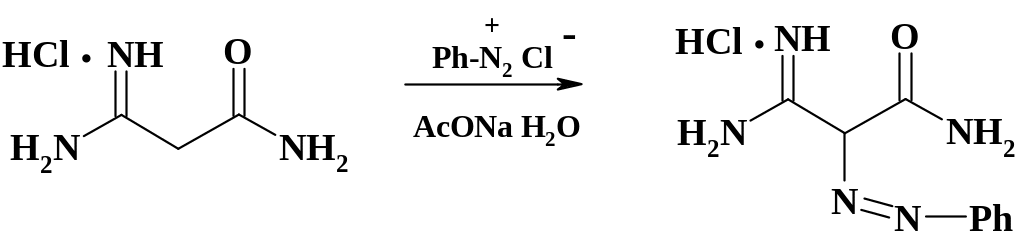
В молекуле исходного соединения имеются NH- группы и СН2-группа, по которым может пойти сочетание. В условиях реакции гидрохлорид не переходит в основание и этот центр оказывается блокированнным, поэтому идет только С- сочетание. Осадок красителя отфильтровывают.
Препарат триазотрин является антагонистом метаболитов пуринового обмена, обладает широким спектром противовирусной активности. Его синтез включает азосочетание гетероциклической соли диазония с нитромалоновым эфиром:
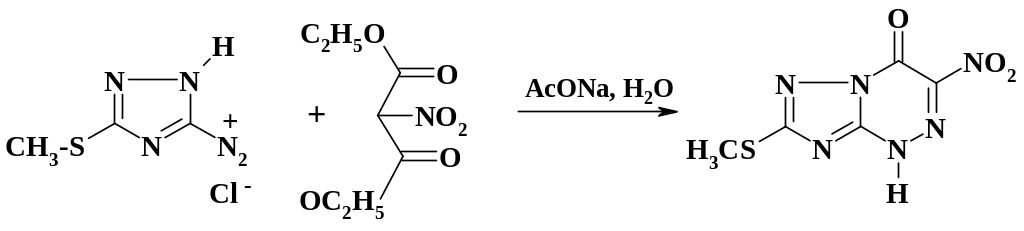
В процессе реакции при сочетании происходит гидролиз одной из эфирных групп, декарбоксилирование и циклизация.
